Cho 0.01 mol một hợp chất của sắt tác dụng hết với H2SO4 đặc nóng dư thoát ra 0.112 l SO2 là sản phẩm khử duy nhất . Công thức của hợp chất sắt đó là
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án D
Quan sát 4 đáp án và kết hợp với giả thiết khí thoát ra chỉ có SO2 ta có hợp chất cần tìm là FeO hoặc hợp chất của sắt với lưu huỳnh (nếu là FeCO3 thì có thêm khí CO2).
Nếu hợp chất đó là FeO thì áp dụng định luật bảo toàn mol electron, ta có:
![]() mà
mà 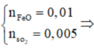 Thỏa mãn
Thỏa mãn
Khi hợp chất cần tìm có dạng FeSx thì khí SO2 sinh ra tù hợp chất FeSx là 0,01x.
Khi đó khí thu được có lượng SO2 là sản phẩm khử (sản phẩm được tạo thành từ H2SO4) là:
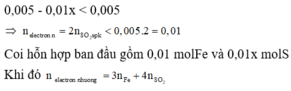
= 0,03 + 0,04x > 0,01 > nelectron nhận
Do đó trường hợp này loại.

Đáp án D
Quan sát 4 đáp án và kết hợp với giả thiết khí thoát ra chỉ có SO2 ta có hợp chất cần tìm là FeO hoặc hợp chất của sắt với lưu huỳnh (nếu là FeCO3 thì có thêm khí CO2).
Nếu hợp chất đó là FeO thì áp dụng định luật bảo toàn mol electron, ta có:
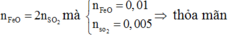
Khi hợp chất cần tìm có dạng FeSx thì khí SO2 sinh ra tù hợp chất FeSx là 0,01x.
Khi đó khí thu được có lượng SO2 là sản phẩm khử (sản phẩm được tạo thành từ H2SO4) là:
0,005 - 0,01x < 0,005
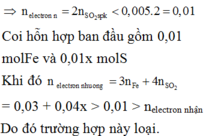






SO2=0.05 mol.
Gọi hợp chất là : FexOy.
Bảo toàn e ta có : x Fe+2y/x \(\rightarrow\) xFe+3 +(3x-2y)e
0.01 mol \(\rightarrow\) 0.01(3x-2y) mol
S+6 +2e\(\rightarrow\)S+4
0.01mol \(\leftarrow\) 0.005 mol
theo bảo toàn e : 0.01(3x-2y)= 0.01\(\Rightarrow\) 3x-2y=1.Chọn x=1,y=1\(\Rightarrow\) công thức FeO
nSO2=0,005 mol
S+6 +2e => S+4
0,01 mol<=0,005 mol
nh/c của sắt=0,01 mol
+) nếu hợp chất của sắt là của Fe+2 =>tm vì Fe+2 nhường 1e thành Fe+3 nhưng SẢN PHẨM KHỬ DUY NHẤT CHỈ CÓ SO2 nên hợp chất của Fe+2 là FeO hoặc FeSO4
+) nếu hợp chất của Fe+3 =>ko tm vì ko nhường electron
+) nếu là Fe3O4 =>nFe+8/3=0,03 mol
3Fe+8/3 =>3Fe+3 +e
0,03 mol =>0,01 mol
ne nhường=ne nhận=0,01 mol=>tm
Vây có FeO FeSO4 Fe3O4 tm