Cho 9,52g hỗn hợp E có công thức C8H8O2 tác dụng vừa đủ với 0,1 mol NaOH tạo thành ancol R' và 3 muối.Đốt cháy R' tạo ra 0,896 lít khí CO2. Tính khối lượng của 3 muối
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án D
X: C8H8O2 (Δ = 5) ; X chứa nhân thơm
X tác dụng với NaOH theo tỉ lệ 1 : 2 nên X là este của phenol hoặc X có 2 nhóm –OH trên vòng.
Các CTCT của X:
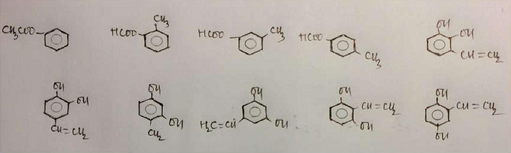

Đáp án : C
X là ancol 2 chức => nX = nE = 0,1 mol
=> MX = 6 , 2 0 , 1 = 62 => X là etylen glycol CH2OH - CH2OH
E + 2NaOH → C2H3O2Na + C3H3O2Na + C2H6O2
Bảo toàn nguyên tố => E có công thức: C7H10O4

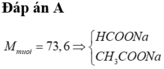
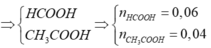
n Ag = 0 , 24 mol
Từ 4 đáp án, Y là ancol đơn chức
Nếu Y là CH3OH
![]()
Như vậy, 2 chất là HCOOCH3 và CH3COOH
Nếu Y không phải CH3OH
![]()

Đáp án : C
X là ancol 3 chức , nX = nE = 0,1 mol
=> MX = 9 , 2 0 . 1 = 92 => X là C3H5(OH)3 (Glyxerol)
E + 3NaOH à CHO2Na + C2H3O2Na + C3H3O2Na + C3H8O3
Bảo toàn nguyên tố => E là : C9H12O6



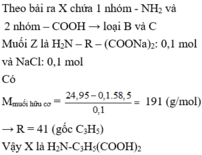
$n_E = \dfrac{9,52}{136} = 0,07(mol)$
Gọi neste tao ancol = a(mol) ; neste tao phenol = b(mol)
Ta có :
a + b = 0,07 và a + 2b = 0,1
Suy ra a = 0,04 ; b = 0,03
Ta thấy
$n_{este\ tạo\ ancol} = n_{CO_2} = 0,04$
Suy ra : R' là $CH_3OH$
Bảo toàn khối lượng :
$m = 9,52 + 0,1.40 - 0,04.32 - 0,03.18 = 11,7(gam)$
\(n_{C_8H_8O_2}=\dfrac{9,52}{136}=0,07\left(mol\right)\)
\(n_{CO_2}=\dfrac{0,896}{22,4}=0,04\left(mol\right)\)
Vì hỗn hợp E tác dụng với NaOH =>ancol R' và 3 muối
Hỗn hợp E chứa este của ancol và este của phenol
Gọi x,y lần lượt là số mol este của ancol và este của phenol
Ta có : \(\left\{{}\begin{matrix}x+y=0,07\\x+2y=0,1\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}x=0,04\\y=0,03\end{matrix}\right.\)
=> nR'=0,04(mol)
C8H8O2 + 2NaOH → C6H5ONa + C2H3O2Na + H2O
=> nH2O=0,03 (mol)
Ta có : số C ancol = \(\dfrac{n_{CO2}}{n_{ancol}}=\dfrac{0,04}{0,04}=1\)
=> Ancol là CH3OH
Ta có : E + NaOH ---------> 3 muối + CH3OH + H2O
Bảo toàn khối lượng ta có :\(m_{3muoi}=9,52+0,1.40-0,04.32-0,03.18=11,7\left(g\right)\)