Hoà tan hoàn toàn 10,2 gam Al2O3 trong dung dịch HNO3 15% a) Tính khối lượng dung dịch HNO3 phản ứng b) Tính số phân tử nước tạo thành mn giúp mình với
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(n_{Al}=\dfrac{10,2}{102}=0,1\left(mol\right)\)
PTHH: Al2O3 + 6HNO3 ---> 2Al(NO3)3 + 3H2O
0,1 0,6 0,2 0,3
\(\rightarrow m_{HNO_3}=0,6.63=37,8\left(g\right)\\ m_{ddHNO_3}=\dfrac{37,8}{15\%}=252\left(g\right)\\ m_{dd\left(sau.pư\right)}=252+10,2=262,2\left(g\right)\\ m_{Al\left(NO_3\right)_3}=0,2.213=42,6\left(g\right)\\ C\%_{Al\left(NO_3\right)_3}=\dfrac{42,6}{262,2}=16,25\%\)

a)
Gọi số mol Al2O3 và ZnO là a,b
=> 102a + 81b = 26,4
nHNO3 = 0,2.5 = 1 (mol)
PTHH: Al2O3 + 6HNO3 --> 2Al(NO3)3 + 3H2O
_______a----->6a----------->2a
ZnO + 2HNO3 --> Zn(NO3)2 + H2O
_b---->2b---------->b
=> 6a + 2b = 1
=> a = 0,1 ; b = 0,2
=> \(\left\{{}\begin{matrix}m_{Al_2O_3}=0,1.102=10,2\left(g\right)\\m_{ZnO}=0,2.81=16,2\left(g\right)\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}\%Al_2O_3=\dfrac{10,2}{26,4}.100\%=38,636\%\\\%ZnO=\dfrac{16,2}{26,4}.100\%=61,364\%\end{matrix}\right.\)
b)
\(\left\{{}\begin{matrix}n_{Al\left(NO_3\right)_3}=0,2\left(mol\right)\\n_{Zn\left(NO_3\right)_2}=0,2\left(mol\right)\end{matrix}\right.\)
PTHH: 4Al(NO3)3 --to--> 2Al2O3 + 12NO2 + 3O2
________0,2------------->0,1
2Zn(NO3)2 --to--> 2ZnO + 4NO2 + O2
__0,2------------->0,2
=> mrắn = 0,1.102 + 0,2.81 = 26,4 (g)

Xét phản ứng Mg tác dụng với dd HNO3, nhận thấy mY tăng=mMg - mX
suy ra mX=3,6-3,04=0,56(gam)
lại có nX=0,448/22,4=0,02(mol) \(\Rightarrow\) MX=0,56/0,02=28
\(\Rightarrow\) X là khí N2
Dễ dàng tìm được dung dịch Y chứa Mg(NO3)2 ; NH4NO3 ; HNO3 dư
Bạn dùng bảo toàn e để tìm số mol NH4NO3
dùng bảo toàn nguyên tố N để tìm HNO3 dư
\(n_{NaOH}=n_{NH_4NO_3}+2n_{Mg\left(NO_3\right)2}+n_{HNO_3dư}\)

a)
\(n_{NO} = 0,01(mol)\)
Bảo toàn electron : \(2n_{Cu} = 3n_{NO}\)
\(\Rightarrow n_{Cu} = 0,015(mol)\)
Vậy :
\(\%m_{Cu} = \dfrac{0,01.64}{1,98}.100\% = 32,32\%\\ \%m_{Al_2O_3} = 100\% - 32,32\% = 67,68\%\)
b)
\(n_{Al_2O_3} = \dfrac{1,98-0,015.64}{102} = 0,01(mol)\)
\(n_{OH^-} = n_{NaOH} + 2n_{Ba(OH)_2} = 0,1.1 + 0,5.0,1.2 = 0,2(mol)\)
Ta có :
\(n_{Cu(NO_3)_2} = n_{Cu} = 0,015(mol)\\ n_{Al(NO_3)_3} = 2n_{Al_2O_3} = 0,02(mol)\)
Mà : \(n_{OH^-} = 4n_{Al(NO_3)_3} + 2n_{Cu(NO_3)_2} + n_{HNO_3\ dư}\)
\(\Rightarrow n_{HNO_3\ dư} = 0,09(mol)\)
Bảo toàn nguyên tố với N :
\(n_{HNO_3\ pư} = 3n_{Al(NO_3)_3} + 2n_{Cu(NO_3)_2} = 0,06(mol)\)
Vậy, \(V = \dfrac{0,09 + 0,06}{1} = 0,15(lít)\)

a) \(n_{SO_3}=\dfrac{3,2}{80}=0,04\left(mol\right)\)
PTHH: SO3 + H2O --> H2SO4
0,04------------->0,04
=> \(m_{H_2SO_4}=0,04.98=3,92\left(g\right)\)
b) \(n_{Na}=\dfrac{0,69}{23}=0,03\left(mol\right)\)
PTHH: 2Na + 2H2O --> 2NaOH + H2
0,03------------>0,03
2NaOH + H2SO4 --> Na2SO4 + 2H2O
Xét tỉ lệ: \(\dfrac{0,03}{2}< \dfrac{0,04}{1}\)=> NaOH hết, H2SO4 dư
2NaOH + H2SO4 --> Na2SO4 + 2H2O
0,03------>0,015---->0,015
\(\left\{{}\begin{matrix}n_{Na_2SO_4}=0,015\left(mol\right)\\n_{H_2SO_4\left(dư\right)}=0,025\left(mol\right)\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}m_{Na_2SO_4}=0,015.142=2,13\left(g\right)\\m_{H_2SO_4}=0,025.98=2,45\left(g\right)\end{matrix}\right.\)
c) \(n_{Na}=\dfrac{2,07}{23}=0,09\left(mol\right)\)
PTHH: 2Na + 2H2O --> 2NaOH + H2
0,09-------------->0,09
Xét tỉ lệ: \(\dfrac{0,09}{2}>\dfrac{0,04}{1}\) => NaOH dư, H2SO4 hết
2NaOH + H2SO4 --> Na2SO4 + 2H2O
0,08<-----0,04------>0,04
=> \(\left\{{}\begin{matrix}n_{NaOH\left(dư\right)}=0,01\left(mol\right)\\n_{Na_2SO_4}=0,04\left(mol\right)\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}m_{NaOH\left(dư\right)}=0,01.40=0,4\left(g\right)\\m_{Na_2SO_4}=0,04.142=5,68\left(g\right)\end{matrix}\right.\)
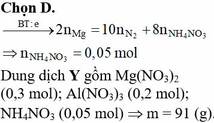
\(n_{Al_2O_3}=\dfrac{10.2}{102}=0.1\left(mol\right)\)
\(Al_2O_3+6HNO_3\rightarrow2Al\left(NO_3\right)_3+3H_2O\)
\(0.1...........0.6..................................0.3\)
\(m_{dd_{HNO_3}}=\dfrac{0.6\cdot63\cdot100}{15}=252\left(g\right)\)
Số phân tử nước :
\(0.3\cdot6\cdot10^{23}=1.8\cdot10^{23}\left(pt\right)\)
a)
n Al2O3 = 10,2/102 = 0,1(mol)
$Al_2O_3 + 6HNO_3 \to 2Al(NO_3)_3 + 3H_2O$
n HNO3 = 6n HNO3 = 0,6(mol)
=> m dd HNO3 = 0,6.63/15% = 252(gam)
b)
n H2O = 3n Al2O3 = 0,3(mol)
Số nguyên tử H2O : N = 0,3.6.1023 = 1,8.1023 phân tử