Cho 6,72 lít CO2 hấp thụ hết bằng 400gam dung dịch KOH 5,6% thu được dd X. Cho dd BaCl2 dư vào X thì được m(g) kết tủa(BaCO3). Tìm m? (Chú ý BaCl2 chỉ tác dụng với K2CO3)
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


![]()
Cho toàn bộ Y tác dụng với dung dịch BaCl2 dư được 11,82 gam kết tủa, đó là BaCO3.
Ta có: 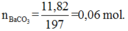
Ta đặt: số mol KOH là: nKOH = 0,1x mol, dd Y chứa KHCO3 = y mol
Nhận thấy ở đây, nếu ta dùng bảo toàn các nguyên tố trước và sau phản ứng thì ta sẽ có các mối liên hệ giữa x và y:
Bảo toàn nguyên tố C ta có:
![]()
Hay 0,1 + 0,02 = 0,06 +y ⇒ y = 0,06 mol
• Bảo toàn nguyên tố K ta được:
![]()
hay 2.0,22+0,1x = 2.0.06+y => x = 1,4
Đáp án B

Đáp án A
nCO2 = 2,24:22,4 = 0,1 mol; nK2CO3 = 0,02 mol; nKOH = 0,1x mol; nBaCO3 = 11,82: 197 = 0,06 mol
Ta thấy: nCO2 + nCO32- (trong K2CO3) = 0,1 + 0,02 > nBaCO3 = 0,06 mol => Hấp thụ CO2 xảy ra 2 PT:
CO2 + OH- → HCO3- (1)
CO2 + 2OH- → CO3 2- + H2O (2)
Bảo toàn nguyên tố C: nCO2 + nK2CO3 = nHCO3- + nBaCO3
=> nHCO3- = 0,1 + 0,02 – 0,06 = 0,06 mol
=> ∑nOH- (1) +(2) = nHCO3- + 2 (nBaCO3 - nK2CO3 ) = 0,06 + 2. ( 0,06 – 0,02) = 0,14 mol
=> CM = n: V = 0,14 : 0,1 = 1,4 M
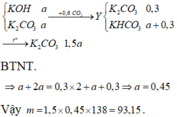
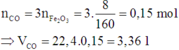
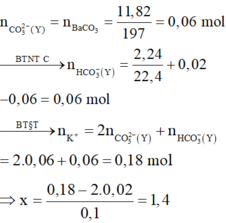


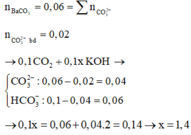
\(n_{CO_2}=\dfrac{6.72}{22.4}=0.3\left(mol\right)\)
\(n_{KOH}=\dfrac{400\cdot5.6\%}{56}=0.4\left(mol\right)\)
\(n_{K_2CO_3}=a\left(mol\right),n_{KHCO_3}=b\left(mol\right)\)
\(2KOH+CO_2\rightarrow K_2CO_3+H_2O\)
\(KOH+CO_2\rightarrow KHCO_3\)
\(\left\{{}\begin{matrix}2a+b=0.4\\a+b=0.3\end{matrix}\right.\)
\(\Leftrightarrow\left\{{}\begin{matrix}a=0.1\\b=0.2\end{matrix}\right.\)
\(K_2CO_3+BaCl_2\rightarrow BaCO_3+2KCl\)
\(0.1...............................0.1\)
\(m_{BaCO_3}=0.1\cdot197=19.7\left(g\right)\)
Ta có : \(n_{CO2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
\(n_{KOH}=\dfrac{400.5,6}{56.100}=0,4\left(mol\right)\)
\(\dfrac{n_{KOH}}{n_{CO2}}=\dfrac{0,4}{0,3}=\dfrac{4}{3}\Rightarrow\)Tạo 2 muối
\(CO2+2KOH\rightarrow K2CO3+H2O\)
x---------->2x-------->x(mol)
\(CO2+KOH\rightarrow KHCO3\)
y-------->y------------->(mol)
Theo bài ta có HPT\(\left\{{}\begin{matrix}x+y=0,3\\2x+y=0,4\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,1\\y=0,2\end{matrix}\right.\)
\(K2CO3+BaCl2\rightarrow BaCO3+2KCl\)
0,1--------------------------->0,1(mol)
\(\Rightarrow m=m_{BaCO3}=0,1.197=19,7\left(g\right)\)
Chúc bạn học tốt ^.^