Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\)
a) Pt : \(Zn+2HCl\rightarrow ZnCl_2+H_2|\)
1 2 1 1
0,2 0,4 0,2 0,2
b) \(n_{HCl}=\dfrac{0,2.2}{1}=0,4\left(mol\right)\)
⇒ \(m_{HCl}=0,4.36,5=14,6\left(g\right)\)
\(C_{ddHCl}=\dfrac{14,6.100}{100}=14,6\)0/0
c) \(n_{ZnCl2}=\dfrac{0,4.1}{2}=0,2\left(mol\right)\)
⇒ \(m_{ZnCl2}=0,2.136=27,2\left(g\right)\)
\(m_{ddspu}=13+100-\left(0,2.2\right)=112,6\left(g\right)\)
\(C_{ZnCl2}=\dfrac{27,2.100}{112,6}=24,16\)0/0
Chúc bạn học tốt
\(n_{Zn}=\dfrac{13}{65}=0.2\left(mol\right)\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(0.2........0.4..........0.2.......0.2\)
\(m_{HCl}=0.4\cdot36.5=14.6\left(g\right)\)
\(C\%_{HCl}=\dfrac{14.6}{100}\cdot100\%=14.6\%\)
\(m_{ZnCl_2}=0.2\cdot136=27.2\left(g\right)\)
\(m_{\text{dung dịch sau phản ứng}}=13+100-0.2\cdot2=112.6\left(g\right)\)
\(C\%_{ZnCl_2}=\dfrac{27.2}{112.6}\cdot100\%=24.1\%\)

\(n_{Fe_2O_3}=\dfrac{20}{160}=0,125\left(mol\right)\)
PTHH:
\(Fe_2O_3+3H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+3H_2O\)
0,125 0,375 0,125 0,375
\(m_{ddH_2SO_4}=\dfrac{0,375.98.100}{25}=147\left(g\right)\)
\(C\%_{Fe_2\left(SO_4\right)_3}=\dfrac{0,125.406}{20+147}\approx30,39\%\)

a, \(Mg+2HCl\rightarrow MgCl_2+H_2\)
b, Ta có: \(n_{Mg}=\dfrac{2,4}{24}=0,1\left(mol\right)\)
Theo PT: \(n_{HCl}=2n_{Mg}=0,2\left(mol\right)\Rightarrow C\%_{HCl}=\dfrac{0,2.36,5}{400}.100\%=1,825\%\)
c, Theo PT: \(n_{MgCl_2}=n_{H_2}=n_{Mg}=0,1\left(mol\right)\)
Ta có: m dd sau pư = 2,4 + 400 - 0,1.2 = 402,2 (g)
\(\Rightarrow C\%_{MgCl_2}=\dfrac{0,1.95}{402,2}.100\%\approx2,36\%\)

\(a,m_{Na_2CO_3}=\dfrac{500.20}{100}=100\left(g\right)\\ \rightarrow n_{Na_2CO_3}=\dfrac{100}{106}=\dfrac{50}{53}\left(mol\right)\)
PTHH: \(Na_2CO_3+2CH_3COOH\rightarrow2CH_3COONa+CO_2\uparrow+H_2O\)
\(\dfrac{50}{53}\)------->\(\dfrac{100}{53}\)--------------->\(\dfrac{100}{53}\)-------------->\(\dfrac{50}{53}\)
\(b,m_{axit}=\dfrac{100}{53}.60=\dfrac{6000}{53}\left(g\right)\\ c,m_{dd}=500+400-\dfrac{50}{53}.44=\dfrac{45500}{53}\left(g\right)\\ m_{CH_3COONa}=\dfrac{100}{53}.82=\dfrac{8200}{53}\left(g\right)\\ \rightarrow C\%_{CH_3COONa}=\dfrac{\dfrac{8200}{23}}{\dfrac{45500}{23}}.100\%=18,02\%\)

nCuO=16/80=0,2(mol)
a) PTHH: CuO + 2HCl-> CuCl2 + H2O
0,2__________0,4________0,2(mol)
b) mHCl=0,4.36,5=14,6(g)
=>mddHCl=(14,6.100)/20=73(g)
c) mCuCl2= 135.0,2=27(g)
mddCuCl2= mCuO + mddHCl= 16+73=89(g)
=> C%ddCuCl2=(27/89).100=30,337%
Câu 9 : Số mol của đồng (II) oxit
nCuO = \(\dfrac{m_{CuO}}{M_{CuO}}=\dfrac{16}{80}=0,2\left(mol\right)\)
a) Pt : CuO + 2HCl → CuCl2 + H2O\(|\)
1 2 1 1
0,2 0,4 0,2
b) Số mol của axit clohidric
nHCl = \(\dfrac{0,2.2}{1}=0,4\left(mol\right)\)
Khối lượng của axit clohidric
mHCl = nHCl . MHCl
= 0,4 . 36,5
= 14,6 (g)
Khối lượng của dung dịch axit clohidric
C0/0HCl = \(\dfrac{m_{ct}.100}{m_{dd}}\Rightarrow m_{dd}=\dfrac{m_{ct}.100}{C}=\dfrac{14,6.100}{20}=73\left(g\right)\)
c) Số mol cuả đồng (II) clorua
nCuCl2 = \(\dfrac{0,4.1}{2}=0,2\left(mol\right)\)
Khối lượng của đồng (II) clorua
mCuCl2 = nCuCl2 . MCuCl2
= 0,2. 135
= 27 (g)
Khối lượng của dung dịch sau phản ứng
mdung dịch sau phản ứng = mCuO + HCl
= 16 + 73
= 89 (g)
Nồng độ phần trăm của đồng (II) clorua
C0/0CuCl2 = \(\dfrac{m_{ct}.100}{m_{dd}}=\dfrac{27.100}{89}=30,34\)0/0
Chúc bạn học tốt

a) K2CO3+2HCl---->2KCl+H2O+CO2
b) m K2CO3=300.6,9/100=20,7(g)
n K2CO3=20,7/138=0,15(mol)
n HCl=2n K2CO3=0,3(mol)
m HCl=0,3.36,5=10,95(g)
m ddHCl=10,95.100/7,3=150(g)
c) m dd sau pư=300+150-0,15.44(m CO2)
=433,4(g)
m KCl=0,3.74,5=22,35(g)
C% KCl=22,35/433,4.100%=5,16%

nFe2O3=0.1(mol)
PTHH Fe2O3+6HCl->2FeCl3+3H2O
a)Theo pthh,nHCl=6 nFe2O3->nHCl =0.1*6=0.6(mol)
mHCl=0.6*36.5=21.9(g)
b)nFeCl3=0.2(mol)
mFeCl3=162.5*0.2=32.5(g)
mdd sau phản ứng:248+16=264(g)
C%muối=32.5:264*100=12.3%
nFe2O3 = 16/160 = 0,1 mol
a/ Fe2O3 + 6HCl -----> 2FeCl3 + 3H2O
(mol) 0,1 0,6 0,2
b/ Từ PTHH => nHCl = 6nFe2O3 = 0,6 mol
=> mHCl = 0,6 x 36,5 = 21,9 (g)
c/ nFeCl3 = 2nFe2O3 = 0,2 mol
=> mFeCl3 = 0,2 x 162,5 = 32,5 (g)
=> %FeCl3 = \(\frac{32,5}{248}.100\approx13,105\%\)

a, PTHH: \(Fe_2O_3+6HCl\rightarrow2FeCl_3+3H_2O\)
b. Ta có \(n_{Fe_2O_3}=\frac{16}{160}=0,1\) (mol)
Theo PTHH: \(n_{HCl}=6n_{Fe_2O_3}=6.0,1=0,6\) (mol)
=> \(m_{HCl}=0,6.36,5=21,9\) (g)
c, Theo PTHH: n FeCl3 = 0,2 (mol)
=> m FeCl3 = 0,2 . 162,5 =32,5 (g)
Áp dụng ĐLBTKL ta có:
\(m_{dd-sau-p.ư}=m_{Fe_2O_3}+m_{ddHCl}=16+248=264\left(g\right)\)
=> C% FeCl3 = \(\frac{32,5}{264}.100\%\approx12,31\%\)

a) Fe + 2HCl --> FeCl2 + H2
b) \(n_{Fe}=\dfrac{22,4}{56}=0,4\left(mol\right)\)
PTHH: Fe + 2HCl --> FeCl2 + H2
_____0,4--->0,8------>0,4--->0,4
=> VH2 = 0,4.22,4 = 8,96(l)
c) mHCl = 0,8.36,5 = 29,2 (g)
=> \(m_{dd\left(HCl\right)}=\dfrac{29,2.100}{7,3}=400\left(g\right)\)
mdd (sau pư) = 22,4 + 400 - 0,4.2 = 421,6 (g)
=> \(C\%\left(FeCl_2\right)=\dfrac{127.0,4}{421,6}.100\%=12,05\%\)

Gọi \(\left\{{}\begin{matrix}n_{Mg}=x\\n_{Zn}=y\end{matrix}\right.\)
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3mol\)
\(Mg+2CH_3COOH\rightarrow\left(CH_3COO\right)_2Mg+H_2\)
x 2x x x ( mol )
\(Zn+2CH_3COOH\rightarrow\left(CH_3COO\right)_2Zn+H_2\)
y 2y y y ( mol )
Ta có:
\(\left\{{}\begin{matrix}24x+65y=11,3\\x+y=0,3\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}x=0,2\\y=0,1\end{matrix}\right.\)
\(\rightarrow\left\{{}\begin{matrix}m_{Mg}=0,2.24=4,8g\\m_{Zn}=0,1.65=6,5g\end{matrix}\right.\)
\(\rightarrow\left\{{}\begin{matrix}\%m_{Mg}=\dfrac{4,8}{11,3}.100=42,47\%\\\%m_{Zn}=100\%-42,47\%=57,53\%\end{matrix}\right.\)
\(m_{CH_3COOH}=60.\left(0,2+0,1\right)=18g\)
\(C\%_{CH_3COOH}=\dfrac{18}{200}.100=9\%\)
\(\left\{{}\begin{matrix}m_{\left(CH_3COO\right)_2Mg}=0,2.142=28,4g\\m_{\left(CH_3COO\right)_2Zn}=0,1.183=18,3g\end{matrix}\right.\)
\(m_{ddspứ}=11,3+200-0,3.2=210,7g\)
\(\rightarrow\left\{{}\begin{matrix}C\%_{\left(CH_3COO\right)_2Mg}=\dfrac{28,4}{210,7}.100=13,47\%\\C\%_{\left(CH_3COO\right)_2Zn}=\dfrac{18,3}{210,7}.100=8,68\%\end{matrix}\right.\)
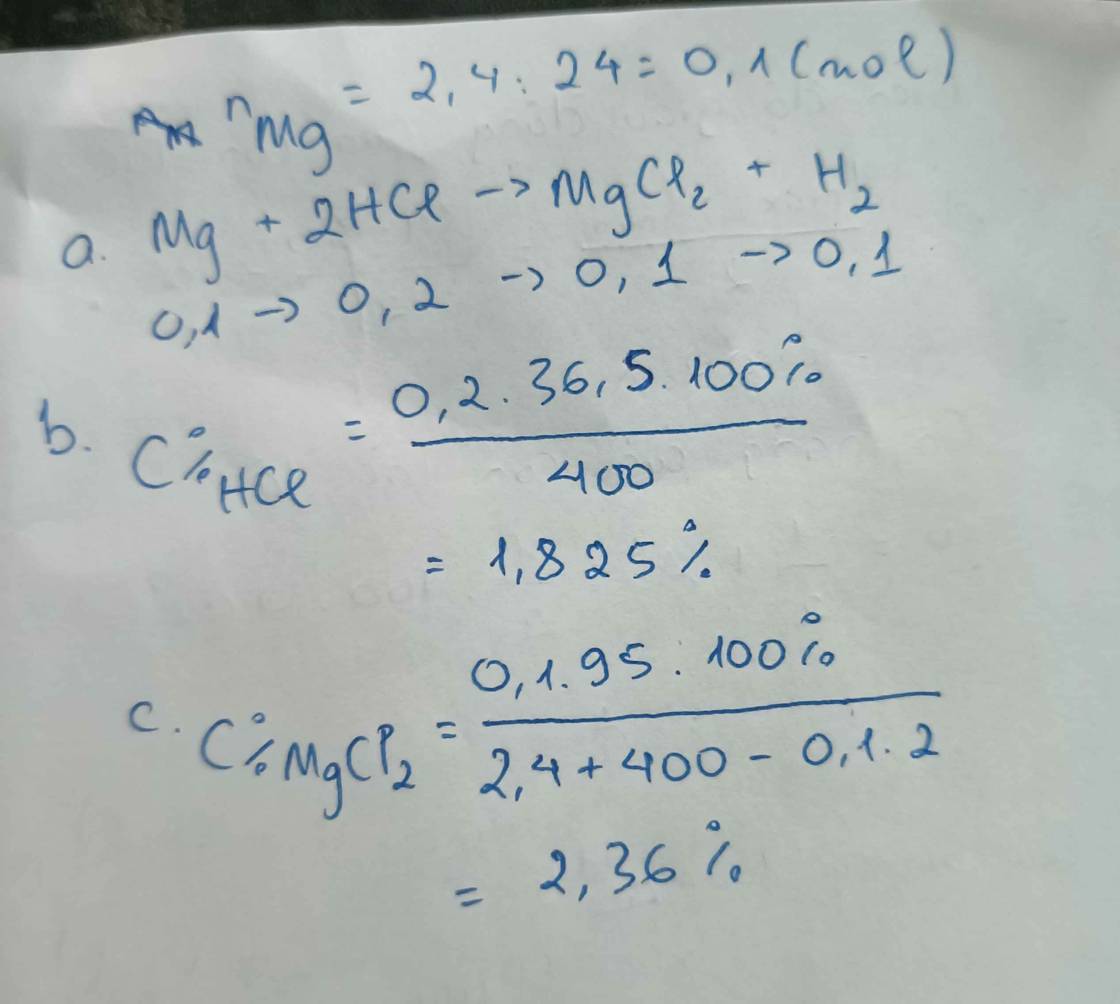
a) ta có phương trình Mg + 2HCl ==> MgCL2 + H2
b) ta đổi 60 kg = 60 000 g
từ câu a) ta có công thức hóa học
Mg + 2HCl ==> MgCl2 + H2
Nồng độ phần trăm của dung dịch sau phản ứng :
Ta có C% = mct / mdd \(\times\)100
=> C% = 48/60 \(\times\) 100 = 80%