Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(m_{HCl}=1,19.500.10=5950g\\ m_{ddHCl\left(37,23\%\right)}=\dfrac{5950}{37,23\%}=159,8g\\ V_{HCl}=159,8:1,19:1,19=112,86ml\)
vậy chọn A

\(a,n_{Zn}=\dfrac{19,5}{65}=0,3mol\\ Zn+2HCl\rightarrow ZnCl_2+H_2\\ n_{H_2}=n_{Zn}=0,3mol\\ V_{H_2}=0,3.24,79=7,437l\\ b,FeO+H_2\xrightarrow[t^0]{}Fe+H_2O\\ n_{FeO}=\dfrac{19,2}{72}=\dfrac{4}{15}mol\\ \Rightarrow\dfrac{0,3}{1}>\dfrac{4:15}{1}\Rightarrow H_2.dư\\ n_{Fe}=n_{FeO}=\dfrac{4}{15}mol\\ m_{Fe}=\dfrac{4}{15}.56\approx14,93g\)

\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
Ta có: \(n_{Al}=\dfrac{0,27}{27}=0,01\left(mol\right)\)
a, \(n_{HCl}=3n_{Al}=0,03\left(mol\right)\Rightarrow m_{HCl}=0,03.36,5=1,095\left(g\right)\)
b, \(n_{H_2}=\dfrac{3}{2}n_{Al}=0,015\left(mol\right)\Rightarrow V_{H_2}=0,015.24,79=0,37185\left(l\right)\)
`#3107.101107`
2.
a)
Số mol của Al trong pứ cần dùng là:
\(\text{n}_{\text{Al}}=\dfrac{\text{m}_{\text{Al}}}{\text{M}_{\text{Al}}}=\dfrac{0,27}{27}=0,01\left(\text{mol}\right)\)
PTHH: \(\text{2Al + 6HCl }\longrightarrow \text{2AlCl}_3+\text{3H}_2\)
Theo pt: 2 : 6 : 2 : 3
`=>` n của HCl cần dùng trong pứ trên là `0,03` mol
Khối lượng của HCl trong pứ đã dùng là:
\(\text{m}_{\text{HCl}}=\text{n}_{\text{HCl}}\cdot\text{M}_{\text{HCl}}=0,03\cdot36,5=1,095\left(g\right)\)
b)
Theo pt: `2` mol Al pứ thu được `3` mol H2
`=>` n của H2 thu được sau pứ là `0,015` mol
Thể tích của khí H2 ở đkc là:
\(\text{V}_{\text{H}_2}=\text{n}_{\text{H}_2}\cdot24,79=0,015\cdot24,79=0,37185\left(l\right)\)
Vậy:
a) `1,095` g
b) `0,37185` l.

Ta có: \(n_{Mg}=\dfrac{2,4}{24}=0,1\left(mol\right)\)
PT: \(Mg+2HCl\rightarrow MgCl_2+H_2\)
_____0,1_____0,2___________0,1 (mol)
a, \(V_{H_2}=0,1.24,79=2,479\left(l\right)\)
b, \(C_{M_{HCl}}=\dfrac{0,2}{1}=0,2\left(M\right)\)

a) Mg + H2SO4 --> MgSO4 + H2
b) \(n_{Mg}=\dfrac{14,4}{24}=0,6\left(mol\right)\)
PTHH: Mg + H2SO4 --> MgSO4 + H2
0,6--->0,6------->0,6----->0,6
=> \(m_{H_2SO_4}=0,6.98=58,8\left(g\right)\)
c)
PTHH: 2H2 + O2 --to--> 2H2O
0,6-->0,3
=> VO2 = 0,3.24,79 = 7,437 (l)
=> Vkk = 7,437.5 = 37,185 (l)

\(a,Fe+H_2SO_4\rightarrow FeSO_4+H_2\\ b,n_{FeSO_4}=n_{H_2SO_4}=n_{H_2}=n_{Fe}=\dfrac{44,8}{56}=0,8\left(mol\right)\\ m_{FeSO_4}=152.0,8=121,6\left(g\right)\\ m_{H_2}=0,8.2=1,6\left(g\right)\\ c,SO_3+H_2O\rightarrow H_2SO_4\\ m_{ddH_2SO_4}=0,8.98:10\%=784\left(g\right)\)

\(n_{Fe}=\dfrac{2,8}{56}=0,05\left(mol\right)\\ a,PTHH:Fe+2HCl\rightarrow FeCl_2+H_2\\ n_{H_2}=n_{FeCl_2}=n_{Fe}=0,05\left(mol\right)\\ V_{H_2\left(đktc\right)}=0,05.22,4=1,12\left(l\right)\\ V_{H_2\left(đkc\right)}=0,05.24,79=1,2395\left(l\right)\\ b,n_{HCl}=0,1.3=0,3\left(mol\right)\\ Vì:\dfrac{0,05}{1}< \dfrac{0,3}{2}\Rightarrow HCldư\\ n_{HCl\left(dư\right)}=0,3-0,05.2=0,2\left(mol\right)\\ n_{FeCl_2}=n_{Fe}=0,05\left(mol\right)\\ V_{ddsau}=V_{ddHCl}=0,1\left(l\right)\\ b,C_{MddFeCl_2}=\dfrac{0,05}{0,1}=0,5\left(M\right);C_{MddHCl\left(dư\right)}=\dfrac{0,2}{0,1}=2\left(M\right)\)
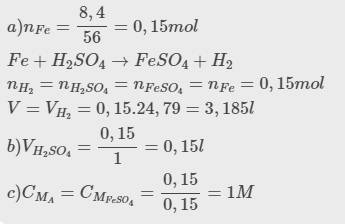
Ta có:
\(m_{HCl}=1000.10\%=100\left(g\right)\)
\(\Rightarrow m_{dd\left(HCl\right)37,23\%}=\frac{100}{37,23\%}=268,6\left(g\right)\)
\(\Rightarrow V_{HCl}=\frac{268,6}{1,19}=225,71\left(ml\right)\)