Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Ta có: \(n_{COOH\left(X\right)}=n_{CO_2}=0,7mol\)
Khi đốt X có: \(n_{CO_2}=0,4mol;n_{CO_2}=0,8mol\)
Theo ĐLBT oxi có \(n_O=2n_{COOH\left(X\right)}+2n_{O_2}=2n_{CO_2}+n_{H_2O}\)
\(\Rightarrow n_{H_2O}=y=0,6mol\)

Đáp án B
Có n H 2 O = n X
=> cả 2 axit trong X đều có 2 nguyên tử H trong phân tử.
Mà 2 axit no=>2 axit là HCOOH và HOOC-COOH.
Gọi số mol mỗi chất lần lượt là x,y(mol)
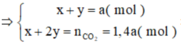
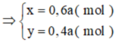
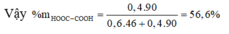

Đáp án C
Đốt cháy a mol X thu được a mol H2O ⇒ 2 Axit trong X đều chỉ có 2H trong phân từ.
⇒ 2 Axit đó là HCOOH (Y) và (COOH)2 (Z).
Giả sử a = 1 mol.
Có nY + nZ = 1
nY + 2nZ = nCO2 = 1,6
⇒ nY = 0,4 ; nZ = 0,6
⇒ %mY = 0,4 . 46 : (0,4.46 + 0,6.90) = 25,41%.

Đáp án A
n CO2 = 0,125 mol , n H2O = 0,13 mol vì n H2O> n CO2 => ancol no
Gọi công thức của axit là : R-(COOH)x ( đặt số mol là a )
An col no 2 chức là : CnH2n(OH)2 ( đặt số mol là b )
n C = n CO2 = 0,125 mol => m C = 1,5 g
n H = 2 n H2O = 0,26 mol => m H = 0,26 g
m hh E = 3,36 = m C + m H + m O => m O = 1,6 g
=> n O ( trong hỗn hợp ) = 0,1 mol
=> 2 a.x + 2b = 0,1 ( 1 )
n H2 = 0,035 mol
Bảo toàn nguyên tố H linh động => 0,035 .2 = a . x + 2 b ( 2)
Giải (1,2 ) ta có b = 0,02 và a.x = 0,03 ( vì a < b => x > 1 )
Ta có n H2O - n CO2= n ancol - n axit . ( số pi – 1 )
=> 0.005 = 0,02 – a . ( số liên kết pi -1 )
Với x = 2 thì a = 0,015 thỏa mãn axit no có 2 chức
Số C trung bình = 0,125 : ( 0,02 + 0,015 ) = 3,57
Vì là axit 2 chức và ancol 2 chức nên số C trong axit hay ancol phải tối thiểu là 2
=> Axit hoặc ancol có 2 hoặc 3 cac bon trong công thức
=> Ta thay vào tìm số C của chất còn lại ( số C phải là số nguyên )
Với số C của axit là 3 thì ta có 0,015 . 3 + 0.02 . Cancol = 0,125
=> Số C trong ancol = 4 thỏa mãn
=> Axit là CH2(COOH)2 ( 0,15 mol )
=> Ancol là C4H8(OH)2 ( 0,02 mol )
=> % m axit = 0,015 . 104 : 3,36 . 100% = 46,42 %

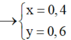
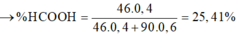

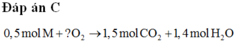


Dễ thấy cả 2 axit đều có 2 H => HCOOH và HCOO - COOH
Đặt số mol 2 chất là x và y,đặt a = 1 thì
x + y = 1
x + 2y = 1,4
=> x = 0,6 ; y = 0,4
=> %mHCOOH = 43,4%