Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

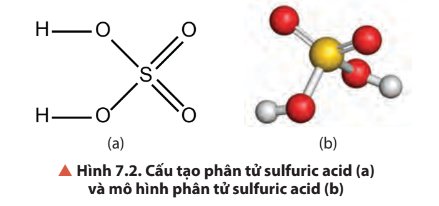
Phân tử có 2 liên kết đơn: H-O
2 liên kết đơn: S-O
2 liên kết đôi S=O

Hình 2.4: \({\rm{HCl + }}{{\rm{H}}_{\rm{2}}}{\rm{O}} \to {{\rm{H}}_{\rm{3}}}{{\rm{O}}^{\rm{ + }}}{\rm{ + C}}{{\rm{l}}^{\rm{ - }}}\)
HCl là chất cho H+, H2O nhận H+
Hình 2.5: NH3 nhận H+, H2O cho H+.

Khi đốt cháy NH4Cl thấy có khói trắng do chất này bị phân huỷ thành hai khí không màu là NH3 và HCl
\(PTHH:NH_4Cl\rightarrow\left(t^o\right)NH_3\uparrow+HCl\uparrow\)

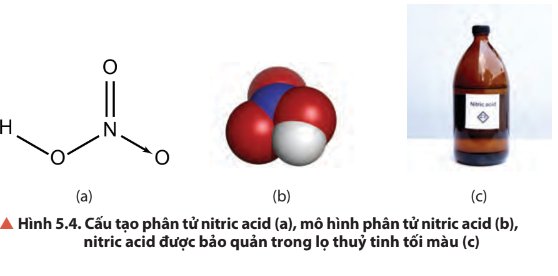
- Liên kết hoá học giữa các nguyên tử trong phân tử HNO3 là liên kết cộng hóa trị và liên kết cho nhận.
- Số oxi hóa của N trong HNO3 là +5. Đây là số oxi hóa cao nhất của N, do đó trong các phản ứng oxi hóa – khử, HNO3 là chất oxi hóa.

Trong phân tử nitrogen có liên kết ba bền vững với năng lượng liên kết lớn (945 kJ/mol).
Do đó ở nhiệt độ thường, phân tử nitrogen bền, khá trơ về mặt hóa học (khó phản ứng hóa học).

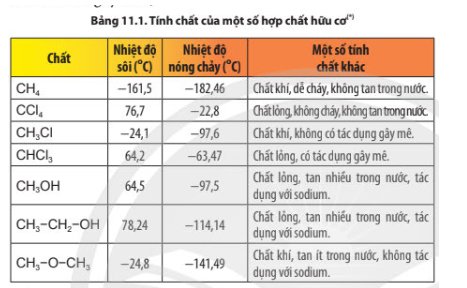
a) CH4 và CCl4 khác nhau về thành phần phân tử,cấu tạo hóa học và tính chất
b) CH3Cl và CHCl3 khác nhau về thành phần phân tử, cấu tạo hóa học và tính chất
c) CH3OH, CH3CH2OH khác nhau về thành phần phân tử, tương tự nhau cấu tạo hóa học và tính chất.
CH3OCH3 khác về thành phần phân tử, cấu tạo hóa học và tính chất so với CH3OH, CH3CH2OH

- Nước có môi trường trung tính: (H+) = (OH-) = 10-7 M \( \Rightarrow \) pH = -lg(10-7) = 7
- Trong môi trường acid: (H+)> (OH-) hay (H+) > 10-7 M
\( \Rightarrow \) -lg(H+) < 10-7
\( \Rightarrow \) pH < 7
- Trong môi trường base: (H+) < (OH- ) hay (H+) < 10-7M
\( \Rightarrow \) -lg(H+) > 10-7
\( \Rightarrow \) pH > 7

Trong hợp chất hữu cơ, có thành phần C, H, O,...Còn hợp chất vô cơ có thể có C hoặc không. Nguyên tố luôn có trong thành phần hợp chất hữu cơ là Carbon (C)

Hiện tượng: Khi đưa hai đũa nhúng HCl đặc và NH3 đặc lại gần nhau, xuất hiện khói trắng.
Phương pháp nhận biết ammonia: sử dụng HCl đặc. Hiện tượng: xuất hiện khói trắng là muối ammonium chloride (NH4Cl).
Phương trình hóa học: NH3 + HCl → NH4Cl
Ta đặt hai bình hở chứa dung dịch HCl đặc và dung dịch NH3 gần nhau thì thấy xuất hiện “khói” trắng.
Vì HCl và NH3 là những hợp chất dễ bay hơi, chúng kết hợp với nhau tạo thành tinh thể muối Ammonium chloride, gây ra hiện tượng “khói”.
=> Phương pháp nhận biết ammonia: Nhúng hai đầu đũa thuỷ tinh quấn bông vào dung dịch HCl đặc (thuốc thử) và NH3 đặc, sau đó đưa lại gần nhau.

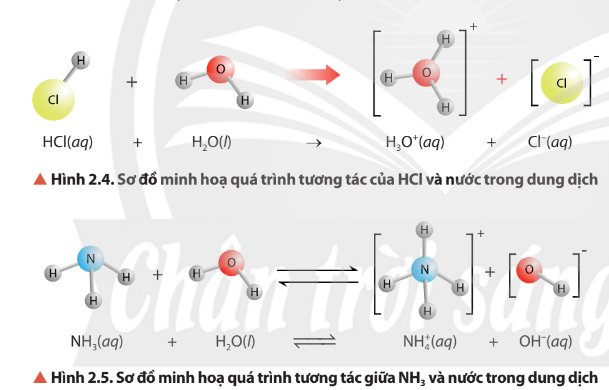






- Trong hình 2.4, H2O nhận H+ nên H2O là base.
- Trong hình 2.5, H2O nhường H+ nên H2O là acid.
- Trong cân bằng ion \(HCO_3^-\)
+ H2O nhận H+ nên H2O là base.
+ H2O nhường H+ nên H2O là acid.