Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.





BTKL
mX + mdd HNO3 = mdd X + mH2O + m↑
=> mdd X = 11,6 + 87,5 – 30 . 0,1 – 46 . 0,15 = 89,2g
=> C%Fe(NO3)3 = 13,565%

M + 2HCl → MCl2 + H2↑
MO + 2HCl → MCl2 + H2O
MCl2 + 2NaOH → M(OH)2↓ + 2NaCl
M(OH)2 → MO + H2O
M + CuCl2 → MCl2 + Cu↓

Pt:
Fe3O4 + 4H2SO4 → FeSO4 + Fe2(SO4)3 + 4H2O
0,1 → 0,4 0,1 0,1
Cu + Fe2(SO4)3 → CuSO4 + 2FeSO4
0,1 ←0,1 → 0,1 0,2
Rắn B là 0,1 mol Cu → x = 6,4 (g)
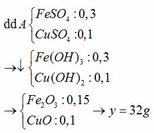

2.
Khí thoát ra là khí \(H_2:n_{H2}=0,2\left(mol\right)\)
\(\rightarrow n_M=0,2\left(mol\right)\)
CuSO4 chỉ tác dụng với M \(\rightarrow n_{CuSO4_{pu}}=0,2\left(mol\right)\)
Trong 62g chất rắn có CuSO4 dư và MSO4
\(\rightarrow m_{MSO4}=62-0,2.160=30\left(g\right)\)
\(m_{MSO4}=14,8+96.0,1-m_{MO}=30g\rightarrow m_{MO}=4g\)
Bảo toàn khối lượng : mhh =mM + mMO + mMSO4
\(14,8=0,2M+4+\left\{30-\left[0,2.\left(M+96\right)\right]\right\}\)
\(\rightarrow M=24\left(Mg\right)\)\(\rightarrow\%m_M=32,43\%,\%m_{MO}=27,03\%,\%m_{SO4}=40,54\%\)
1.
\(nH_2\) để khử oxit \(=0,09\left(mol\right)\)
\(A_2O_x+xH_2\rightarrow2A+xH_2O\left(1\right)\)
\(CuO+H_2\rightarrow Cu+H_2O\left(2\right)\)
Do Cu không tác dụng với hcl nên chỉ có kim loại a sinh ra pư với HCl sinh ra khí H2
\(nH_{2_{sinh.ra}}=0,06\left(mol\right)\)
Gọi hóa trị củaA là x
\(2A+2xHCl\rightarrow2AClx+xH_2\left(3\right)\)
0,12/x__________________0,06
Giả sử hoá trị của A không đổi trong oxit và trong muối ( trừ trường hợp của \(Fe_2O_3\)) nên \(NH_2\left(1\right)=NH_2\left(3\right)\)
\(n_{CuO}=n_{H2}=0,09-0,02=0,03\)
\(n_A=0,03.6=1,2\rightarrow n_{A2Ox}=0,06\)
\(2A+16x=\frac{5,44-0,03.80}{0,06}=50,666\left(loai\right)\)
Vậy giả sử oxit là \(Fe_2O_3\)