Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
Bảo toàn điện tích: 2x = 0,05 + 0,12 – 0,12 ⇒ x = 0,025
Ba2+ + SO42- → BaSO4
0,025 ← 0,025 → 0,025 (mol)
NH4+ + OH- → NH3 + H2O
0,05 → 0,05 → 0,05 0,05 ( mol)
mchất rắn = mX + mBa(OH)2 – mBaSO4 – mNH3 – mH2O = 7,875g

Theo BTĐT: x = ( 0,12 + 0 ,05 - 0,12):2 = 0,025 (mol)
Cho 0 ,03 Ba(OH)2 vào dd X
Ba2+ + SO42- --->BaSO4
NH4+ OH- ---> NH3 +H2O
=> m = 7,875g

Đáp án C
Trong 100ml dd X có 0,1 mol Ba2+, 0,15 mol .
Trong 200ml dung dịch X có 0,2 mol Cl-.
Do đó trong 50 ml dung dịch X có 0,05 mol Ba2+, 0,075 mol , 0,05 mol Cl- và x mol K+
Theo định luật bảo toàn điện tích được x = 0,025
Khi cô cạn xảy ra quá trình:


Đáp án A
Bảo toàn điện tích suy ra x = 0,025 mol
Ba2++ SO42-→BaSO4
0,03 0,025 0,025
OH-+ NH+4→ NH3+ H2O
0,06 0,05
Dung dịch Y có 0,12 mol Na+; 0,12 mol Cl-; 0,005 mol Ba2+; OH- 0,01 mol
Khi cô cạn thu được m = 0,12.23+ 0,12.35,5+ 0,005.137+ 0,01.17 = 7,875 gam




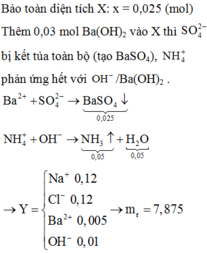
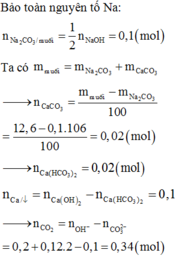
nOH- = 0,2.0,75 + 0,2.1,5.2 = 0,75 mol
nCO2 = 0,6
=> \(\frac{nOH}{nCO2}=\frac{0,75}{0,6}=1,25>1=>\) 2 muối
2OH- + CO2 => CO32- + H2O
2a------>a-------->a
OH- + CO2 => HCO3-
b---------->b---------->b
ta có 2a + b = 0,75
a + b = 0,6
=> a=0,15 ; b= 0,45
nBa2+ = 0,2.1,5 = 0,3 mol > nCO32- => n tủa = nCO3 = 0,15
=> m tủa = 0,15.197 = 29,55 mol =x
nNa+ = 0,2.0,75 = 0,15 mol
=> nBa dư = 0,3 - 0,15 = 0,15
=> m = 0,15.23 + 0,15.137 + 0,45.61 = 51,45(g)