K
Khách
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.
Các câu hỏi dưới đây có thể giống với câu hỏi trên

29 tháng 11 2019
Đáp án A
Ta có: mFe = 40%.m = 0,4m (g) → mCu = m - 0,4m = 0,6m (g)
Sau phản ứng còn 0,65m (g) kim loại > mCu = 0,6m (g)
Khối lượng Fe còn dư: 0,65m - 0,6m = 0,05m (g)
Vậy: mFe phản ứng = 0,4m - 0,05m = 0,35m (g)
Do Fe còn dư sau phản ứng nên tạo thành muối Fe2+
Quá trình nhường electron:
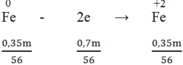
Quá trình nhận electron:
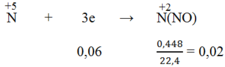
Áp dụng định luật bảo toàn electron, ta có:
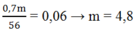
Ta có:
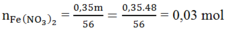
![]()

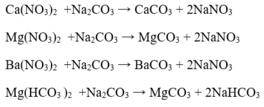

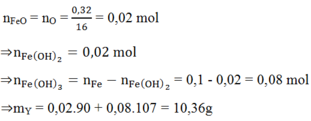
a,CuO=> Cu hóa trị II.
E=A/n Trong đó :E là đương lượng gam của nguyên tố(g); A là khối lượng mol nguyên tử của ngưyên tố; n là hoá trị của nguyên tố. do đó đương lượng Cu= 64/2=32 b, Đương lượng của hợp chất ĐL = E = M/n Trong đó : E là đương lượng gam của chất cần xác định (g); M là khối lượng mol phan tử của chất cần xác định (g); n là số điện tích trao đổi. đương lượng MgSO4 = (24+32+16*4)/(2+2)=30 c, vì đồng chiếm 79,9 % , oxi chiếm 20,1 %=> CTPT: CuO ... quay lại câu a