Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

3Fe+2O2->Fe3O4
Fe3O4+8HCl->2FeCl3+FeCl2+4H2O
nHCl=0.6(mol)
->nFe3O4=0.075(mol)->m3=17.4(g)
nFe=0.225(mol)->m1=12.6(g)
nO2=0.15(mol)
m2=4.8(g)

nCu=0,3mol
pthh: 2Cu+O2=> 2CuO
0,3->0,15->0,3
=> m1=0,3.80=24g
=> v=0,15.22,4=3,36l
CuO+2HCl=>CuCl2+H2O
0,3->0,6
=> m2=0,6.36,5=21,9g
nCuO = 19,2 : 64 = 0,3 mol
PTHH: 2Cu + O2 ===> 2CuO
0,3 0,15 0,3 (mol)
CuO + 2HCl ===> CuCl2 + H2O
0,3 0,6 (mol)
Lập tỉ lệ các số mol theo pt, ta có:
V = 0,15 x 22,4 = 3,36 lít
m1 = 0,3 x 80 = 24 gam
m2 = 0,6 x 36,5 = 21,9 gam

Bài 1 :
Độ tan của KNO3 ởi 20 độ C là :
\(S_{KNO_3\left(20^OC\right)}=\dfrac{60.100}{190}=\dfrac{6000}{190}\approx31,579\left(g\right)\)

Bài 9 :
\(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
Đặt x, y lần lượt số mol Mg , Zn phản ứng với axit
PTHH :
\(Mg\left(x\right)+H_2SO_4\left(x\right)-->MgSO_4\left(x\right)+H_2\left(x\right)\)
\(Zn\left(y\right)+H_2SO_4\left(y\right)-->ZnSO_4\left(y\right)+H_2\left(y\right)\)
Gỉa sử trong hỗn hợp chỉ có Zn :
\(x+y=n_{Zn}=n_{H_2}=0,1\)
\(\Rightarrow m_{Zn}=0,1.65=6,5\left(g\right)\)
\(\Rightarrow65x+65y=65\left(x+y\right)=6,5\left(g\right)< 7,8\left(g\right)\)
Vậy chứng tỏ axit vẫn dư sau phản ứng .
Bài 7 :
PTHH :
\(Fe+2HCl-->FeCl_2+H_2\left(1\right)\)
\(2Al+6HCl-->2AlCl_3+3H_2\left(2\right)\)
Gỉa sử trong hỗn hợp X chỉ có Fe :
\(n_{Fe}=\dfrac{22}{56}=0,4\left(mol\right)\Rightarrow n_{HCl}=0,4.2=0,8\left(mol\right)\)
\(n_{HCl}=0,6\left(mol\right)< 0,8\left(mol\right)\)
Chứng tỏ kim loại không tan hết .(1)
\(Gỉa\) sử trong hỗn hợp chỉ có Al :
\(n_{Al}=\dfrac{22}{27}=0,814=>n_{HCl}=3.0,814=2,44\left(mol\right)>0,6\left(mol\right)\)
Chứng tỏ kim loại không tan hết (2)
Từ (1),(2) chứng tỏ hh X không tan hết .
HÌNH NHƯ SAI ĐỀ .

6)Gọi 2x,y là số mol Al,Fe
Theo gt:\(m_{hhKL}\)=\(m_{Al}+m_{Fe}\)=27.2x+56y=54x+56y=11(g)(1)
Ta có PTHH:
2Al+6HCl->\(2AlCl_3\)+3\(H_2\)(1)
2x......6x........................3x.....(mol)
Fe+2HCl->\(FeCl_2\)+\(H_2\)(2)
y........2y.....................y....(mol)
Theo PTHH(1);(2):\(n_{H_2\left(1;2\right)}\)=3x+y=8,96:22,4=0,4(mol)(2)
Từ (1);(2)=>\(\left\{{}\begin{matrix}x=0,1\left(mol\right)\\y=0,1\left(mol\right)\end{matrix}\right.\)=>\(\left\{{}\begin{matrix}m_{Al}=54x=54.0,1=5,4\left(g\right)\\n_{Fe}=56y=0,1.56=5,6\left(g\right)\end{matrix}\right.\)
Vậy % về khối lượng là:
%\(m_{Al}\)=\(\dfrac{5,4}{11}.100\%\)=49,1%
%\(m_{Fe}\)=\(\dfrac{5,6}{11}.100\%\)=50,9%
b)Theo PTHH(1);(2):\(n_{HCl\left(1;2\right)}\)=6x+2y=0,6+0,2=0,8(mol)
mặt khác:\(C_{M\left(ddHCl\right)}\)=2M=>\(V_{ddHCl}\)=0,8:2=0,4l

a, \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(n_{H_2}=\dfrac{0,896}{22,4}=0,04\left(mol\right)\)
Theo PT: \(n_{Zn}=n_{H_2}=0,04\left(mol\right)\Rightarrow m_1=m_{Zn}=0,04.65=2,6\left(g\right)\)
\(n_{HCl}=2n_{H_2}=0,08\left(mol\right)\Rightarrow m_{HCl}=0,08.36,5=2,92\left(g\right)\)
\(\Rightarrow m_2=m_{ddHCl}=\dfrac{2,92}{14,6\%}=20\left(g\right)\)
b, Ta có: m dd sau pư = mZn + m dd HCl - mH2 = 22,52 (g)
\(n_{ZnCl_2}=n_{H_2}=0,04\left(mol\right)\)
\(\Rightarrow C\%_{ZnCl_2}=\dfrac{0,04.136}{22,52}.100\%\approx24,16\%\)


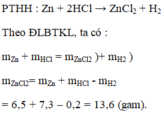
Số mol ZnO thu được là: nZnO =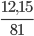 =0,15 mol
=0,15 mol
PTHH: 2Zn + O2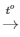 2ZnO
2ZnO
Tỉ lệ PT: 2mol 1mol 2mol
Phản ứng: 0,15mol ← 0,15mol
=> Khối lượng Zn phản ứng là: m1 = mZn = 0,15.65 = 9,75 gam
Lấy 0,15 mol ZnO cho vào dung dịch HCl
PTHH: ZnO + 2HCl → ZnCl2 + H2O
Tỉ lệ PT: 1mol 2mol
P/ứng: 0,15mol → 0,3mol
=> Khối lượng HCl phản ứng là: mHCl = m2 = 0,3.36,5 = 10,95 gam
=> m1 + m2 = 9,75 + 10,95 = 20,7 gam
Đáp án cần chọn là: A