..
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a, Lã kẽm có một lớp Sắt màu xám bao phủ bên ngoài.
PTHH:
\(Zn+FeCl_2\rightarrow ZnCl_2+Fe\)
0,03 0,03 0,03 0,03
Gọi nZn = nFe = a(mol)
0,27g = 65a - 56a
=> a = 0,03(mol)
b, \(m_{Zn\left(pư\right)}=0,03.65=1,95\left(g\right)\)
\(m_{Fe\left(sra\right)}=0,03.56=1,68\left(g\right)\)
c, \(m_{FeCl_2}=0,03.127=3,81\left(g\right)\)
\(m_{dd}=1,95+200=201,95\left(g\right)\)
\(C\%FeCl_2=\dfrac{3,81}{201,95}.100\%=1,89\left(\%\right)\)

a.
C% = \(\dfrac{m_{ct}}{m_{dd}}\) ⇒ \(m_{ct}\) = 250 . \(\dfrac{7,3}{100}\) = 18,25 gam
⇒\(n_{HCl}\) = 0,5 mol
PTHH: Mg + 2HCl →MgCl2 + H2
⇒\(n_{Mg}\) = 0,25 mol
⇒\(m_{Mg}\)= 12 gam
b. C% = \(\dfrac{m_{ct}}{m_{dd}}\) = \(\dfrac{m_{Mg}}{m_{Mg}+m_{HCl}}\) = 4,58%
a) Khối lượng HCl tham gia PƯ là:
mct= mdd.\(\dfrac{C\%}{100\%}\)= 250. \(\dfrac{7,3\%}{100\%}\)= 18,25 (g)
Số mol HCl tham gia PƯ là:
n=m:M= 18,25 : 36,5 = 0,5 (mol)
PTHH: Mg + 2HCl -> MgCl2 + H2
số mol Mg tham gia PƯ là
0,5 . 1 : 2 = 0,25 (mol)
Khối lượng Mg tham gia PƯ là
m= n.M = 0,25 . 24 = 6 (g)
b) Số mol MgCl2 là:
0,5 . 1 : 2 = 0,25 (mol)
Khối lượng MgCl2 thu được là
m = n.M = 0,25 . 95 = 23,75 (g)
C% MgCl2 trong dd là
23,75 : (250 + 6) . 100% \(\approx\) 9,3%

số mol Cu điều chế được là:
n = m:M = 9,6 : 64 = 0,15 (mol)
PTHH: CuCl2 + Fe -> FeCl2 + Cu
Khối lượng Fe cần dùng là:
m=n.M= 0,15 . 56 = 8,4 (g)
Khối lượng CuCl2 cần dùng là:
m=n.M= 0,15 . 135 = 20,25 (g)
nồng độ % CuCl2 trong dd là:
20,25 : 200 . 100% = 10,125 (%)

Ta có: \(n_{Cu}=\dfrac{8,32}{64}=0,13\left(mol\right)\)
\(n_{O_2}=\dfrac{6,81725}{24,79}=0,275\left(mol\right)\)
PT: \(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
\(2Cu+O_2\underrightarrow{t^o}2CuO\)
Theo PT: \(n_{O_2}=\dfrac{2}{3}n_{Fe}+\dfrac{1}{2}n_{Cu}\) \(\Rightarrow n_{Fe}=0,315\left(mol\right)\)
\(\Rightarrow a=0,315.56=17,64\left(g\right)\)
Theo PT: \(\left\{{}\begin{matrix}n_{Fe_3O_4}=\dfrac{1}{3}n_{Fe}=0,105\left(mol\right)\\n_{CuO}=n_{Cu}=0,13\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%n_{Fe_3O_4}=\dfrac{0,105}{0,105+0,13}.100\%\approx44,7\%\\\%n_{CuO}\approx55,3\%\end{matrix}\right.\)
\(\overline{M_{hh}}=\dfrac{m_{Fe_3O_4}+n_{CuO}}{n_{Fe_3O_4}+n_{CuO}}=\dfrac{0,105.232+0,13.80}{0,105+0,13}=147,91\left(g/mol\right)\)

Gọi x, y là số mol của Mg và Cu.
Theo đề có: \(\dfrac{24x}{64y}=\dfrac{3}{4}\Leftrightarrow x-2y=0\left(1\right)\)
Lại có: \(24x+64y=11\left(2\right)\)
Từ (1), (2) giải hệ phương trình ta được: \(\left\{{}\begin{matrix}x=\dfrac{11}{56}\\y=\dfrac{11}{112}\end{matrix}\right.\)
BTNT:
\(n_{MgO}=n_{Mg}=\dfrac{11}{56},n_{CuO}=n_{Cu}=\dfrac{11}{112}\)
\(\Rightarrow m_{sp}=m_{MgO}+m_{CuO}=\dfrac{11}{56}.40+\dfrac{11}{112}.80=15,7\left(g\right)\)
\(n_{O_2}=\dfrac{1}{2}\left(x+y\right)=\dfrac{1}{2}\left(\dfrac{11}{56}+\dfrac{11}{112}\right)=0,15\left(mol\right)\Rightarrow V_{O_2}=0,15.22,4=3,36\left(l\right)\)

Ta có: \(n_{Al}=\dfrac{5,4}{27}=0,2\left(mol\right)\)
\(n_{O_2}=\dfrac{4,958}{24,79}=0,2\left(mol\right)\)
PT: \(2Cu+O_2\underrightarrow{t^o}2CuO\)
\(4Al+3O_2\underrightarrow{t^o}2Al_2O_3\)
Theo PT: \(n_{O_2}=\dfrac{1}{2}n_{Cu}+\dfrac{3}{4}n_{Al}\)
⇒ nCu = 0,1 (mol)
⇒ m = 0,1.64 = 6,4 (g)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Cu}=\dfrac{6,4}{6,4+5,4}.100\%\approx54,2\%\\\%m_{Al}\approx45,8\%\end{matrix}\right.\)

a, Ta có: 23nNa + 39nK = 2,94 (1)
PT: \(2Na+2H_2O\rightarrow2NaOH+H_2\)
\(2K+2H_2O\rightarrow2KOH+H_2\)
Theo PT: \(n_{H_2}=\dfrac{1}{2}n_{Na}+\dfrac{1}{2}n_K=\dfrac{1,12}{22,4}=0,05\left(mol\right)\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{Na}=0,06\left(mol\right)\\n_K=0,04\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Na}=\dfrac{0,06.23}{2,94}.100\%\approx46,9\%\\\%m_K\approx53,1\%\end{matrix}\right.\)
b, Theo PT: \(\left\{{}\begin{matrix}n_{NaOH}=n_{Na}=0,06\left(mol\right)\\n_{KOH}=n_K=0,04\left(mol\right)\end{matrix}\right.\)
Ta có: m dd sau pư = 2,94 + 97,16 - 0,05.2 = 100 (g)
\(\Rightarrow\left\{{}\begin{matrix}C\%_{NaOH}=\dfrac{0,06.40}{100}.100\%=2,4\%\\C\%_{KOH}=\dfrac{0,04.56}{100}.100\%=2,24\%\end{matrix}\right.\)

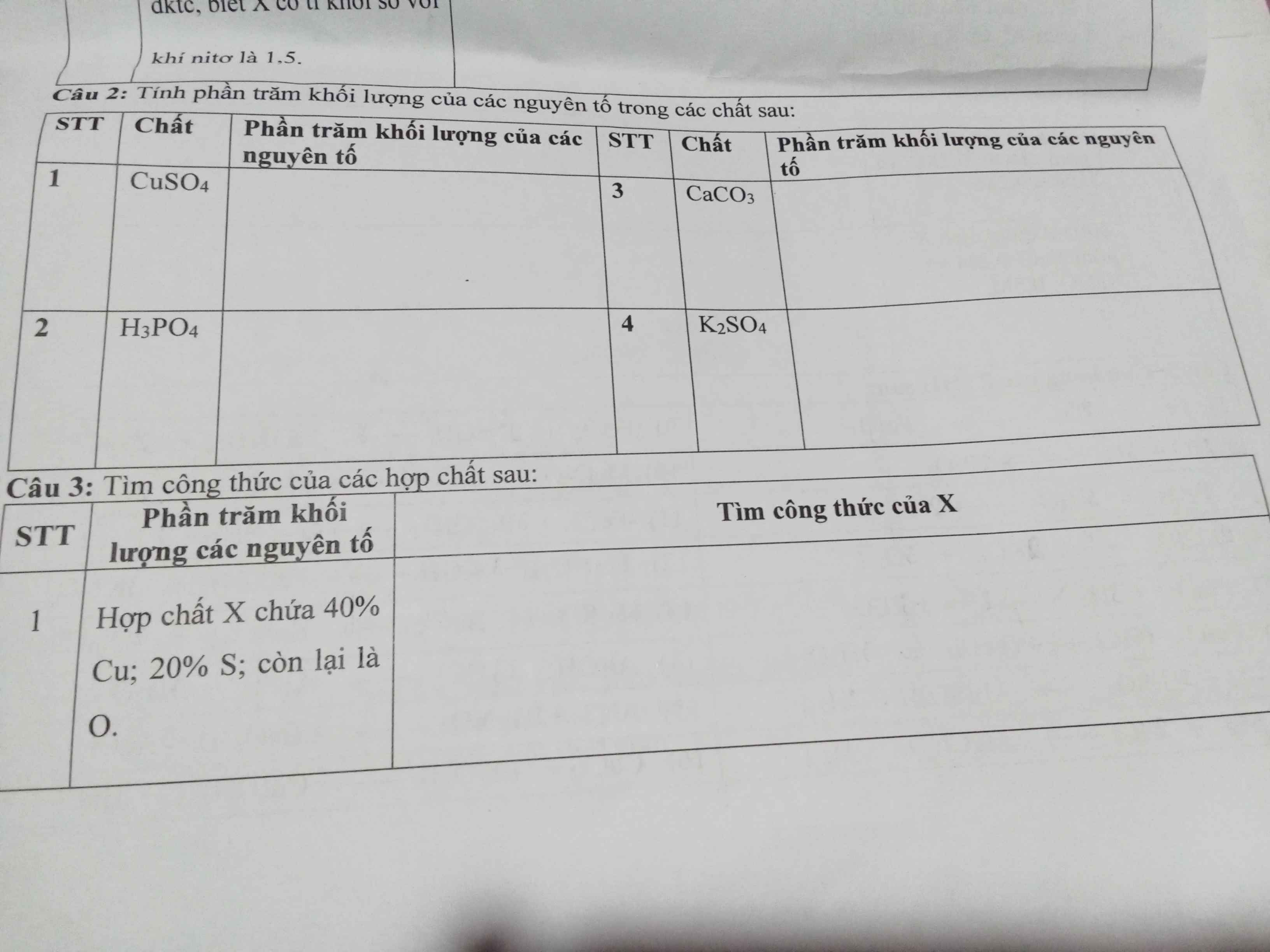
1)
\(\%_{Cu}=\dfrac{64.100\%}{64+96}=40\%,\%_S=\dfrac{32.100\%}{64+96}=20\%,\%_O=100\%-40\%-20\%=40\%\)
2)
\(\%_H=\dfrac{3.100\%}{3+31+16.4}=3,06\%,\%_P=\dfrac{31.100\%}{3+31+16.4}=31,63\%\\ \%_O=100\%-3,06\%-31,63\%=65,31\%\)
3)
\(\%_{Ca}=\dfrac{40.100\%}{100}=40\%,\%_C=\dfrac{12.100\%}{100}=12\%,\%_O=\dfrac{16.100\%}{100}=16\%\text{_}\)
4)
\(\%_K=\dfrac{39.100\%}{39.2+32+16.4}=22,41\%,\%_S=\dfrac{32.100\%}{39.2+32+16.4}=18,39\%\\ \%_O=100\%-22,41\%-18,39\%=59,2\%\)
Câu 3:
Gọi Công thức hóa học của X là: \(Cu_xS_yO_z\)
Ta có:;
\(x:y:z=\dfrac{40}{64}:\dfrac{20}{32}:\dfrac{40}{16}=0,625:0,625:2,5=1:1:4\)
=> CTHC: \(CuSO_4\)