giups mik bài 1 với 3đc ko ạ
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


- leetrunghieu
- 01/01/2022
Đáp án:
Ta lấy các chất đổ lần lượt vào nhau thu được kết quả như bảng trên
Dd nào chỉ tạo 1 kết tủa với các chất còn lại là K2SO4
Dd nào tạo kết tủa keo trắng, xong đó kết tủa tan dần rồi lại xuất hiện, lại tan hết => đó là Al(NO3)3
Dd nào tạo 1 kết tủa và 1 khí bay lên ( mùi khai) với các chất còn lại là (NH4)2SO4
Dd tạo 2 kết tủa với các chất còn lại là Ba(NO3)2
Dd tạo 1 kết tủa keo trắng, sau đó kết tủa tan và 1 chất khí với các chất khác là NaOH
Các PTHH xảy ra:
K2SO4 + Ba(NO3)2→ BaSO4↓ + 2KNO3
Al(NO3)3 + NaOH → Al(OH)3↓ + 3NaNO3
Al(OH)3↓ + NaOH → NaAlO2 + 2H2O
(NH4)2SO4 + Ba(NO3)2 → BaSO4↓ + 2NH4NO3
2NaOH + (NH4)2SO4 → Na2SO4 + 2NH3 + 2H2O
Từ bảng trên => nhận biết được cả 5 chất

m=mNaCl+mKCl
Giải thích các bước giải:
Ta có: Gọi số mol M2CO3;MHCO3 và MCl lần lượt là x; y; z, ta có:
M2CO3+2HCl→2MCl+H2O+CO2
MHCO3+HCl→MCl+H2O+CO2
(2M+60)x+(M+61)y+(M+35,5)z=43,71
Phần 2: nAgCl=0,48(mol)
MCl+AgNO3→MNO3+AgCl
AgNO3+HCl→AgCl+HNO3
Phần 1:
KOH+HCl→KCl+H2O
nKOH=0,1(mol)⇒ưnHCldư=0,1(mol)
⇒nMCl=0,38(mol)⇒2x+y+z=0,76(1)
Do nCO2=0,4(mol)⇒x+y=0,4(2)
⇒x+z=0,36
Ta có:(2M+60)x+(M+61)y+(M+35,5)z=43,71
⇒(2M+60)x+(M+61)(0,4−x)+(M+35,5)(0,36−x)=43,71
⇒0,76M−36,5x=6,53⇒x=0,76M−6,5336,5
Ta có: Vì x+y=0,4⇒0<x<0,4⇒0<0,76M−6,5336,5<0,36
⇒0<0,76M−6,53<14,6⇒6,53<0,76M<21,13
⇒8,6<M<27,8⇒M là Na
⇒106x+84y+58,5z=43,71(3)
Từ (1);(2);(3)⇒x=0,3;y=0,1;z=0,06
⇒∑nHCl=0,3.2+0,1+0,1.2=0,9(mol)⇒mHCl=32,85(g)⇒mddHCl=312,26(g)
⇒V=297,39(ml)
Ta có: m=mNaCl+mKCl

\(n_{BaCO_3}=\dfrac{7,88}{197}=0,04\left(mol\right)\)
\(n_{Ba\left(OH\right)_2}=0,3.0,2=0,06\left(mol\right)\)
\(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
PTHH: FeCO3 + H2SO4 --> FeSO4 + CO2 + H2O
2Al + 3H2SO4 --> Al2(SO4)3 + 3H2
=> \(n_{Al}=\dfrac{2}{3}.n_{H_2}=0,1\left(mol\right)\)
TH1: Kết tủa không bị hòa tan
PTHH: Ba(OH)2 + CO2 --> BaCO3 + H2O
0,04<---0,04
\(\Rightarrow n_{CO_2}=0,04\left(mol\right)\)
\(\Rightarrow n_{FeCO_3}=0,04\left(mol\right)\)
m = 0,04.116 + 0,1.27 = 7,34 (g)
TH2: Kết tủa bị hòa tan 1 phần
PTHH: Ba(OH)2 + CO2 --> BaCO3 + H2O
0,06----->0,06--->0,06
BaCO3 + CO2 + H2O --> Ba(HCO3)2
0,02---->0,02
=> \(n_{CO_2}=0,06+0,02=0,08\left(mol\right)\)
\(\Rightarrow n_{FeCO_3}=0,08\left(mol\right)\)
m = 0,08.116 + 0,1.27 = 11,98 (g)

\(n_{CO_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\\ n_{NaOH}=0,5.0,1=0,05\left(mol\right)\\ n_{Na_2CO_3}=1,5.0,1=0,15\left(mol\right)\)
Xét \(T=\dfrac{0,05}{1}=\dfrac{1}{2}\) => Tạo muối NaHCO3
PTHH: \(NaOH+CO_2\rightarrow NaHCO_3\)
0,05---->0,05----->0,05
\(Na_2CO_3+CO_2+H_2O\rightarrow2NaHCO_3\)
bđ 0,15 0,05
sau pư 0,1 0 0,1
Vậy ddX gồm \(\left\{{}\begin{matrix}Na_2CO_3:n_{Na_2CO_3}=0,1\left(mol\right)\\NaHCO_3:n_{NaHCO_3}=0,05+0,1=0,15\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}n_{CO_3^{2-}}=0,1\left(mol\right)\\n_{HCO_3^-}=0,15\left(mol\right)\end{matrix}\right.\)
\(n_{BaCO_3\downarrow}=\dfrac{43,34}{197}=0,22\left(mol\right)\)
Xét \(0,22< 0,1+0,15=0,25\)
=> Trong dd có chứa muối \(HCO_3^-\)
+) TH1: Muối đó là NaHCO3 dư
\(n_{Ba^{2+}}=n_{BaCO_3}=0,22\left(mol\right)\\ n_{BaCl_2}=2.0,1=0,2\left(mol\right)\\ \xrightarrow[]{\text{BTNT Ba}}n_{Ba\left(OH\right)_2}=0,22-0,2=0,02\left(mol\right)\\ \rightarrow a=C_{M\left(Ba\left(OH\right)_2\right)}=\dfrac{0,02}{0,1}=0,2M\)
+) TH2: Muối đó là Ba(HCO3)2
\(\xrightarrow[\text{BTNT C}]{}n_{Ba\left(HCO_3\right)_2}=\dfrac{1}{2}n_{HCO_3^-}=\dfrac{1}{2}.\left(0,25-0,22\right)=0,015\left(mol\right)\\ \sum n_{Ba^{2+}}=n_{Ba\left(HCO_3\right)_2}+n_{BaCO_3}=0,015+0,22=0,235\left(mol\right)\\ \xrightarrow[\text{BTNT Ba}]{}n_{Ba\left(OH\right)_2}=0,235-0,2=0,035\left(mol\right)\\ \rightarrow a=C_{M\left(Ba\left(OH\right)_2\right)}=\dfrac{0,03}{0,1}=0,35M\)
Vậy \(0,2\le a\le0,35\)

Gọi số mol C2H5OH, C6H6 là a, b (mol)
=> 46a + 78b = 5,79 (1)
\(n_{NaOH}=0,75.0,8=0,6\left(mol\right)\)
\(n_{CaCO_3}=\dfrac{27}{100}=0,27\left(mol\right)\)
TH1: Y chỉ chứa muối là Na2CO3
PTHH: 2NaOH + CO2 --> Na2CO3 + H2O
0,27<----0,27
Na2CO3 + CaCl2 --> CaCO3 + 2NaCl
0,27<----------------0,27
=> \(n_{CO_2}=0,27\left(mol\right)\)
PTHH: C2H5OH + 3O2 --to--> 2CO2 + 3H2O
a------------------->2a
C6H6 + \(\dfrac{15}{2}\)O2 --to--> 6CO2 + 3H2O
b-------------------->6b
=> 2a + 6b = 0,27 (2)
(1)(2) => a = 0,114 (mol); b = 0,007 (mol)
TH2: Y chứa muối là Na2CO3 và NaHCO3
PTHH: 2NaOH + CO2 --> Na2CO3 + H2O
0,6---->0,3------->0,3
Na2CO3 + CO2 + H2O --> 2NaHCO3
0,03--->0,03
Na2CO3 + CaCl2 --> CaCO3 + 2NaCl
0,27<----------------0,27
=> \(n_{CO_2}=0,3+0,03=0,33\left(mol\right)\)
Có: 2a + 6b = 0,33 (3)
(1)(3) => a = 0,075 (mol); b = 0,03 (mol)

a)
\(n_{Ca}=\dfrac{8}{40}=0,2\left(mol\right)\)
PTHH: Ca + 2H2O --> Ca(OH)2 + H2
0,2--------------->0,2----->0,2
=> \(m_{Ca\left(OH\right)_2}=0,2.74=14,8\left(g\right)\)
\(m_{dd}=8+492,4-0,2.2=500\left(g\right)\)
\(C\%=\dfrac{14,8}{500}.100\%=2,96\%\)
b)
\(\dfrac{1}{10}\) dd A chứa 0,02 mol Ca(OH)2
Gọi công thức chung của 2 khí là XO2
\(M_{XO_2}=27.2=54\left(g/mol\right)\Rightarrow M_X=22\left(g/mol\right)\)
\(n_{CaXO_3}=\dfrac{1,1}{40+22+16.3}=0,01\left(mol\right)\)
TH1: Nếu kết tủa không bị hòa tan
PTHH: Ca(OH)2 + XO2 --> CaXO3 + H2O
0,01<---0,01
=> V = 0,01.22,4 = 0,224 (l)
TH2: Nếu kết tủa bị hòa tan 1 phần
PTHH: Ca(OH)2 + XO2 --> CaXO3 + H2O
0,02---->0,02---->0,02
CaXO3 + XO2 + H2O --> Ca(HXO3)2
0,01--->0,01
=> V = (0,02 + 0,01).22,4 = 0,672 (l)
a)
\(n_{Ca}=\dfrac{8}{40}=0,2\left(mol\right)\)
PTHH: \(Ca+2H_2O\rightarrow Ca\left(OH\right)_2+H_2\uparrow\)
0,2--------------->0,2----------->0,2
ddA có chứa chất tan: Ca(OH)2
\(m_{ddA}=8+492,4-0,2.2=500\left(g\right)\\ m_{Ca\left(OH\right)_2}=0,2.74=14,8\left(g\right)\\ \rightarrow C\%_{Ca\left(OH\right)_2}=\dfrac{14,8}{500}.100\%=2,96\%\)
b)
1/10 ddA có chứa: \(n_{Ca\left(OH\right)_2}=\dfrac{0,2}{10}=0,02\left(mol\right)\)
Quy hết hỗn hợp CO2, SO2 về RO2
\(M_{RO_2}=27.2=54\left(g\text{/}mol\right)\\ \Leftrightarrow M_R+16.2=54\\ \Leftrightarrow M_R=22\left(g\text{/}mol\right)\)
+) TH1:Nếu kết tủa không bị tan
\(n_{CaRO_3}=\dfrac{1,1}{110}=0,01\left(mol\right)\)
PTHH: \(RO_2+Ca\left(OH\right)_2\rightarrow CaRO_3\downarrow+H_2O\)
0,01<----0,01<--------0,01
Xét \(n_{Ca\left(OH\right)_2\left(pư\right)}=0,01< 0,02=n_{Ca\left(OH\right)_2\left(bđ\right)}\)
=> TH này có thoả mãn
\(V=V_{RO_2}=0,01.22,4=0,224\left(l\right)\)
+) TH2:Nếu kết tủa bị tan
Tương tự TH1: nRO2 (tạo muối trung hoà) = 0,01 (mol)
\(n_{Ca\left(OH\right)_2\left(tạo.muối.axit\right)}=0,02-0,01=0,01\left(mol\right)\)
PTHH: \(Ca\left(OH\right)_2+2RO_2\rightarrow Ca\left(HRO_3\right)_2\)
0,01---------->0,02
\(\rightarrow\sum n_{RO_2}=0,01+0,02=0,03\left(mol\right)\\ \rightarrow V_{RO_2}=0,03.22,4=0,672\left(l\right)\)
Vậy \(0,224\le V\le0,672\)

Do ancol đa chức nên \(x\ge2\), mà \(n\ge x\) => \(n\ge2\)
(Do nếu n < x thì số C < số OH, dẫn đến việc nhiều nhóm OH gắn vào 1 nguyên tử C --> vô lí)

Do tổng số hạt trong hạt nhân là 17
=> p + n = 17 (1)
Do số hạt không mang điện nhiều hơn số hạt mang điện là 1
=> n - p = 1 (2)
(1)(2) => p = 8 (hạt); n = 9(hạt)
e = p = 8 (hạt)
Nguyên tố đó là O
\(m_O=\dfrac{16}{12}.1,9926.10^{-23}=2,6568.10^{-23}\left(g\right)\)
Xét \(\dfrac{NTK_O}{NTK_S}=\dfrac{16}{32}=\dfrac{1}{2}\)
=> Nguyên tử O nhẹ hơn nguyên tử S 2 lần
NTK là số khối lượng A particle, trong sách giáo khoa Việt có 2 từ là nguyên tử và phân tử, do khó phân biệt nên chọn từ particle.
trong dãy có S có NTK cao nhất là 32. Nếu lấy các nguyên tử so sánh theo tỉ lệ viêt như sau
N: S= 14:32 ( 7: 16)
0: S= 16:32
F: S= 18:32
Na: S= 23:32
Tổng hạt là NTK
n / N = NKT - p .


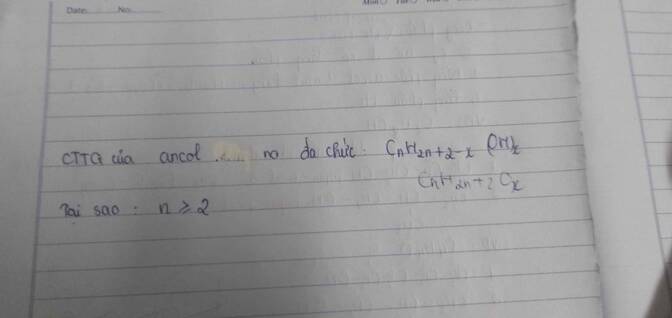

Bài 1:
\(PTK_{HCl}=1.1+35,5.1=36,5\left(đvC\right)\)
\(PTK_{Fe_3O_4}=56.3+16.4=232\left(đvC\right)\)
\(PTK_{KOH}=39.1+16.1+1.1=56\left(đvC\right)\)
\(PTK_{Al_2\left(SO_4\right)_3}=27.2+\left(32.1+16.4\right).3=342\left(đvC\right)\)
\(PTK_{FeCl_3}=56.1+35,5.3=162,5\left(đvC\right)\)
\(PTK_{H_3PO_4}=1.3+31.1+16.4=98\left(đvC\right)\)
\(PTK_{Al\left(OH\right)_3}=27.1+\left(16.1+1.1\right).3=78\left(đvC\right)\)
Bài 2:
Do số hạt mang điện là 22
\(\Rightarrow\left\{{}\begin{matrix}n=34-22=12\\p=e=\dfrac{22}{2}=11\end{matrix}\right.\)
A là Na(Natri)
Bài 3:
a) \(PTK_B=2.32=64\left(đvC\right)\)
b)
CTHH: XO2
\(PTK_B=NTK_X+2.16=64\left(đvC\right)\)
=> NTKX = 32 (đvC)
=> X là S (Lưu huỳnh)