Theo giá trị khối lượng tính bằng gam của nguyên tử Cacbon là 1,9926×10^-23 gam, hãy tính khối lượng bằng gam của nguyên tử Lưu Huỳnh
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


- Tổng số hạt cơ bản của nguyên tử A là 40: P+N=E= 40 (1)
- Nguyên tử A trung hoà về điện: P=E=Z (2)
- Mặt khác: N-P=1 (3)
(1), (2), (3) lập hệ:
\(\left\{{}\begin{matrix}P+E+N=40\\P=E=Z\\N-P=1\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}P=E=Z=13\\N=14\end{matrix}\right.\)
Với Z=13 => A là Nhôm (ZAl=13)
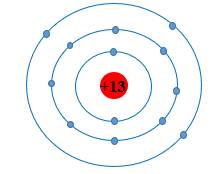
Cấu hình A: 1s22s22p63s23p1
Sơ đồ nguyên tử A:

\(n_{Cu}=\dfrac{9,6}{64}=0,15\left(mol\right)\\3 Cu+8HNO_3\rightarrow3Cu\left(NO_3\right)_2+2NO+4H_2O\\ n_{HNO_3}=\dfrac{8}{3}.0,15=0,4\left(mol\right)\\ n_{Cu\left(NO_3\right)_2}=n_{Cu}=0,15\left(mol\right)\\ n_{NO}=\dfrac{2}{3}.0,15=0,1\left(mol\right)\\ V=V_{NO\left(đktc\right)}=0,1.22,4=2,24\left(l\right)\\ m_{Cu\left(NO_3\right)_2}=188.0,15=28,2\left(g\right)\\ m_{HNO_3}=63.0,4=25,2\left(g\right)\)

\(Đặt.CTTQ:Fe_aO_b\left(a,b:nguyên,dương\right)\\ Ta.có:a=\dfrac{70\%.160}{56}=2\\ b=\dfrac{160-2.56}{16}=3\\ Với:a=2;b=3\Rightarrow CTHH:Fe_2O_3\left(Sắt\left(III\right)oxit\right)\)

\(Đặt:a=\%V_{H_2}\left(a>0\right)\\\overline{M}_{hhA}=8,5.2=17\left(\dfrac{g}{mol}\right)\\ \Leftrightarrow 2a+32.\left(100\%-a\right)=17\\ \Leftrightarrow a=50\%\\ \Rightarrow\%V_{H_2}=\%V_{O_2}=50\%\\ \%m_{H_2}=\dfrac{2}{2+32}.100\approx5,882\%\Rightarrow\%m_{O_2}\approx100\%-5,882\%\approx94,118\%\)

2KMnO4-to>K2MnO4+MnO2+O2
1------------------------------------0,5
m O2=16 g
->nO2=\(\dfrac{16}{32}\)=0,5 mol
=>%m KMnO4=\(\dfrac{1.158}{316}.100=50\%\)
\(2KMnO_4\underrightarrow{^{^{t^0}}}K_2MnO_4+MnO_2+O_2\)
Bảo toàn khối lượng :
\(m_{O_2}=m_{KMnO_4}-m_{Cr}=316-300=16\left(g\right)\)
\(n_{O_2}=\dfrac{16}{32}=0.5\left(mol\right)\)
\(\Rightarrow n_{KMnO_4}=0.5\cdot2=1\left(mol\right)\)
\(\%KMnO_{4\left(np\right)}=\dfrac{1\cdot158}{300}\cdot100\%=52.67\%\)

\(\overline{M}_{hhX}=\dfrac{2.44+3.16}{2+3}=27,2\left(\dfrac{g}{mol}\right)\\ \Rightarrow d_{\dfrac{X}{H_2}}=\dfrac{27,2}{2}=13,6\)

\(n_{Fe}=a\left(mol\right),n_{Al}=b\left(mol\right)\)
\(m_{hh}=56a+27b=11\left(g\right)\left(1\right)\)
\(n_{H_2}=\dfrac{8.96}{22.4}=0.4\left(mol\right)\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
\(a.........a..............a\)
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
\(b.........1.5b................1.5b\)
\(n_{H_2}=a+1.5b=0.4\left(mol\right)\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.1,b=0.2\)
\(\%Fe=\dfrac{0.1\cdot56}{11}\cdot100\%=50.91\%\)
\(\%Al=100\%-50.91\%=49.09\%\)
\(n_{H_2SO_4}=0.4\cdot2=0.8\left(mol\right)\)
\(C\%_{H_2SO_4}=\dfrac{0.8\cdot98}{200}\cdot100\%=39.2\%\)

\(m_{1đ.v.C}=\dfrac{1,9926.10^{-23}}{12}=0,16605.10^{-23}\left(g\right)\\ m_S=32.0,16605.10^{-23}=5,3136.10^{-23}\left(g\right)\)