Khái niệm AO xuất phát từ mô hình Rutherford – Bohr hay mô hình hiện đại về nguyên tử?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Xác suất tìm thấy electron trong toàn phần không gian bên ngoài đám mây là khoảng 10%.

- Electron ở càng xa hạt nhân thì năng lượng càng cao
=> Electron ở gần hạt nhân có mức năng lượng thấp hơn electron ở xa hạt nhân
=> Electron cần phải thu năng lượng để có thể chuyển từ lớp gần ra lớp xa hạt nhân

- Mô hình hành tinh nguyên tử mô tả về sự chuyển động của electron.
- Hình a không mô tả sự chuyển động của electron
- Hình b mô tả sự chuyển động của electron
=> Hình b thể hiện mô hình hành tinh nguyên tử và Hình a thể hiện mô hình hiện đại của nguyên tử.

Ta có: P+E+N= 34
Mà: P=E
=> 2P+N=34 => N= 34 - 2P
Mà:
\(P\le N\le1,5P\\ \Leftrightarrow P\le34-2P\le1,5P\\ \Leftrightarrow3P\le34\le3,5P\\ \Rightarrow11,33\ge P\ge9,71\\ \Rightarrow\left[{}\begin{matrix}P=E=Z=10\\P=E=Z=11\end{matrix}\right.\Leftrightarrow\left[{}\begin{matrix}N=14\left(loại\right)\\N=12\left(nhận\right)\end{matrix}\right.\)
Vậy: Với Z=11 => Nguyên tố đó là Natri (Na)

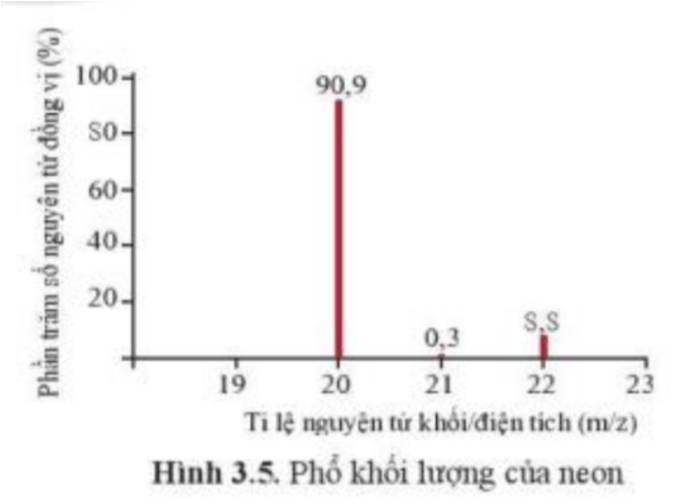
a) Neon có 3 đồng vị bền:
+ Đồng vị 20Ne chiếm 90,9%
+ Đồng vị 21Ne chiếm 0,3%
+ Đồng vị 22Ne chiếm 8,8%
b) Công thức tính nguyên tử khối trung bình: \(M = \frac{{aA + bB + cC + {\text{dD}} + ...}}{{100}}\)
=> \({M_{Ne}} = \frac{{90,9.20 + 0,3.21 + 8,8.22}}{{100}} = 20,18\)
Vậy nguyên tử khối trung bình của Neon là 20,18.

Ta có: nCu = 6,354 : 63,54 = 0,1 (mol)
Gọi tỉ lệ phần trăm của đồng vị 63Cu trong tự nhiên là x
=> Tỉ lệ phần trăm của đồng vị 65Cu trong tự nhiên là 100 – x
- Nguyên tử khối trung bình của Cu là 63,54
=> \(63,54 = \frac{{63.x + 65.(100 - x)}}{{100}}\)
=> x = 73
=> Tỉ lệ phần trăm của đồng vị 63Cu trong tự nhiên là 73%
=> Trong 0,1 mol Cu sẽ có 0,1.73% = 0,073 mol 63Cu
=> Trong 0,1 mol Cu sẽ có 0,1 - 0,073 = 0,027 mol 65Cu

Đáp án đúng là: A
A. Đúng. Những nguyên tử có cùng số proton thì thuộc cùng một nguyên tố hóa học.
Mà nguyên tử trung hòa về điện nên số proton = số electron
B. Sai. Để hai nguyên tử A và B thuộc cùng một nguyên tố hóa học thì A và B phải có cùng số proton.
C. Sai. Các nguyên tử mà hạt nhân có cùng số proton thuộc cùng một nguyên tố hóa học

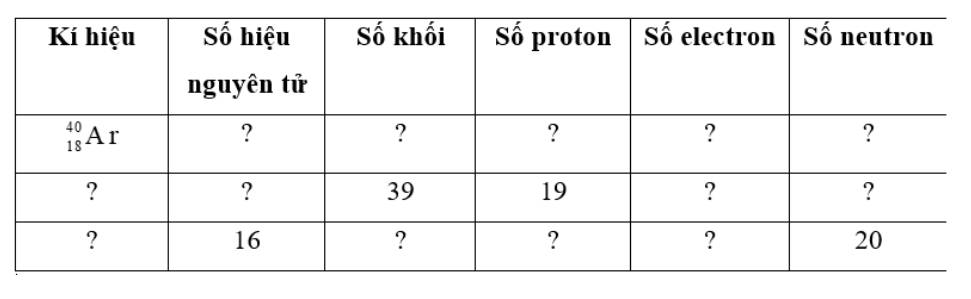
- \({}_{18}^{40}{\text{Ar}}\)
+ Có số hiệu nguyên tử = số proton = số electron = 18
+ Số khối = 40
+ Số neutron = 40 – 18 = 22
- Số khối = 39, số proton = 19 => Nguyên tố Kali (K)
+ Số hiệu nguyên tử = số proton = số electron = 19
+ Số neutron = 39 – 19 = 20
- Số hiệu nguyên tử = 16, số neutron = 20
+ Số hiệu nguyên tử = số proton = số electron = 16 => Nguyên tố lưu huỳnh (S)
+ Số khối = số proton + số neutron = 16 + 20 = 36
Hoàn thành bảng
Kí hiệu | Số hiệu nguyên tử | Số khối | Số proton | Số electron | Số neutron |
\({}_{18}^{40}{\text{Ar}}\) | 18 | 40 | 18 | 18 | 22 |
\({}_{19}^{39}K\) | 19 | 39 | 19 | 19 | 20 |
\({}_{16}^{36}S\) | 16 | 36 | 16 | 16 | 20 |

Khái niệm AO (orbital nguyên tử) xuất phát từ mô hình hiện đại về nguyên tử