Hoàn thành các phản ứng sau:
a) HCHO + HCN →
b) CH3COCH(CH3)2 + I2 + NaOH →
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


CH3 – CO – CH3 + 3 I2 + 4 NaOH → CH3COONa + 3 NaI + CHI3 + 3 H2O.

a: Thuốc thử Tollens là Ag(NH3)2OH
\(HCHO+2Ag\left(NH_3\right)_2OH\rightarrow\left(NH_4\right)_2CO_3+4Ag+2H_2O+6NH_3\)
b: \(HCHO+Cu\left(OH\right)_2+NaOH\rightarrow2Cu_2O+Na_2CO_3+6H_2O\)
a) HCHO + 2[Ag(NH3)2]OH → (NH4)2CO3 + 4Ag + 2H2O + 6NH3
b) HCHO + 4Cu(OH)2 + 2NaOH → 2Cu2O + Na2CO3 + 6H2O

1: Kết tủa đó là chất Cu(OH)2
2: \(CuSO_4+2NaOH\rightarrow Cu\left(OH\right)_2+Na_2SO_4\)
\(CH_3CHO+2Cu\left(OH\right)_2\rightarrow CH_3COONa+Cu_2O+3H_2O\)
1. Kết tủa Cu(OH)2
2.
\(CuSO_4+2NaOH\rightarrow Cu\left(OH\right)_2\downarrow\left(xanh.lam\right)+Na_2SO_4\\ 2Cu\left(OH\right)_2+CH_3CHO+NaOH\rightarrow CH_3COONa+Cu_2O\downarrow\left(đỏ.gạch\right)+3H_2O\)

*Tham khảo:
- Na2S là muối của natri và lưu huỳnh, có công thức hóa học là Na2S. Nó tồn tại dưới dạng bột màu trắng và tan trong nước. Na2S có mùi hắc và độc, được sử dụng trong công nghiệp để sản xuất các hợp chất lưu huỳnh khác.
- Na2SO3 là muối của natri và axit sulfurous, có công thức hóa học là Na2SO3. Nó tồn tại dưới dạng bột màu trắng và tan trong nước. Na2SO3 có tính khử mạnh và được sử dụng trong công nghiệp thực phẩm để làm chất chống oxy hóa và chất bảo quản.
- K2SO4 là muối của kali và axit sulfuric, có công thức hóa học là K2SO4. Nó tồn tại dưới dạng bột màu trắng và tan trong nước. K2SO4được sử dụng trong nông nghiệp như một nguồn cung cấp kali và lân cho cây trồng.
- K2CO3là muối của kali và axit cacbonic, có công thức hóa học là K2CO3 Nó tồn tại dưới dạng bột màu trắng và tan trong nước. K2 CO3 được sử dụng trong công nghiệp hóa chất và sản xuất thuốc nhuộm, thuốc tẩy và thuốc nhuộm.

Hiện tượng: Có lớp bạc sáng bóng bám vào thành ống nghiệm.
Giải thích: Vì aldehyde đã khử Ag+ trong thuốc thử Tollens về Ag.
Phương trình hoá học:
\(CH_3CHO+2\left[Ag\left(NH_3\right)_2\right]OH\rightarrow\left(t^o\right)CH_3COONH_4+2Ag+3NH_3+H_2O\)
Tham khảo:
- Thêm từ từ dung dịch NH3 5% vào ống nghiệm chứa 1 mL dung dịch AgNO3 1% và lắc nhẹ.
- Có kết tủa xám xuất hiện
PTHH: AgNO3 + NH3 + H2O → AgOH + NH4NO3
- Sau đó kết tủa tan dần, tạo dung dịch trong suốt
PTHH: AgOH + 2NH3 → [Ag(NH3)2]OH
- Nhỏ vài giọt dung dịch CH3CHO 5% vào ống nghiệm, lắc đều.
- Đun nóng nhẹ hỗn hợp trong ống nghiệm trên ngọn lửa đèn cồn.
- Hiện tượng: xuất hiện kết tủa màu trắng xám của kim loại bạc, bám vào thành ống nghiệm, có thể soi gương được.
CH3CHO + 2[Ag(NH3)2]OH \(\underrightarrow{t^o}\) CH3COONH4 + 2Ag + 3NH3 + H2O

Tham khảo:
a) CH3-CH2-CHO + 2[H] → CH3-CH2-CH2OH
b) CH3-CH2-CH(CH3)-CHO + 2[H] → CH3-CH2-CH(CH3)-CH2OH
c) CH3-CO-CH2-CH3 + 2[H] → CH3-CH(OH)-CH2-CH3
d) CH3-CO-CH(CH3)-CH3 + 2[H] → CH3-CH(OH)-CH(CH3)-CH3

Tham khảo:
- Các hợp chất carbonyl có nhiệt độ sôi cao hơn các hydrocarbon có khối lượng phân tử tương đương. Do trong phân tử có chứa nhóm carbonyl phân cực làm cho phân tử hợp chất carbonyl phân cực.
- Các hợp chất carbonyl có nhiệt độ sôi thấp hơn các alcohol có khối lượng phân tử tương đương. Do các hợp chất carbonyl không tạo được liên kết hydrogen liên phân tử như alcohol.
- Các hợp chất carbonyl có nhiệt độ sôi cao hơn các hydrocarbon có khối lượng phân tử tương đương.
Do trong phân tử có chứa nhóm carbonyl phân cực làm cho phân tử hợp chất carbonyl phân cực.
- Các hợp chất carbonyl có nhiệt độ sôi thấp hơn các alcohol có khối lượng phân tử tương đương.
Do các hợp chất carbonyl không tạo được liên kết hydrogen liên phân tử như alcohol.

Tham khảo:
a) propanal: CH3 – CH2 – CHO.
b) 3 – methylbut – 2 – enal: 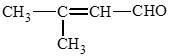
c) pentan – 2 – one: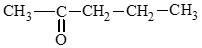
d) 3 – methylbutan – 2 – one.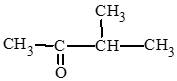
a) HCHO + HCN → HCH(OH)-CN
b) CH3COCH(CH3)2 + 3 I2 + 4 NaOH → (CH3)2CHCOONa + CHI3 + 3NaI + 3H2O
a) HCHO + HCN → HCH(OH)-CN
b) CH3COCH(CH3)2 + 3I2 + 4NaOH → (CH3)2CHCOONa + CHI3 + 3NaI + 3H2O