Cho 11,9 gam hỗn hợp gồm Al và Zn tan hoàn toàn trong dd H2SO4 loãng dư, có 8,96 lít khí thoát ra(đktc) . Tính khối lượng muối sunfat khan thu được?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


nCO2 =\(\dfrac{1,568}{22,4}\)=0,07 mol , n NaOH=\(\dfrac{6,4}{40}=0,16mol\)
Phương trình hóa học:
2NaOH + CO2 → Na2CO3 + H2O
Lúc ban đầu: 0,07 0,16 0 (mol)
Phản ứng: 0,07 → 0,14 0,07
Sau phản ứng: 0 0,02 0,07
Chất còn dư là NaOH và dư: 0,02.40 = 0,8 g

a) Sửa đề: XOy có hoá trị II
CTHH của A là \(MgXO_y\) (lập CTHH dựa trên quy tắc hoá trị)
\(PTK_A=3,75.32=120\left(g/mol\right)\)
=> \(y=\dfrac{120.53,33\%}{16}=4\)
=> A có dạng `MgXO_4`
`=> 24 + X + 16.4 = 120`
`=> X = 32`
`=> X: S`
b) `MgSO_4`

Gọi n NaCl=x mol , nKCl = y mol
n AgCl=0,4 mol
NaCl+AgNO3->NaNO3+AgCl
x-------------------x-----------x
KCl+AgNO3->KNO3+AgCl
y-------------------y--------------y
ta có hệ :
\(\left\{{}\begin{matrix}58,5x+74,5y=25\\x+y=0,4\end{matrix}\right.=>\left\{{}\begin{matrix}x=0,3\\y=0,1\end{matrix}\right.\)
=>m NaCl=0,3.58,5=17,55g
=>%mNaCl=70,2%
->%mKCl=29,8%
b)n AgNO3=n AgCl=0,4
=>m AgNO3=0,4.170=68g
m dd AgNO3=\(\dfrac{68}{0,17}\)=400g
->m ddY=100+400-57,4=442,6g
vậy mddY=442,6g

Số mol OH- = 0,5 . 0,4 = 0,2 mol mà số mol kết tủa Fe(OH)3 = 0,05 mol
Nên có 0,15 mol OH- tạo kết tủa và 0,05 mol OH- trung hòa lượng H+ còn lại.
Vậy số mol OH- dư trong Y là 0,05 . 2 = 0,1 mol
→ nên số H+ phản ứng là 0,6 mol H+.
Lập hệ số mol Fe là x ; Fe3O4 là y
⇒ 56x + 232y = 10,24
Bảo toàn e cho nhận: 3x + y = 0,3 + a
Số mol H+ phản ứng:
4.nNO + 2.nNO2 + 8.nFe3O4= 0,6 mol
→ 4.0,1 + 2a + 8y =0,6
Giải hệ ta được: a = 0,02; x = 0,1; y = 0,02 mol
Vậy nếu phản ứng với Ba(OH)2 dư thì sẽ có 0,08 mol Fe(OH)3; 0,05 mol BaSO4
Nên khối lượng là: 20,21 gam. (Chia 2 vì chỉ lấy 1 nửa dung dịch).

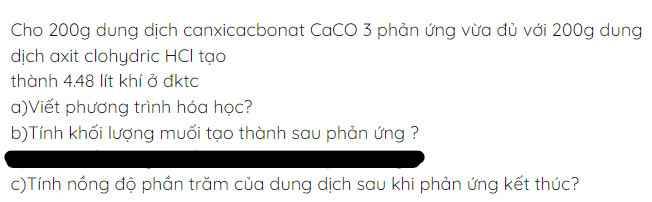
CaCO3 ko phải là chất dễ tan và không có dd cuả chúng
a) Số mol CO2 thu được ở đktc là:
nCO2 = \(\dfrac{4,48}{22,4}\) = 0,2 (mol)
PTHH: CaCO3 + 2HCl -> CaCl2 + H2O + CO2↑
----------0,2---------0,4--------0,2----0,2-------0,2
b)
Khối lượng CaCl2 tạo thành là:
mCaCl2 = n.M = 0,2.111 = 22,2 (g)
Nồng độ phần trăm dd thu được sau phản ứng là:
C%CaCl2 = (mct/mddspư).100 = \(\dfrac{22,2}{211,2}100\) ≃ 10,5 %

Mg(OH)2 + 2HCl → MgCl2+ 2H2O
Cu(OH)2 + 2HCl → CuCl2CuCl2 + 2H2O
NaOH + HCl → NaCl + H2O
Số mol HCl phản ứng : 0,4 x 1 = 0,4 (mol)
=> mHCl = 0,4 x 36,5 = 14,6 (gam)
Theo phương trình hoá học nH2O = nHCl = 0,4 mol
mH2O = 0,4 x 18 = 7,2g
Theo định luật bảo toàn khối lượng, ta có : m + 14,6 = 24,1 + 7,2
Vậy m = 16,7 gam.



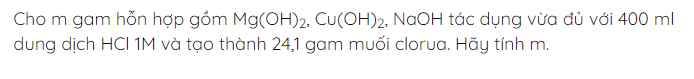
Bảo toàn H :n H2=n H2SO4=\(\dfrac{8,96}{22,4}=0,4mol\)
BTKLg :
m hh +m axit= m muối +m H2
=>m muối =11,9+0,4.98 -0,4.2=50,3g