
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Theo đề ta có : \(\left\{{}\begin{matrix}2.\left(2Z_M+N_M\right)+2Z_X+N_X=140\\2Z_M-2Z_X=22\\N_M-Z_M=1\\Z_X=N_X\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}Z_M=19\\N_M=20\\Z_X=8\\N_X=8\end{matrix}\right.\)
\(\left\{{}\begin{matrix}A_M=Z_M+N_M=19+20=39\\A_X=Z_X+N_X=8+8=16\end{matrix}\right.\)
=> M (Z=19) : Kali (K), X (Z=8) là Oxi (\(CTPT:O_2\))
Hợp chất A : K2O (Kali oxit)

2)Cho nguyên tố A có Z = 16 và B có Z = 26.
a) Viết cấu hình electron và xác định vị trí của A, B trong hệ thống tuần hoàn(số thứ tự, chu kỳ, phân nhóm, nhóm).
\(A:1s^22s^22p^63s^23p^4\)
=> A thuộc ô 16, chu kì 3, phân nhóm A, nhóm IA
\(B:1s^22s^22p^63s^23p^63d^64s^2\)
=> B thuộc ô 26, chu kì 4, phân nhóm B, nhóm VIIIB
b)A, B là kim loại hay phi kim ? Giải thích.
A là phi kim do có 6e lớp ngoài cùng
B là kim loại do có 2e lớp ngoài cùng

\(SO_3+Ba\left(OH\right)_2\rightarrow BaSO_4+H_2O\\ n_{BaSO_4}=n_{SO_3}=\dfrac{12}{80}=0,15\left(mol\right)\\ m_{dd.giảm}=m_{BaSO_4}-m_{SO_3}=0,15.233-12=22,95\left(g\right)\)
=> Dung dịch X giảm 22,95 gam so với dung dịch ban đầu.
so với Ba(OH)2 cơ mà ạ sao lại lấy mbaso4- mso3 là s ạ

\(\Sigma m_{NaOH}=0,5.5.40+200.1,33.30\%=179,8\left(g\right)\)
\(m_{dd}=\left(500+200\right).1,33=931\left(g\right)\)
\(\Rightarrow C\%_{NaOH}=\dfrac{179,8}{931}.100=19,31\%\)

1.a) \(A+HCl\rightarrow ACl+\dfrac{1}{2}H_2\)
Ta có : \(n_A=2n_{H_2}=2.\dfrac{2,8}{22,4}=0,25\left(mol\right)\)
\(\Rightarrow M_A=\dfrac{9,75}{0,25}=39\)
Vậy A là Kali (K)
b)\(n_{HCl}=2n_{H_2}=0,25\left(mol\right)\)
\(\Rightarrow m_{HCl}=0,25.26,5=9,125\left(g\right)\)
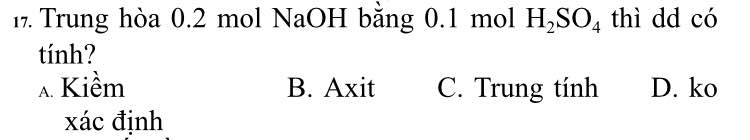
C
Cặp chất có thể tồn tại trong dung dịch khi 2 chất đó không phản ứng được với nhau
=> Chọn C. KCl và NaNO3
A loại vì : \(BaCl_2+CuSO_4\rightarrow BaSO_4+CuCl_2\)
B loại vì : \(2NaOH+H_2SO_4\rightarrow Na_2SO_4+2H_2O_{ }\)
D loại vì : \(Na_2CO_3+2HCl\rightarrow2NaCl+H_2O\)