Cho 21,7g hỗn hợp X gồm khi loại BA và KL R tác dụng hết với nước dư thu được 6,72g lít khí H2
a, tìm kim loại R
b, tính % theo khối lượng mỗi kim loại trong hỗn hợp X
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Câu 6:
Gọi a, b là số mol của KClO3 và KMnO4
TH1 : Y có CO2, N2 và O2 dư
KClO3 ----> KCl + 3/2 O2
2 KMnO4 ----> K2MnO4 + MnO2 + O2
gọi nO2 = x ; =>nO2/kk = 3x*0.2 = 0.6x , nN2 = 3x*0.2 = 2.4x
hh khí gồm nO2 = 1.6x ; nN2 = 2.4x
Pt
C + O2 ---> CO2
n CO2 = nC = 0. 528/12 = 0.044
hh khí gồm : n CO2 = 0.044 ; nO2 = 1.6x - 0.044 ; nN2 = 2.4x
=> 0.044 + 1.6x - 0.044 + 2.4x = 0.044*100/22.92
<=> x = 0.048
=> mhh đầu = mY + mO2 = 0.894*100/8.132 + 0.048*32 = 12.53
TH 2 : Y có CO, CO2, N2
bảo toàn C : nCO + nCO2 = nC = 0.044 => nCO = 0.044 - nCO2
bảo toàn O : 0.5*nCO + nCO2 = nO2 = 1.6a
thay * vào được 0.5*(0.044 - nCO2) + nCO2 = 1.6a =>nCO2 = 3.2a- 0.044
tổng mol hh : nCO + nCO2 + nN2 = 0.044 + 2.4a
=>(3.2a - 0.044 )/( 0.044 + 2.4a ) = 22.92/100
a = sấp sỉ 0.02
=> m = m rắn + mO2 = 0.894*100/8.132 + 0.02 * 32 = 11,646 gam
#cre:hoc24
Câu 2:
a) số hạt nơ tơ ron = ( 52 - 16)/2 = 18
Số hạt e = số hạt p = (52 - 18)/2= 17
b)
lớp 1 có 2 e
lớp 2 có 8 e
lớp 3 có 7 e
c ) nguyên tử khối của X = ( 52 - 17) . 1,013 = 35.455 đvc
d) khối lượng bằng gam của X = 35.455 . 1/ 6,02x10^ 23 = 35.455/6,02x10^ 23
Vì 1đvc = 1/6,02x10^ 23 gam
Câu 3
% K = 100% - ( 37,65% +16,47%) = 45.88%
đặt CTHH của B là KxNyOz
X: Y : Z = 45.88/39 : 16,47/14 : 37,65/16 = 1:1:2
Vậy B là KNO2 vậy A là KNO3

mk viết gọn nhé !!
C4H10.............. CH3_CH2_CH2_CH3
C3H6....................CH2=CH-CH3
C2H6O..............CH3_CH2_OH
CH3CL...............CH3_CL
C3H7Br................CH3_CH2_CH2_Br
cái cuối k rõ CT
C4H10: CH3-CH2-CH2-CH3
CH3-CH(CH3)-CH3
C3H6: CH2=CH2=CH2
CH3-CH=CH2
C2H6O: CH3-CH2-O-H
CH3-O-CH3
CH3Cl: CH3-Cl
C3H7Br: CH3-CH2-CH2-Br
CH3-Br-CH-CH3
còn cái công thức cuối ko rõ nên mình ko làm nhak

Gọi x, y, z lần lượt là các số mol của CH4 , C2H4 và C2H2 có trong 2,8 lít hỗn hợp:
nhh = 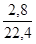 = 0, 125 mol
= 0, 125 mol
Khi cho 2,8 lít hỗn hợp đi qua bình đựng nướcBrôm chỉ có C2H4 và C2H2 phản ứng
Phương trình phản ứng:
C2H4 + Br2 -> C2H4Br2
C2H2 + 2 Br2 -> C2H2Br
Ta có: nBr2 = y + 2z =  = 0, 125
= 0, 125
Đốt cháy 5,6 lít hỗn hợp
CH4 + 2O2 -> CO2 + 2h2O
2x 2x
C2H4 + 3O2-> 2CO2 + 2H2O
2y 4y
2C2H2 + O2 -> 4 CO2 + 2 H2O
2z 4z
Ta có: n CO2 = 2x + 4y + 4z = 0,375 + y
n NaOH = 0,876 mol
CO2 + 2NaOH -> Na2CO3 + H2O
1mol 2mol
n NaOH phản ứng = 2n CO2 = 0,75 + 2y
n NaOH dư = 0, 876 - 0,75 - 2y = 0,126 - 2y
Ta có hệ phương trình 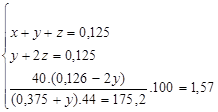
Giải hệ ta được: y = 0,025
x = z = 0, 05
% CH4 = 40%
% C2H4 = 20%
% C2H2 = 40%
bạn ơi mình ko hiểu từ chỗ nầy làm chi tiết hơn được ko
Ta có: n CO2 = 2x + 4y + 4z = 0,375 + y
n NaOH = 0,876 mol
CO2 + 2NaOH -> Na2CO3 + H2O
1mol 2mol
n NaOH phản ứng = 2n CO2 = 0,75 + 2y
n NaOH dư = 0, 876 - 0,75 - 2y = 0,126 - 2y

mddHCl=52,14.1,05=54,747(g)
=>mHCl=54,747.10/100=5,4747(g)
=>nHCl=5,4747/36,5~0,15(mol)
FexOy+2y HCl---> xFeCl2y/x+yH2O
0,075/y___0,15
Ta có:
4=0,075/y(56x+16y)
=>x/y=2/3
=>CT: Fe2O3
ptpứ : FexOy + 2yHCl --> xFeCl2y/x + yH2O
mddHCl = 52,14x1,05 = 54,75(g)
nHCl = 54,75x10%/36,5 = 0,15(mol)
=>nFexOy = 0,15/2y(mol)
=>mFexOy = 4g
nên MFexOy = 4x2y/0,15 =160y/3
maMFexOy = 56x+16y
=>56x+16y = 160y/3
Giải pt trên ta dc x=2,y=3.Vậy công thức của oxit sắt là Fe2O3

nCa(OH)2 1M=1.0,3=0,3(mol)
nCa(OH)2 2,5M=2,5.0,2=0,5(mol)
=>nCa(OH)2 sau khi trộn=0,5+0,3=0,8(mol)
Vdd=300+200=500(ml)
=>CM=0,8/0,5=1,6(M)

a.
- Lấy mẫu thử vả đánh dấu
- Dẫn các mẫu thử vào nước vôi trong
+ Mẫu thử xuất hiện kết tủa trắng chất ban đầu là SO2
SO2 + Ca(OH)2 → CaSO3 + H2O
+ Mẫu thử không hiện tượng chất ban đầu là CH4, C2H2, C2H4 (I)
- Cho dung dịch brom vào nhóm I
+ Mẫu thử không làm mất màu dung dịch brom chất ban đầu là CH4
+ Mẫu thử lám mất màu dung dịch brom là C2H4 và C2H2 (II)
C2H4 + Br2→ C2H4Br2
C2H2 + 2Br2 → C2H2Br4
- Cho Ag2O vào nhóm II
+ Mẫu thử xuất hiện kết tủa vàng chất ban đầu là C2H2
C2H2 + Ag2O ---NH3---> C2Ag2 + H2O
+ Mẫu thử không hiện tượng chất ban đầu là C2H4
b.
- Lấy mẫu thử và đánh dấu
- Dẫn các mẫu thử vào nước vôi trong
+ Mẩu thử xuất hiện kết tủa trắng chất ban đầu là CO2
CO2 + Ca(OH)2 → CaCO3 + H2O
+ Mẫu thử không hiên tượng chất ban đầu là CH4, C2H4, H2 (I)
- Dẫn nhóm I vào dung dịch brom
+ Mẫu thử làm mất màu dung dịch brom chất ban đầu là C2H4
C2H4 + Br2 → C2H4Br2
+ Mẫu thử không hiện tượng chất ban đầu là CH4, H2 (II)
- Dẫn khí clo vào nhóm II
+ Mẫu thử làm mất màu của khí clo chất ban đầu là CH4
CH4 + Cl2 ---ánh sáng---> CH3Cl + HCl
+ Mẫu thử không hiện tượng chất ban đầu là H2

gọi kim loại đó là A
2A + O2 ==> 2AO
0,2<==0,1
ta có :
mO2= 16,2-13= 3,2 g
=> nO2= 3,2/32= 0,1 mol
MA= 13/0,2=65 g
=> A là kẽm (Zn)