Nung 31,32 gam dung dịch X gồm FexOy và sắt (II) cacbonat trong không khí đến khi khối lượng không đổi. Sau khi phản ứng kết thúc, thu được 26,40 gam một oxit sắt duy nhất và V lít khí CO2 (đktc). Hấp thụ hết lượng khí CO2 vào 120ml dung dịch Ca(OH)2 1M, kết thúc phản ứng thu được 9,00 gam kết tủa
a/ Viết các phương trình phản ứng hóa học xảy ra.
b/ Xác định công thức FexOy, tính V và phần trăm về khối lượng của FexOy trong hỗn hợp rắn X
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a)
\(C+O_2\xrightarrow[]{t^o}CO_2\) (1)
\(2C+O_2\xrightarrow[]{t^o}2CO\) (2)
\(Fe_3O_4+CO\xrightarrow[]{t^o}3FeO+CO_2\) (3)
\(Fe_3O_4+4CO\xrightarrow[]{t^o}3Fe+4CO_2\) (4)
\(Ba\left(OH\right)_2+CO_2\rightarrow BaCO_3\downarrow+H_2O\) (5)
\(Ba\left(OH\right)_2+2CO_2\rightarrow Ba\left(HCO_3\right)_2\) (6)
\(Ba\left(HCO_3\right)_2\xrightarrow[]{t^o}BaCO_3\downarrow+CO_2\uparrow+H_2O\) (7)
\(Fe+CuSO_4\rightarrow FeSO_4+Cu\) (8)
b)
Ta có: \(\left\{{}\begin{matrix}n_{BaCO_3\left(5\right)}=\dfrac{19,7}{197}=0,1\left(mol\right)\\n_{BaCO_3\left(7\right)}=\dfrac{14,775}{197}=0,075\left(mol\right)\end{matrix}\right.\)
Theo (5): \(n_{Ba\left(HCO_3\right)_2}=n_{BaCO_3\left(7\right)}=0,075\left(mol\right)\)
Theo (3), (4): \(n_{CO_2}=2n_{Ba\left(HCO_3\right)_2}+n_{BaCO_3\left(5\right)}=0,3\left(mol\right)\)
BTNT C: \(n_C=n_{CO_2}=0,3\left(mol\right)\)
=> m = 0,3.12 = 3,6 (g)
\(n_{Fe_3O_4}=\dfrac{23,2}{232}=0,1\left(mol\right)\)
Theo (8): \(n_{Fe}=n_{Cu}=n_{CuSO_4\left(pư\right)}=0,03\left(mol\right)\)
Gọi \(\left\{{}\begin{matrix}n_{FeO}=x\left(mol\right)\\n_{Fe_3O_4}=y\left(mol\right)\end{matrix}\right.\)
=> 72x + 232y = 21,84 - 0,03.64 = 19,92 (*)
BTNT Fe: \(3n_{Fe_3O_4\left(bđ\right)}=3n_{Fe_3O_4\left(dư\right)}+n_{FeO}+n_{Fe}\)
=> x + 3y = 3.0,1 - 0,03 = 0,27 (**)
Từ (*), (**) => \(\left\{{}\begin{matrix}x=0,18\\y=0,03\end{matrix}\right.\)
=> mB = 0,18.72 + 0,03.232 + 56.0,03 = 21,6 (g)
Theo BTNT: \(m_{O\left(pư\right)}=m_{giảm}=23,2-21,6=1,6\left(g\right)\)
=> \(n_{O\left(pư\right)}=\dfrac{1,6}{16}=0,1\left(mol\right)\)
Theo (3), (4): \(n_{CO_2\left(sinh.ra\right)}=n_{CO}=n_{O\left(oxit\right)}=0,1\left(mol\right)\)
=> \(n_{CO_2\left(1\right)}=0,3-0,1=0,2\left(mol\right)\)
=> \(\overline{M}_A=\dfrac{0,2.44+0,1.28}{0,2+0,1}=\dfrac{116}{3}\left(g/mol\right)\)
=> \(d_{A/H_2}=\dfrac{\dfrac{116}{3}}{2}=\dfrac{58}{3}\)

$n_{H_2SO_4} = 0,2.0,3 = 0,06(mol)$
$n_{NaOH} = 0,06.0,5 = 0,03(mol)$
$2NaOH + H_2SO_4 \to Na_2SO_4 + 2H_2O$
$n_{H_2SO_4\ dư} = \dfrac{1}{2}n_{NaOH} = 0,015(mol)$
$n_{H_2SO_4\ pư} = 0,06 - 0,015 = 0,045(mol)$
$R + H_2SO_4 \to RSO_4 + H_2$
$n_R = n_{H_2SO_4} = 0,045(mol)$
$\Rightarrow R = \dfrac{1,44}{0,045} = 32$
(Sai đề)

Trích mẫu thử
Cho quỳ tím vào các mẫu thử
- mẫu thử làm quỳ tím hóa xanh là $NaOH$
- mẫu thử không đổi màu quỳ tím là $Na_2SO_4$
- mẫu thử làm quỳ tím hóa đỏ là $H_2SO_4,HCl$
Cho dung dịch $BaCl_2$ vào hai mẫu thử còn :
- mẫu thử tạo kết tủa trắng là $H_2SO_4$
$BaCl_2 + H_2SO_4 \to BaSO_4 + 2HCl$
- mẫu thử không hiện tượng là HCl
_ Trích mẫu thử.
_ Nhỏ vài giọt từng mẫu thử vào giấy quỳ tím.
+ Nếu quỳ tím chuyển xanh, đó là NaOH.
+ Nếu quỳ tím chuyển đỏ, đó là H2SO4, HCl. (1)
+ Nếu quỳ tím không đổi màu, đó là Na2SO4.
_ Nhỏ một lượng từng mẫu thử nhóm (1) vào ống nghiệm chứa dd Ba(NO3)2.
+ Nếu xuất hiện kết tủa trắng, đó là H2SO4.
PT: \(Ba\left(NO_3\right)_2+H_2SO_4\rightarrow BaSO_{4\downarrow}+2HNO_3\)
+ Nếu không hiện tượng, đó là HCl.
_ Dán nhãn.

$n_{K_2CO_3} = 0,02(mol) ; n_{KHCO_3} = 0,02(mol)$
Vì $K_2CO_3,KHCO_3$ phản ứng đồng thời với dung dịch $HCl$
nên ta gọi : $n_{K_2CO_3\ pư} = 0,02a(mol) ; n_{KHCO_3\ pư} = 0,02a(mol)$
$K_2CO_3 + 2HCl \to 2KCl + CO_2 + H_2O$
$KHCO_3 + HCl \to KCl + CO_2 + H_2O$
$n_{HCl} = 2n_{K_2CO_3} + n_{KHCO_3} = 0,02a.2 + 0,02a = 0,025.1,2$
Suy ra : a = 0,5
$n_{CO_2} = n_{K_2CO_3} + n_{KHCO_3} = 0,04a = 0,02(mol)$

Vì không thấy xuất hiện kết tủa => HCl dư, Na2CO3 hết
\(Na_2CO_3+2HCl\rightarrow2NaCl+CO_2\uparrow+H_2O\)
b----------------------------------->b
=> V = 22,4b
=> Chọn B

Ta có: \(\left\{{}\begin{matrix}n_{M_2O_3}=\dfrac{8}{2M_M+48}=\dfrac{4}{M_M+24}\left(mol\right)\\n_{H_2SO_4}=0,3.1=0,3\left(mol\right)\\n_{NaOH}=\dfrac{50.24\%}{40}=0,3\left(mol\right)\end{matrix}\right.\)
PTHH:
\(M_2O_3+3H_2SO_4\rightarrow M_2\left(SO_4\right)_3+3H_2O\)
\(\dfrac{4}{M_M+24}\rightarrow\dfrac{12}{M_M+24}\)
\(2NaOH+H_2SO_4\rightarrow Na_2SO_4+2H_2O\)
0,3--------->0,15
=> \(\dfrac{12}{M_M+24}+0,15=0,3\)
=> \(M_M=56\left(g/mol\right)\)
=> M là Fe
CTHH của oxit là `Fe_2O_3`

a) `NaOH + H_2SO_4 -> NaHSO_4 + H_2O`
b) `2NaOH + H_2SO_4 -> Na_2SO_4 + 2H_2O`

a) $n_{CO_2} = \dfrac{1,568}{22,4} = 0,07(mol)$
$n_{NaOH} = \dfrac{6,4}{40} = 0,16(mol)$
$2NaOH + CO_2 \to Na_2CO_3 + H_2O$
Ta thấy :
$n_{NaOH} : 2 > n_{CO_2} : 1$ nên NaOH dư
$n_{NaOH\ pư} = 2n_{CO_2} = 0,14(mol)$
$m_{NaOH\ dư} = 6,4 - 0,14.40 = 0,8(gam)$
b) $n_{Na_2CO_3} = n_{CO_2} = 0,07(mol)$
$m_{Na_2CO_3} = 0,07.106 = 7,42(gam)$

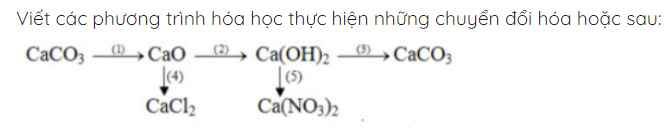
(1) \(CaCO_3\underrightarrow{t^o}CaO+CO_2\)
(2) \(CaO+H_2O\rightarrow Ca\left(OH\right)_2\)
(3) \(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3+H_2O\)
(4) \(CaO+2HCl\rightarrow CaCl_2+H_2O\)
(5) \(Ca\left(OH\right)_2+2HNO_3\rightarrow Ca\left(NO_3\right)_2+2H_2O\)



a)
\(4Fe_xO_y+\left(3x-2y\right)O_2\xrightarrow[]{t^o}2xFe_2O_3\) (1)
\(4FeCO_3+O_2\xrightarrow[]{t^o}2Fe_2O_3+4CO_2\uparrow\) (2)
\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3\downarrow+H_2O\) (3)
Có thể có: \(2CO_2+Ca\left(OH\right)_2\rightarrow Ca\left(HCO_3\right)_2\) (4)
b) Ta có: \(\left\{{}\begin{matrix}n_{CaCO_3}=\dfrac{9}{100}=0,09\left(mol\right)\\n_{Ca\left(OH\right)_2}=0,12.1=0,12\left(mol\right)\\n_{Fe_2O_3}=\dfrac{26,4}{160}=0,165\left(mol\right)\end{matrix}\right.\)
TH1: không xảy ra (3)
Theo PT: \(n_{Ca\left(OH\right)_2\left(pư\right)}=n_{CO_2}=n_{CaCO_3}=0,09\left(mol\right)\)
Nhận xét: \(0,09< 0,12\) => \(Ca\left(OH\right)_2\) dư (tm)
Theo (2): \(n_{FeCO_3}=n_{CO_2}=0,09\left(mol\right)\)
=> \(m_{Fe_xO_y}=31,32-0,09.116=20,88\left(g\right)\)
BTNT Fe: \(x.n_{Fe_xO_y}+n_{FeCO_3}=2n_{Fe_2O_3}\)
=> \(n_{Fe_xO_y}=\dfrac{2.0,165-0,09}{x}=\dfrac{0,24}{x}\left(mol\right)\)
=> \(M_{Fe_xO_y}=\dfrac{20,88}{\dfrac{0,24}{x}}=87x\left(g/mol\right)\)
=> 56x + 16y = 87x
=> \(\dfrac{x}{y}=\dfrac{16}{31}\) (Loại)
TH2: có xảy ra PT (3):
BTNT Ca: \(n_{Ca\left(HCO_3\right)_2}=n_{Ca\left(OH\right)_2}-n_{CaCO_3}=0,03\left(mol\right)\)
BTNT C: \(n_{FeCO_3}=n_{CO_2}=n_{CaCO_3}+n_{Ca\left(HCO_3\right)_2}=0,15\left(mol\right)\)
=> \(m_{Fe_xO_y}=31,32-0,15.116=13,92\left(g\right)\)
BTNT Fe: \(x.n_{Fe_xO_y}+n_{FeCO_3}=2n_{Fe_2O_3}\)
=> \(n_{Fe_xO_y}=\dfrac{2.0,165-0,15}{x}=\dfrac{0,18}{x}\left(mol\right)\)
=> \(M_{Fe_xO_y}=\dfrac{13,92}{\dfrac{0,18}{x}}=\dfrac{232}{3}x\left(g/mol\right)\)
=> \(56x+16y=\dfrac{232}{3}x\)
=> \(\dfrac{x}{y}=\dfrac{3}{4}\)
=> FexOy là Fe3O4
\(n_{Fe_3O_4}=\dfrac{0,18}{x}=\dfrac{0,18}{3}=0,06\left(mol\right)\)
=> \(\%m_{Fe_3O_4}=\dfrac{0,06.232}{31,32}.100\%=44,44\%\)