hấp thụ hết V lít CO2 (dktc)vào bình đựng 240 ml dung dịch NaOH 1,25M thu được dung dịch chứa 25,35 gam chất tan. Tìm V
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Gọi CT hidrocacbon cần tìm là CxHy (x,y \(\in\) N*)
Ta có : \(n_{CO_2}=\dfrac{22}{44}=0,5\left(mol\right)\) => nC = 0,5 (mol)
\(n_{H_2O}=\dfrac{13,5}{18}=0,75\Rightarrow n_H=1,5\left(mol\right)\)
Vì n CO2 < n H2O => hidrocacbon là ankan
=> \(n_A=0,75-0,5=0,25\left(mol\right)\)
BTNT O => \(n_{O_2}=\dfrac{0,5.2+0,75}{2}=0,875\left(g\right)\)
Bảo toàn khối lượng => m A = 22+13,5 - 0,875.32=7,5 (g)
=> \(M_A=\dfrac{7,5}{0,25}=30\)(g/mol)
=> x:y= 0,5 : 1,5 = 1:3
=> CTĐGN : (CH3)n
Ta có : 15n=30
=> n=2
=> CTPT của A : C2H6

nCuO=16/80=0,2(mol)
a) PTHH: CuO + H2SO4 -> CuSO4 + H2O
0,2___________0,2_____0,2(mol)
b) mCuSO4=160.0,2=32(g)
c) mH2SO4=0,2.98=19,6(g)
=>C%ddH2SO4= (19,6/100).100=19,6%

Câu 70: Chất được sử dụng để trung hòa axit là
A. Al(OH)3.
B. Fe(OH)2.
C. NaOH.
D. Cu(OH)2.

Số mol của khí cacbonic ở dktc
nCO2 = \(\dfrac{V_{CO2}}{22,4}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
a) CO2 + Ba(OH)2 → BaCO3 + H2O\(|\)
1 1 1 1
0,15 0,15 0,15
b) Số mol của bari cacbonat
nBaCO3 = \(\dfrac{0,15.1}{1}=0,15\left(mol\right)\)
Khối lượng của bari cacbonat
mBaCO3 = nBaCO3 . MBaCO3
= 0,15 . 197
= 29,55 (g)
Số mol của dung dịch bari hidroxit
nBa(OH)2 = \(\dfrac{0,15.1}{1}=0,15\left(mol\right)\)
300ml = 0,3l
Nồng độ mol của dung dịch bari hidroxit
CMBa(OH)2 = \(\dfrac{n}{V}=\dfrac{0,15}{0,3}=0,5\left(M\right)\)
Chúc bạn học tốt

Đặt nK2O=a(mol); nK2O=b(mol) (a,b>0)
Ta có: nHCl=0,6(mol)
K2O + H2O -> 2 KOH
a____________2a(mol)
Na2O + H2O -> 2 NaOH
b___________2b(mol)
KOH + HCl -> KCl + H2O
2a____2a____2a(mol)
NaOH + HCl -> NaCl + H2O
2b___2b______2b(mol)
Ta có hpt:
\(\left\{{}\begin{matrix}94a+62b=25\\2a+2b=0,6\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,2\\b=0,1\end{matrix}\right.\)
=> mK2O=0,2.94=18,8(g)
=>%mK2O= (18,8/25).100=75,2%
=>%mNa2O=24,8%
b) m(muối)= mKCl+ mNaCl= 74,5.0,4+ 58,5.0,2=41,5(g)

nMgO=4,8/40=0,12(mol)
nHCl= (7,3%.300)/36,5= 0,6(mol)
PTHH: MgO + 2 HCl -> MgCl2 + H2O
Ta có: 0,6/2 > 0,12/1
-> MgO hết, HCl dư , tisnhh theo nMgO
=> Chất tan trong dd thu được có: MgCl2 và HCl(dư)
nMgCl2=nMgO=0,12(mol)
=> mMgCl2= 95.0,12=11,4(g)
nHCl(dư)= 0,6 -0,12.2=0,36(mol)
=>mHCl(dư)=0,36.36,5=13,14(g)
mddsau= mMgO + mddHCl= 4,8+300= 304,8(g)
=>C%ddMgCl2= (11,4/304,8).100=3,74%
C%ddHCl(dư)= (13,14/304,8).100=4,311%

a) Lúc đầu: C12H22O11 + H2SO4 → 12C(đen) + H2SO4.11H2O
Sau đó: C12H22O11 + 24H2SO4 → 12CO2↑ + 24SO2↑ + 35H2O
Khi nhỏ axit H2SO4 đặc vào saccarozo, ta thấy đường nhanh chóng hóa đen, sau đó khối rắn tăng thể tích rất nhanh và thoát khí mùi hắc (SO2). Quan sát phương trình ta thấy chỉ 1 mol đường nhưng tạo ra những (12 + 24 = 35) mol khí, vì vậy thể tích khối rắn tăng lên nhanh.
b) 3H2SO4 + 2Fe(OH)3 ⟶ Fe2(SO4)3 + 6H2O
Hiện tượng : Chất rắn màu nâu đỏ Sắt III hidroxit (Fe(OH)3) tan dần trong dung dịch H2SO4, tạo ra dung dịch màu vàng nâu
c) CuO + 2HCl ⟶ 2H2O + CuCl2
Hiện tượng : Chất rắn màu đen đồng II oxit (CuO) tan dần trong dd, tạo thành dd màu xanh lam là CuCl2.
d)Cu + 2H2SO4 ⟶ 2H2O + SO2 + CuSO4
Hiện tượng: Chất rắn màu đỏ Đồng (Cu) tan dần trong dung dịch và sủi bọt khí do khí mùi hắc Lưu huỳnh dioxit (SO2) sinh ra.
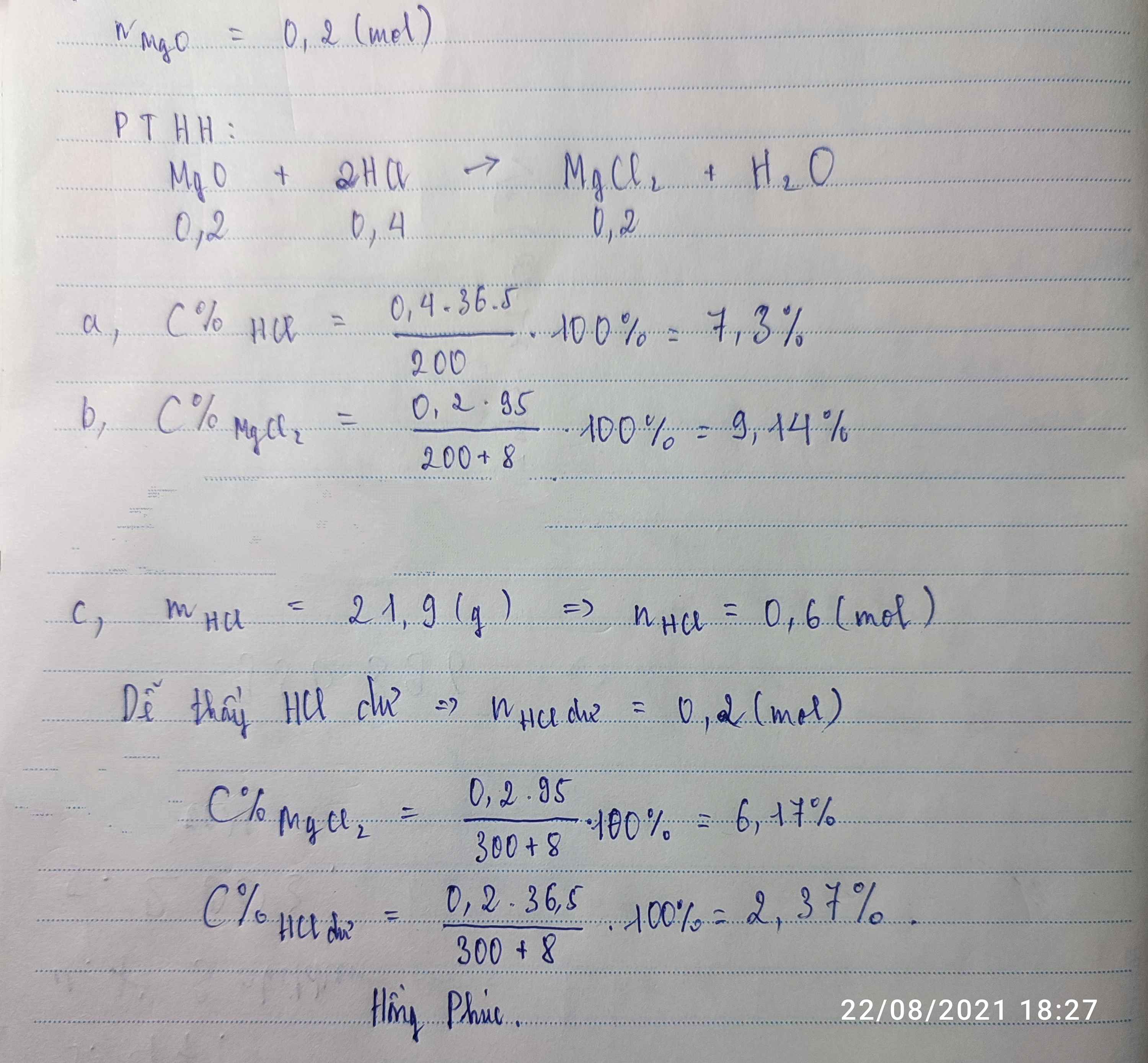
\(n_{NaOH}=0,24.1,25=0,3mol\)
Nếu muối là \(Na_2CO_3\)
\(\rightarrow n_{Na_2CO_3}=0,5n_{NaOH}=0,15\)
\(\rightarrow m_{Na_2CO_3}=0,15.106=15,9< 25,35\)
Nếu muối là \(NaHCO_3\)
\(\rightarrow n_{NaHCO_3}=n_{NaOH}=0,3\)
\(\rightarrow m_{NaHCO_3}=0,3.84=25,2< 25,35\)
Vậy tạo muối \(\hept{\begin{cases}x\left(mol\right)=Na_2CO_3\\y\left(mol\right)=NaHCO_3\end{cases}}\)
Bảo toàn Na là \(2x+y=0,3\)
Mặt khác \(106x+84y=25,35\)
Ta giải được nghiệm âm
Bạn xem lại đề nhé