Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Hòa tan 9,4g một oxit kim loại hóa trị I vào H2O, thu được 200ml dung dịch Bazơ 1M.
Tìm oxit kim loại

PTHH: A2O + H2O → 2AOH
\(n_{AOH}\) = 0,2 ×1=0,2 ( mol ) ( vì 200 ml = 0,2 l )
Theo PT: \(n_{A_2O}=\dfrac{1}{2}n_{AOH}=\) = 12 × 0,2 = 0,1 ( mol )
⇒ \(M_{A_2O}=\dfrac{9,4}{0,1}=94\) ( G )
Ta có: 2\(M_A\) + 16 = 94
⇔ 2\(M_A\)= 78
⇔ \(M_A\) =39 ( g )
Vậy A là kim loại Kali K

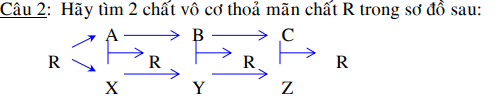
R là NaCl
A là Na, X là Cl2
B là NaOH, Y là HCl
C là Na2SO4, Z là BaCl2
\(NaCl-^{đpnc}\rightarrow Na+\dfrac{1}{2}Cl_2\)
\(Na+H_2O\rightarrow NaOH+\dfrac{1}{2}H_2\)
\(Cl_2+H_2-^{as}\rightarrow2HCl\)
\(NaOH+HCl\rightarrow NaCl+H_2O\)
\(2NaOH+H_2SO_4\rightarrow Na_2SO_4+2H_2O\)
\(2HCl+BaO\rightarrow BaCl_2+H_2O\)
\(BaCl_2+Na_2SO_4\rightarrow BaSO_4+2NaCl\)

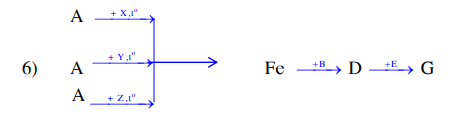
A là Fe2O3
D là FeCl2
G là ZnCl2
X là H2, Y là CO, Z là Al
B là HCl , E là Zn
\(Fe_2O_3+3H_2-^{t^o}\rightarrow2Fe+3H_2O\)
\(Fe_2O_3+3CO-^{t^o}\rightarrow2Fe+3CO_2\)
\(Fe_2O_3+2Al-^{t^o}\rightarrow2Fe+Al_2O_3\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(Zn+FeCl_2\rightarrow ZnCl_2+Fe\)

a) \(ZnO+2HCl\rightarrow ZnCl_2+H_2O\)
\(n_{ZnO}=\dfrac{16,2}{81}=0,2\left(mol\right)\)
\(n_{HCl}=2n_{ZnO}=0,4\left(mol\right)\)
=> \(C\%_{HCl}=\dfrac{0,4.36,5}{600}.100=2,43\%\)
b)\(n_{ZnCl_2}=n_{ZnO}=0,2\left(mol\right)\)
\(m_{ZnCl_2}=0,2.136=27,2\left(g\right)\)
c) \(C\%_{ZnCl_2}=\dfrac{27,2}{600+16,2}.100=4,41\%\)
Số mol của kẽm oxit
nZnO = \(\dfrac{m_{ZnO}}{M_{ZnO}}=\dfrac{16,2}{81}=0,2\left(mol\right)\)
Pt : 2HCl + ZnO → ZnCl2 + H2O\(|\)
2 1 1 1
0,4 0,2 0,2
a) Số mol của axit clohidric
nHCl = \(\dfrac{0,2.2}{1}=0,4\left(mol\right)\)
Khối lượng của axit clohidric
mHCl = nHCl . MHCl
= 0,4 . 36,5
= 14,6 (g)
Nồng độ phần trăm của dung dịch axit clohidric
C0/0HCl = \(\dfrac{m_{ct}.100}{m_{dd}}=\dfrac{14,6.100}{600}=2,43\)0/0
b) Số mol của muối kẽm clorua
nZnCl2 = \(\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
Khối lượng của muối kẽm clorua
mZnCl2 = nZnCl2 . MZnCl2
= 0,2 . 136
= 27,2 (g)
Khối lượng của dung dịch sau phản ứng
mdunh dịch sau phản ứng = mHCl + mZnO
= 600 + 16,2
= 616,2 (g)
Nồng độ phần trăm của muối kẽm clorua
C0/0ZnCl2 = \(\dfrac{m_{ct}.100}{m_{dd}}=\dfrac{27,2.100}{600}=4,53\)0/0
Chúc bạn học tốt

Đặt a,b là số mol Mg, R trong 8 gam A. Đặt x,y là hoá trị thấp cao của R
mA = 24a + bR = 8 (1)
Với HCl -> 2a + bx = 0,2 .2 (2)
Trong 9,6 gam A ( gấp 1,2 lần 8 gam A ) chứa 1,2a và 1,2b mol Mg, R
Với Cl2 -> 2 . 1,2a + 1,2by = 2 ( 30,9 - 9,6 ) / 71 (3)
Với 1 ≤ x ≤ y ≤ 3 -> Chọn x = 2; y = 3
(2)(3) -> a = b = 0,1
(1) -> R= 56 -> = Fe

Cho dung dịch HCl vào các mẫu thử
+ Tan, tạo thành dung dịch có màu xanh lục nhạt, có khí không màu, không mùi, nhẹ hơn không khí thoát ra : Fe
Fe + 2HCl → FeCl2 + H2
+ Tan, tạo thành dung dịch có màu hồng, có khí mùi sốc thoát ra : MnO2
4HCl + MnO2 ⟶ Cl2 + 2H2O + MnCl2
+ Tan, tạo dung dịch trong suốt, khí thoát ra có mùi hắc : Na2SO3
Na2SO3 + 2HCl → 2NaCl + SO2↑ + H2O
+ Tan, tạo thành dung dịch trong suốt, khí không màu thoát ra, nặng hơn không khí : KHCO3
KHCO3 + HCl → KCl + CO2 + H2O
+ Tan, tạo dung dịch màu xanh lục nhạt, khí thoát ra có mùi trứng thối: H2S
FeS + 2HCl → FeCl2 + H2S
+ Không tan : Na2SiO3
Trích mẫu thử:
- Cho dd HCl vào các mẫu thử.
+ Nếu tan, tạo thành dung dịch không màu ( trong suốt ) và có mùi hăng thì là: Na2SO3.
PT: Na2SO3 + 2HCl → 2NaCl + SO2\(\uparrow\) + H2O.
+ Nếu tan, tạo thành dd có màu xanh nước biển nhạt và có khí H2 thoát ra thì là: Fe.
PT: Fe + 2HCl → FeCl2 + H2.
+ Nếu tan, tạo thành dung dịch có màu hồng và có khí sộc vào mũi thì là: MnO2.
PT: MnO2 + 4HCl → MnCl2 + Cl2 + H2O.
+ nếu tan, tạo thành dd trong suốt và có khí CO2 thoát ra thì là: KHCO3.
PT: KHCO3 + HCl → KCl + CO2 + H2O.
+ Nếu tan, tạo thành dd màu xanh nước biển nhạt, có mùi thối thoát ra là: FeS.
PT: FeS + 2HCl → FeCl2 + H2S.
+ Nếu không tan là: Na2SiO3.

Khí thoát ra là H2
Ta có \(n_{H_2SO_4}=0,2a\)<\(n_{H_2}=0,4a\)
=> Sau phản ứng H2SO4 hết, Na còn dư nên tiếp tục phản ứng với nước trong dung dịch tạo H2 nên n H2 > n H2SO4
\(H_2SO_4+Na\rightarrow Na_2SO_4+H_2\)
\(Na+H_2O\rightarrow NaOH+\dfrac{1}{2}H_2\)
=> Dung dịch gồm : Na2SO4 và NaOH
Chất phản ứng là : HCl, Ba(OH)2, KHSO4, Al(OH)3, (NH4)2CO3, Ba(HCO3)2
NaOH + HCl → NaCl + H2O
Na2SO4 + Ba(OH)2 ⟶ 2NaOH + BaSO4
KHSO4 + 2NaOH → Na2SO4 + KOH + H2O
Al(OH)3 + NaOH ⟶ 2H2O + NaAlO2
(NH4)2CO3 + 2NaOH → Na2CO3 + 2NH3 + 2H2O
2NaOH + Ba(HCO3)2 → BaCO3 + Na2CO3 + 2H2O