
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a. \(n_{NaOH}=0,2mol;n_{FeCl_3}=0,2.0,6=0,12mol\)
\(3NaOH+FeCl_3->3NaCl+Fe\left(OH\right)_3\)
Lập tỷ lệ \(\dfrac{n_{NaOH}}{3}=\dfrac{0.2}{3}< \dfrac{n_{FeCl_3}}{1}=0,12\) => FeCl3 còn dư
\(n_{kếttủa}=n_{Fe\left(OH\right)_3}=\dfrac{1}{3}n_{NaOH}=\dfrac{0,2}{3}\left(mol\right)\)
\(m_{kt}=\dfrac{0.2}{3}.107=7,13g\)
b. \(V_{ddspu}=200+200=400\left(mL\right)\)

CTTQ của B: \(M_3PO_4\)
Theo đề có:
\(3M_M+31.1+16.4=164\)
=> \(M_M=23\left(Na\right)\), chọn C

Ở TN1 các phản ứng có thể xảy ra là:
\(K_2CO_3+2HCl->2KCl+H_2O+CO_2\)
\(CaCO_3+2HCl->CaCl_2+H_2O+CO_2\)
\(NaHCO_3+HCl->NaCl+H_2O+CO_2\)
\(Na_2CO_3+HCl->NaCl+H_2O+CO_2\)
TN2:
\(CaCO3-t^0->CaO+CO_2\)
\(2NaHCO_3-t^0->Na_2CO_3+H_2O+CO_2\)
\(CaSO_4-t^0->CaO+SO_3\)
TN3: Chất sau nung là Na2CO3
\(Na_2CO_3+2HCl->NaCl+H_2O+CO_2\)

Gọi CTTQ là \(C_2O_y\) (O hoá trị II, y là hoá trị của C)
\(\%m_O=\dfrac{16y}{12.2+16y}=\dfrac{72,72}{100}\)
=> y = 4, chọn D

Đề ra, ta có hợp chất X là \(Al\left(YO_3\right)_3\) và:
\(\%m_Y=\dfrac{3M_Y}{27+3\left(M_y+16.3\right)}=\dfrac{19.72}{100}\)
=> \(M_y=14\left(N\right)\), chọn C

ɑ) Cho 4 oxit Na2O, Fe2O3, CuO, Al2O3 vào HCl dư:
\(Na_2O+2HCl\rightarrow2NaCl+H_2O\)
\(Fe_2O_3+6HCl\rightarrow2FeCl_3+3H_2O\)
\(CuO+2HCl\rightarrow CuCl_2+H_2O\)
\(Al_2O_3+3HCl\rightarrow2AlCl_3+3H_2O\)
Cho hỗn hợp cả 4 oxit vào nước dư:
- Trước hết, Na2O tác dụng với nước tạo thành dd kiềm:
\(Na_2O+H_2O\rightarrow2NaOH\)
\(Fe_2O_3,CuO,Al_2O_3\) không tác dụng với nước.
- Nhưng, vì Al2O3 lưỡng tính nên có tác dụng với NaOH:
\(Al_2O_3+2NaOH\rightarrow2NaAlO_2+H_2O\)
b) Cho NaHCO3 vào dd Ba(OH)2 đến dư:
\(2NaHCO_3+Ba\left(OH\right)_2\rightarrow Na_2CO_3+BaCO_3+2H_2O\)
Nhỏ từ từ AlCl3 vào NaOH:
- Giai đoạn 1: Không xuất hiện kết tủa.
\(AlCl_3+4NaOH\rightarrow NaAlO_2+3NaCl+2H_2O\)
- Giai đoạn 2: Khi NaOH dần dần hết ⇒ thấy kết tủa trắng keo.
\(AlCl_3+3NaOH\rightarrow Al\left(OH\right)_3\downarrow+3NaCl\)
Kim loại A tác dụng với muối B tạo ra 2 chất khí ⇒ A là Na, B là (NH4)2CO3:
- Giai đoạn 1: \(2Na+2H_2O\rightarrow2NaOH+H_2\)
- Giai đoạn 2: \(2NaOH+\left(NH_4\right)_2CO_3\rightarrow Na_2CO_3+2NH_3+2H_2O\)
Cho HCl vào dd \(\left(NH_4\right)_2CO_3\):
\(\left(NH_4\right)_2CO_3+2HCl\rightarrow2HCl+H_2O+CO_2\)
CO2 làm cho nước vôi trong vẩn đục.

Có p + n + e = 52
Mà p = e => 2p + n = 52 (*)
Số hạt mang điện chiếm 32,69%, tức p + e chiếm 32,69%, hay 2p chiếm 32,69%
\(\dfrac{2p}{52}=\dfrac{32,69}{100}\)=> p = 9
Thay vào (*) => n = 34

PTHH:
\(M_2CO_3+2HCl\rightarrow2MCl+CO_2\uparrow+H_2O\) (1)
\(MHCO_3+HCl\rightarrow MCl+CO_2\uparrow+H_2O\) (2)
\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3\downarrow+H_2O\) (3)
\(CO_2+2NaOH\rightarrow Na_2CO_3+H_2O\) (4)
\(CO_2+Na_2CO_3+H_2O\rightarrow2NaHCO_3\) (5)
\(CO_2+CaCO_3+H_2O\rightarrow Ca\left(HCO_3\right)_2\) (6)
Giả sử kết tủa chưa bị hoà tan
Nếu chỉ có muối \(Na_2CO_3\xrightarrow[]{\text{BTNT Na}}n_{Na_2CO_3}=\dfrac{1}{2}n_{NaOH}=0,005\left(mol\right)\)
`=>` \(m_{Na_2CO_3}=0,005.106=0,53\left(g\right)\)
Nếu chỉ có muối \(NaHCO_3\xrightarrow[]{\text{BTNT Na}}n_{NaHCO_3}=n_{NaOH}=0,01\left(mol\right)\)
`=>` \(m_{NaHCO_3}=0,01.84=0,84\left(g\right)\)
Vậy \(0,53\le m_{muối}\le0,84< 2,46\left(g\right)\)
`=>` Chứng tỏ trong 2,46 gam muối có muối Ca(HCO3)2, kết tủa bị hoà tan một phần
`=>` \(m_{Ca\left(HCO_3\right)_2}=2,46-0,84=1,62\left(g\right)\)
`=>` \(n_{Ca\left(HCO_3\right)_2}=\dfrac{1,62}{162}=0,01\left(mol\right)\)
\(\xrightarrow[]{\text{BTNT Ca}}n_{CaCO_3}=n_{Ca\left(OH\right)_2}-n_{CaCO_3}=0,03\left(mol\right)\)
\(\xrightarrow[]{\text{BTNT C}}n_X=n_{CO_2}=n_{CaCO_3}+2n_{Ca\left(HCO_3\right)_2}+n_{NaHCO_3}=0,06\left(mol\right)\)
`=>` \(\overline{M_X}=\dfrac{5,08}{0,06}=\dfrac{254}{3}\left(g/mol\right)\)
`=>` \(M_{MHCO_3}< \dfrac{254}{3}< M_2CO_3\)
`=>` \(\left\{{}\begin{matrix}M_M< \dfrac{254}{3}-61=\dfrac{71}{3}\\M_M>\dfrac{\dfrac{254}{3}-60}{2}=\dfrac{37}{3}\end{matrix}\right.\)
`=>` \(\dfrac{37}{3}< M_M< \dfrac{71}{3}\)
Kết hợp với M có hoá trị I
`=> M` là `Na`
CTHH của 2 muối lần lượt là `Na_2CO_3, NaHCO_3`
Gọi \(\left\{{}\begin{matrix}n_{Na_2CO_3}=x\left(mol\right)\\n_{NaHCO_3}=y\left(mol\right)\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}106x+84y=5,08\\x+y=0,06\end{matrix}\right.\)
`<=>` \(\left\{{}\begin{matrix}x=\dfrac{1}{550}\left(mol\right)\\y=\dfrac{16}{275}\left(mol\right)\end{matrix}\right.\)
`=>` \(\left\{{}\begin{matrix}\%m_{Na_2CO_3}=\dfrac{106}{550}.100\%=19,27\%\\\%m_{NaHCO_3}=100\%-19,27\%=80,73\%\end{matrix}\right.\)

Ta có: \(\left\{{}\begin{matrix}n_{CO_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\\n_{H_2O}=\dfrac{0,8}{18}=\dfrac{2}{45}\left(mol\right)\end{matrix}\right.\)
`=>` \(\left\{{}\begin{matrix}n_C=0,4\left(mol\right)\\n_H=\dfrac{2.2}{45}=\dfrac{4}{45}\left(mol\right)\\n_O=\dfrac{5,6-\dfrac{4}{45}-0,4.12}{16}=\dfrac{2}{45}\left(mol\right)\end{matrix}\right.\)
Gọi CTTQ của A là \(C_xH_yO_z\)
`=>` \(x:y:z=0,4:\dfrac{4}{45}:\dfrac{2}{45}=9:2:1\)
`=>` A có dạng \(\left(C_9H_2O\right)_n\)
`=>` \(n=\dfrac{28}{126}=\dfrac{2}{9}\) (Đề sai)


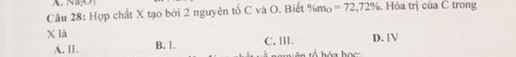


Bài 12:
- Hoà tan hỗn hợp vào nước dư, lọc tách thu được dd Na2CO3 và chất rắn A: Fe(OH)3, BaCO3
- Cho dd HCl dư vào dd Na2CO3, cô cạn dd thu được, đpnc thu được Na
\(Na_2CO_3+2HCl\rightarrow2NaCl+CO_2\uparrow+H_2O\)
\(2NaCl\xrightarrow[]{đpnc}2Na+Cl_2\uparrow\)
- Nung chất rắn A tới khối lượng không đổi, rồi hoà vào nước, lọc tách thu được dd Ba(OH)2 và Fe2O3
\(BaCO_3\xrightarrow[]{t^o}BaO+CO_2\uparrow\\ 2Fe\left(OH\right)_3\xrightarrow[]{t^o}Fe_2O_3+3H_2O\\ BaO+H_2O\rightarrow Ba\left(OH\right)_2\)
- Cho dd HCl dư vào dd Ba(OH)2, cô cạn dd thu được, đpnc thu được Ba
\(Ba\left(OH\right)_2+2HCl\rightarrow BaCl_2+2H_2O\\ BaCl_2\xrightarrow[]{đpnc}Ba+Cl_2\uparrow\)
11.
\(CaCO_3-t^0->CaO+CO_2\)
\(CaO+H_2O->Ca\left(OH\right)_2\)
\(Ca\left(OH\right)_2+NaHCO_3->CaCO_3+NaOH+H_2O\)
\(Ca\left(OH\right)_2+2NaHCO_3->CaCO_3+Na_2CO_3+H_2O\)