Giải thích sự khác biệt về góc liên kết trong phân tử NH3 Với góc 109,5 độ Trong phân tử methane
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Bạn tham khảo nhé
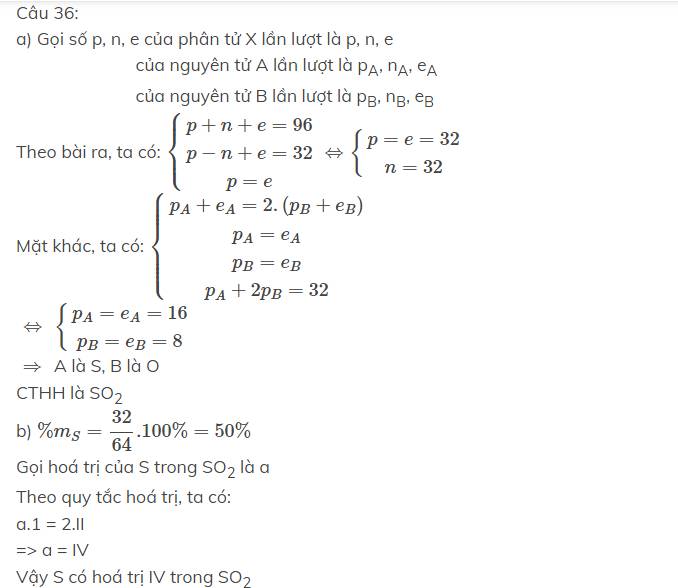
Bổ sung thêm phần a là số khối của S là 32, của O là 16
Chi tiết hơn tại: https://hoc24.vn/cau-hoi/.6765277239454

Gọi công thức oxit của phi kim X la \(X_aO_b\)
Ta có \(M_{X_ao_b}=22.M_{H_2}=22.2=44\)\((g/mol)\)
\(M_X.a+16.b=44\)
`@`TH1 : `a = 1 ; b = 2`
\(\rightarrow M_X+16.2=44\)
\(\rightarrow M_X=12\)\((g/mol)\)
Vậy X là nguyên tố Cacbon C
`@`TH2 : `a = 2 ; b = 1`
\(\rightarrow2.M_X+16=44\)
`->M_X = 14 ( g//mol)`
Vậy X là nguyên tố Nitơ ( N )

\(n_{CO_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
PTHH: \(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3\downarrow+H_2O\)
0,1<----------0,1
=> \(C_{M\left(Ca\left(OH\right)_2\right)}=\dfrac{0,1}{0,2}=0,5M\)
\(n_{CO_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
Tạo muối trung hòa → tạo muối \(CO\dfrac{2}{3}\)
Phương trình hóa học :
\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3+H_2O\)
Theo phương trình hóa học :
\(\rightarrow n_{CO_2}=n_{Ca\left(OH\right)_2}=0,1\left(mol\right)\)
Mà \(V_{Ca\left(OH\right)_2}=200\left(ml\right)=0,2\left(l\right)\)
\(CM_{Ca\left(OH\right)_2}=0,5\left(M\right)\)

Gọi số proton, notron và electron của nguyên tử đó lần lượt : p,n,e
\(\left\{{}\begin{matrix}p=e\\p+n+e=48\end{matrix}\right.\)
`<=> 2p + n = 48` `(1)`
Số hạt mang điện gấp đôi số hạt không mang.
`=>` \(\left\{{}\begin{matrix}2p+n=48\\2p-2n=0\left(2\right)\end{matrix}\right.\)
Từ `(1) , (2) => ` \(\left\{{}\begin{matrix}p=e=16\\n=16\end{matrix}\right.\)
`p = 16 ->` Nguyên tố là lưu huỳnh `(S)`
Theo đề, ta có hệ phương trình:
\(\left\{{}\begin{matrix}2Z+N=48\\2Z=2N\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}2Z+N=48\\Z-N=0\end{matrix}\right.\Leftrightarrow Z=N=16\)
=>Nguyên tử đó là của nguyên tốc lưu huỳnh
Kí hiệu: S

Hợp chất vô cơ : Dung dịch $FeCl_2$ làm mất màu dung dịch brom
$6FeCl_2 + 3Br_2 \to 4FeCl_3 + 2FeBr_3$
Hợp chất hữu cơ : Dung dịch $CH_2=CH-CH_2-COOH$,....
$CH_2=CH-CH_2-COOH + Br_2 \to CH_2Br-CHBr-CH_2-COOH$

Bài 26 :
$A : CaCO_3 ; A_1 : CaO ; B_1 : CO_2 ; X_1 : H_2O ; X_3 : NaOH ; A_2 : Ca(OH)_2 ; B_2 : NaHCO_3 ; X_2 : HCl ; X_4 : KOH ; A_3 : CaCl_2 $
$B_3 : Na_2CO_3$
$CaCO_3 \xrightarrow{t^o} CaO + CO_2$
$CO_2 + CaO \xrightarrow{t^o} CaCO_3$
$CaO + H_2O \to Ca(OH)_2$
$CO_2 + NaOH \to NaHCO_3$
$2NaHCO_3 + Ca(OH)_2 \to Na_2CO_3 + CaCO_3 + 2H_2O$
$Ca(OH)_2 + 2HCl \to CaCl_2 + 2H_2O$
$2NaHCO_3 + 2KOH \to Na_2CO_3 + K_2CO_3 + 2H_2O$
$CaCl_2 + Na_2CO_3 \to CaCO_3 + 2NaCl$
Bài 31 :
$X : Fe_2O_3 ; A : C ; B : CO ; C : H_2 ; E : Cl_2 ; F : FeCl_3 ; H : HCl ; K : O_2 $
$Fe_2O_3 + 3C \xrightarrow{t^o} 2Fe + 3CO$
$Fe_2O_3 + 3CO \xrightarrow{t^o} 2Fe + 3CO_2$
$Fe_2O_3 + 3H_2 \xrightarrow{t^o} 2Fe + 3H_2O$
$2Fe + 3Cl_2 \xrightarrow{t^o} 2FeCl_3$
$Fe + 2HCl \to FeCl_2 + H_2$
$2FeCl_2 + Cl_2 \to 2FeCl_3$
$4Fe + 3O_2 \xrightarrow{t^o} 2Fe_2O_3$
$Fe_2O_3 + 6HCl \to 2FeCl_3 + 3H_2O$
Bài 32 :
$A : S ; B : Na_2S ; C : NaHS ; E : CaS ; D : K_2S$
$(1) H_2S + \dfrac{1}{2}O_2 \xrightarrow{t^o} S + H_2O$
$(2)S + 2Na \xrightarrow{t^o} Na_2S$
$(3) Na_2S + H_2S \to 2NaHS$
$(4) 2NaHS + 2KOH \to Na_2S + K_2S + 2H_2O$
$(5) : K_2S + Ca(OH)_2 \to CaS + 2KOH$
$(6) : CaS + 2HCl \to CaCl_2 + H_2S$
$(7) : Na_2S + 2HCl \to 2NaCl + H_2S$
$(8) : NaHS + Ca(OH)_2 \to CaS + NaOH + H_2O$

Bài 18 :
$A : Cu(OH)_2 ; B : CuO ; C : Cu ; D: H_2SO_4 $
$Cu(OH)_2 + H_2SO_4 \to CuSO_4 + 2H_2O$
$CuO + H_2SO_4 \to CuSO_4 + H_2O$
$Cu + 2H_2SO_{4_{đặc}} \xrightarrow{t^o} CuSO_4 +S O_2 + 2H_2O$
$CuSO_4 + BaCl_2 \to CuCl_2 + BaSO_4$
$CuCl_2 + 2AgNO_3 \to Cu(NO_3)_2 + 2AgCl$
$Cu(NO_3)_2 + 2KOH \to Cu(OH)_2 + 2KNO_3$
$Cu(OH)_2 \xrightarrow{t^o} CuO + H_2O$
$CuO + H_2 \xrightarrow{t^o} Cu + H_2O$
Bài 19 :
$X : MnO_2 ; X_1 : Cl_2 ; X_2 : FeCl_3 ; X_3 : Fe(NO_3)_3 ; X_4 : Ba(NO_3)_2$
$Y : CuO ; Y_1 : CuCl_2 ; Y_2 : Cu(NO_3)_2 ; Y_3 : Cu ; Y_4 : CuSO_4 $
$M : BaSO_4$
$MnO_2 + 4HCl \to MnCl_2 + Cl_2 + 2H_2O$
$2Fe + 3Cl_2 \xrightarrow{t^o} 2FeCl_3$
$Cu + Cl_2 \xrightarrow{t^o} CuCl_2$
$FeCl_3 + 3AgNO_3 \to 3AgCl + Fe(NO_3)_3$
$2Fe(NO_3)_3 + 3Ba(OH)_2 \to 2Fe(OH)_3 + 3Ba(NO_3)_2$
$CuO + 2HCl \to CuCl_2 + H_2O$
$CuCl_2 + 2AgNO_3 \to 2AgCl + Cu(NO_3)_2$
$Fe + Cu(NO_3)_2 \to Fe(NO_3)_2 + Cu$
$Cu +2H_2SO_{4_{đặc}} \xrightarrow{t^o} CuSO_4 + SO_2 + 2H_2O$
$CuSO_4 + 2BaCl_2 \to BaSO_4 + CuCl_2$
$Ba(NO_3)_2 + H_2SO_4 \to BaSO_4 + 2HNO_3$

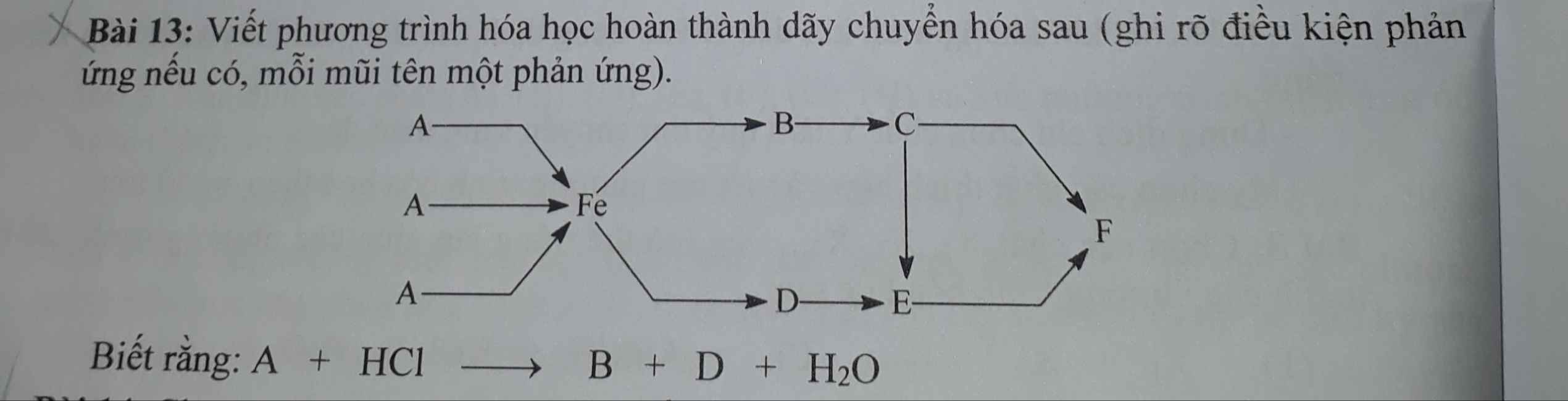
$A : Fe_3O_4 ; B : FeCl_2 ; D : FeCl_3 ; C : Fe(OH)_2 ; E : Fe(OH)_3 : F : Fe_2O_3$
$Fe_3O_4 + 4CO \xrightarrow{t^o} 3Fe + 4CO_2$
$Fe_3O_4 + 4C \xrightarrow{t^o} 3Fe + 4CO$
$Fe_3O_4 + 4H_2 \xrightarrow{t^o} 3Fe + 4H_2O$
$Fe + 2HCl \to FeCl_2 + H_2$
$2Fe + 3Cl_2 \xrightarrow{t^o} 2FeCl_3$
$FeCl_2 + 2KOH \to Fe(OH)_2 + 2KCl$
$FeCl_3 + 3KOH \to Fe(OH)_3 + 3KCl$
$4Fe(OH)_2 + O_2 + 2H_2O \to 4Fe(OH)_3$
$4Fe(OH)_2 + O_2 \xrightarrow{t^o} 2Fe_2O_3 + 4H_2O$
$2Fe(OH)_3 \xrightarrow{t^o} Fe_2O_3 + 3H_2O$





Nguyên tử \(N\) trong \(NH_3\) và \(C\) trong \(CH_4\) đều lai hóa \(sp^3\). Trong \(NH_3\),\(N\)
một cặp e chưa liên kết một \(AO\) lai hóa chứa cặp e , làm cho góc liên kết giảm đi so với góc tứ diện .Trong \(CH_4,C\) không có cặp e chưa liên kết nên góc liên kết bằng góc tứ diện
cảm ơn