Giúp em câu 8 với ạ 
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


PTHH: `CuO + H_2SO_4 -> CuSO_4 + H_2O`
Theo PT: `n_{H_2SO_4} = n_{CuSO_4} = n_{CuO} = 0,2 (mol)`
`=> m_{ddH_2SO_4} = (0,2.98)/(20\%) = 98 (g)`
`=> m_{dd} = 98 + 0,2.80 = 114 (g)`
`=>` \(\text{dd ban đầu có: }\left\{{}\begin{matrix}m_{CuSO_4}=0,2.160=32\left(g\right)\\m_{H_2O}=114-32=82\left(g\right)\end{matrix}\right.\)
Gọi \(n_{CuSO_4.5H_2O}=a\left(mol\right)\left(ĐK:a< 0\right)\)
`=>` \(\text{tách ra: }\left\{{}\begin{matrix}m_{CuSO_4}=160a\left(g\right)\\m_{H_2O}=5a.18=90a\left(g\right)\end{matrix}\right.\)
`=>` \(\text{dd còn lại: }\left\{{}\begin{matrix}m_{CuSO_4}=32-160a\left(g\right)\\m_{H_2O}=82-90a\left(g\right)\end{matrix}\right.\)
Ta có: \(S_{CuSO_4\left(10^oC\right)}=17,4\left(g\right)\)
`=>` \(\dfrac{32-160a}{82-90a}.100=17,4\)
`<=>` \(a=\dfrac{4433}{36085}\left(mol\right)\left(TM\right)\)
`=>` \(m_{CuSO_4.5H_2O}=\dfrac{4433}{36085}.250\approx30,71\left(g\right)\)

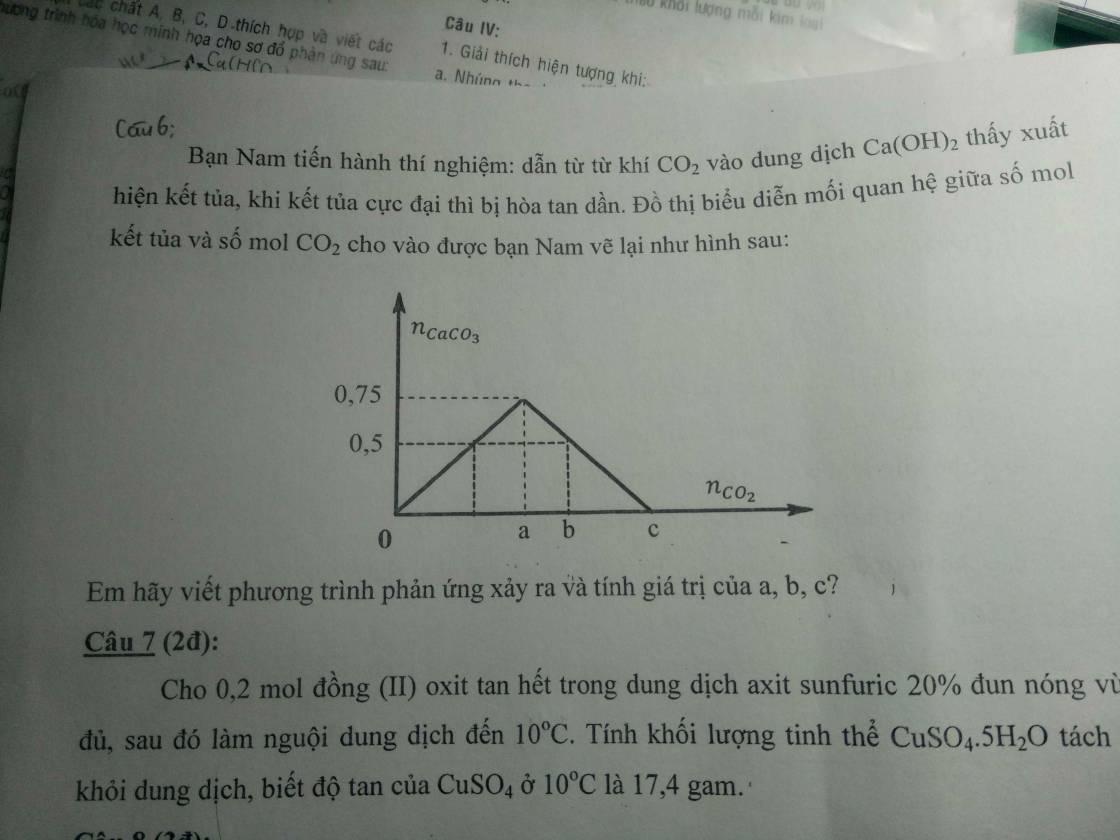
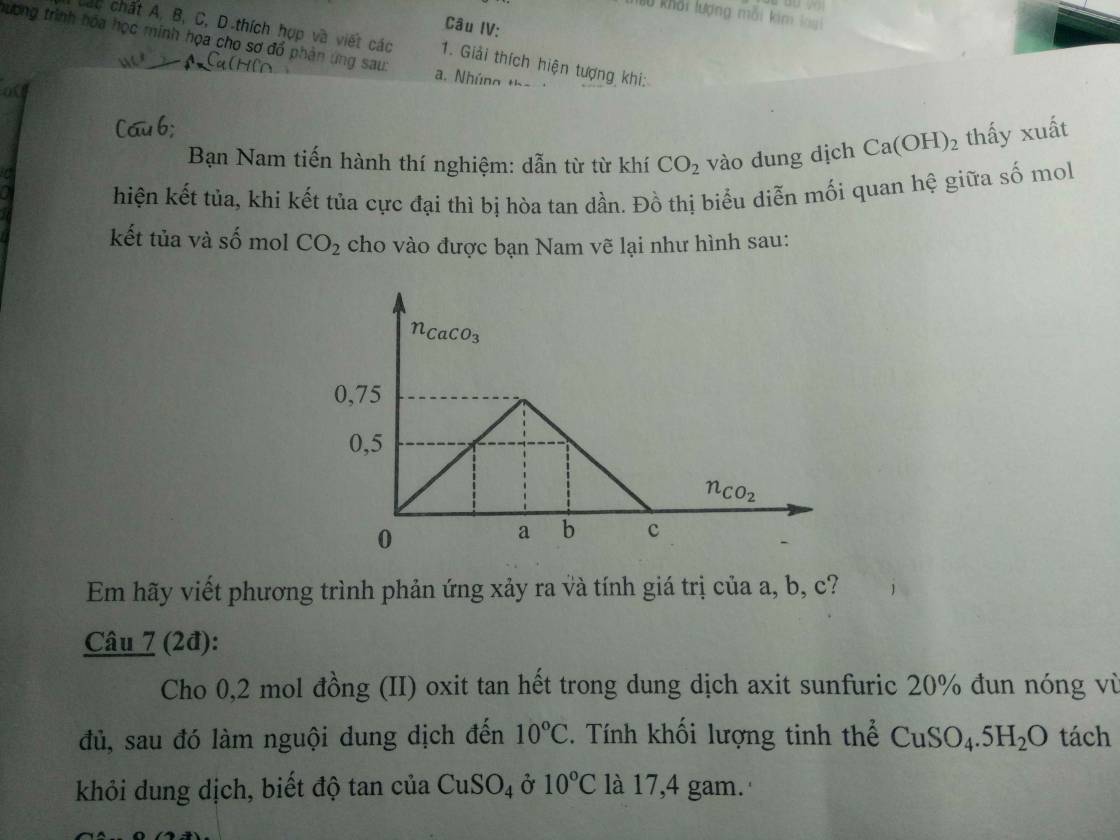
Tại lúc `n_{CO_2} = a (mol)`, kết tủa tăng lên đến cực đại là 0,75 mol
Tại lúc `n_{CO_2} = b (mol)`, kết tủa bị hòa tan một phần và còn lại 0,5 mol
Tại lúc `n_{CO_2} = c (mol)`, kết tủa bị hòa tan vừa hết
PTHH:
`Ca(OH)_2 + CO_2 -> CaCO_3 + H_2O`
`CaCO_3 + CO_2 + H_2O -> Ca(HCO_3)_2`
`-` Tại lúc `n_{CO_2} = a (mol)`
Theo PT: `a = n_{CO_2} = n_{Ca(OH)_2} = n_{CaCO_3} = 0,75 (mol)`
`-` Tại lúc `n_{CO_2} = b (mol)`
BTNT Ca: `n_{Ca(HCO_3)_2} = n_{Ca(OH)_2} - n_{CaCO_3} = 0,25 (mol)`
BTNT C: `b = n_{CO_2} = n_{CaCO_3} + 2n_{CO_2} = 1 (mol)`
`-` Tại lúc `n_{CO_2} = c (mol)`
BTNT Ca: `n_{Ca(HCO_3)_2} = n_{Ca(OH)_2} = 0,75 (mol)`
BTNT C: `c = n_{CO_2} = 2n_{Ca(HCO_3)_2} = 1,5 (mol)`

\(n_{H2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
Pt : \(Fe+2HCl\rightarrow FeCl_2+H_2|\)
0,15 0,3 0,15
a) \(m_{Fe}=0,15.56=8,4\left(g\right)\)
b) \(m_{HCl}=0,3.36,5=10,95\left(g\right)\)
⇒ \(C\%_{ddHCl}=\dfrac{10,95.100}{100}=10,95\%\)
Chúc bạn học tốt

Câu 2:
X: MnO2
X1: Cl2
X2: BaCl2
X3: FeCl3
M: BaSO4
Y: CuO
Y1: CuCl2
Y2: Cu(NO3)2
Y3: Cu
Y4: CuSO4
$(1)MnO_2 + 4HCl_{đặc} \xrightarrow{t^o} MnCl_2 + Cl_2 \uparrow + 2H_2O$
$(2)Cl_2 + Ba \xrightarrow{t^o} BaCl_2$
$(3) 3BaCl_2 + Fe_2(SO_4)_3 \rightarrow 3BaSO_4 \downarrow + 2FeCl_3$
$(4)2FeCl_3 + 3Ba(OH)_2 \rightarrow 2Fe(OH)_3 \downarrow + 3BaCl_2$
`(5) CuO + 2HCl -> CuCl_2 + H_2O`
$(6) CuCl_2 + 2AgNO_3 \rightarrow 2AgCl \downarrow + Cu(NO_3)_2$
$(7) Cu(NO_3)_2 + Fe \rightarrow Fe(NO_3)_2 + Cu \downarrow`
`(8) Cu + Fe_2(SO_4)_3 -> CuSO_4 + 2FeSO_4`
$(9) CuSO_4 + BaCl_2 \rightarrow BaSO_4 \downarrow + CuCl_2$


Câu 1: B
Câu 2: D
Câu 3: XO: X hóa trị II; \(YH_2\): Y hóa trị II \(\Rightarrow XY\Rightarrow\) A
Câu 4: Ta có: \(27\times2+16x=102\Leftrightarrow x=3\Rightarrow\) C
Câu 5: Ta có: \(31\times2+16x=142\Leftrightarrow x=5\Rightarrow\) D
Câu 6:
a. Ta có: \(56\times2+16x=160\Leftrightarrow x=3\Rightarrow\) C
b. C
Câu 7:
a. Ta có: \(31\times2+16x=142\Leftrightarrow x=5\Rightarrow\) C
b. D
Câu 8: X có hóa trị VI \(\Rightarrow\) \(XO_3\)
\(\%m_O=\dfrac{\left(16\times3\times100\right)}{M_X+16\times3}=100-40=60\Leftrightarrow M_X=32\Rightarrow\) X là S
\(\Rightarrow CTHH:SO_3\Rightarrow\) D

\(\circ\) Tạo \(Fe\left(OH\right)_3\):
PTPƯ: \(FeCl_3+3LiOH\rightarrow Fe\left(OH\right)_3\downarrow+3LiCl\)
PT ion RG: \(Fe^{3+}+3OH^-\rightarrow Fe\left(OH\right)_3\downarrow\)
\(\circ\) Tạo \(Cu\left(OH\right)_2\):
PTPƯ: \(CuSO_4+2NaOH\rightarrow Cu\left(OH\right)_2\downarrow+Na_2SO_4\)
PT ion RG: \(Cu^{2+}+2OH^-\rightarrow Cu\left(OH\right)_2\downarrow\)
\(\circ\) Tạo \(Mg\left(OH\right)_2\):
PTPƯ: \(MgCl_2+Ca\left(OH\right)_2\rightarrow Mg\left(OH\right)_2\downarrow+CaCl_2\)
PT ion RG: \(Mg^{2+}+2OH^-\rightarrow Mg\left(OH\right)_2\downarrow\)



Gọi \(\left\{{}\begin{matrix}n_{Fe_3O_4}=a\left(mol\right)\\n_{Al}=b\left(mol\right)\end{matrix}\right.\Rightarrow232a+27b=93,9\left(1\right)\)
Vì chất rắn B sau phản ứng + dd NaOH -> H2 => Al dư
B gồm: Al, Al2O3, Fe
\(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
PTHH: \(3Fe_3O_4+8Al\xrightarrow[]{t^o}9Fe+4Al_2O_3\)
a-------->\(\dfrac{8}{3}a\)----->3------>\(\dfrac{4}{3}a\)
\(Al_2O_3+2NaOH\rightarrow2NaAlO_2+H_2O\)
\(2NaOH+2Al+2H_2O\rightarrow2NaAlO_2+3H_2\)
0,1<-------0,1<----------------0,1<----------0,15
`=>` \(b-\dfrac{8}{3}a=0,1\left(2\right)\)
Từ `(1), (2) =>` \(\left\{{}\begin{matrix}a=0,3\left(mol\right)\\b=0,9\left(mol\right)\end{matrix}\right.\)
`=>` \(\left\{{}\begin{matrix}m_{Fe_3O_4}=0,3.232=69,6\left(g\right)\\m_{Al}=0,9.27=24,3\left(g\right)\end{matrix}\right.\)
Theo PT: \(n_{NaAlO_2}=n_{NaOH}=0,45.2=0,9\left(mol\right)\)
b) \(n_{Al\left(OH\right)_3}=\dfrac{62,4}{78}=0,8\left(mol\right)\)
PTHH: \(NaAlO_2+HCl+H_2O\rightarrow Al\left(OH\right)_3\downarrow+NaCl\)
`-` TH1: Kết tủa chưa bị hòa tan
Theo PT: \(n_{HCl}=n_{Al\left(OH\right)_3}=0,8\left(mol\right)\)
`=>` \(V=\dfrac{0,8}{2}=0,4\left(l\right)=400\left(ml\right)\)
`-` TH2: Kết tủa tan ra 1 phần
PTHH: \(Al\left(OH\right)_3+3HCl\rightarrow AlCl_3+3H_2O\)
BTNT Na: `n_{NaCl} = n_{NaAlO_2} = 0,9 (mol)`
BTNT Al: `n_{AlCl_3} = n_{NaAlO_2} - n_{Al(OH)_3} = 0,1 (mol)`
BTNT Cl: `n_{HCl} = n_{NaCl} + 3n_{AlCl_3} = 1,2 (mol)`
`=>` \(V=\dfrac{1,2}{2}=0,6\left(l\right)=600\left(ml\right)\)