Khử 6,4g một oxide kim loại cần 2,688 lít H2. Lấy kim loại sinh ra cho tác dụng với dd HCl thì tạo 1,792 lít H2. Xác định tên kim loại.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{HCl}=\dfrac{250.18,25\%}{100\%}:36,5=1,25\left(mol\right)\)
\(n_{H_2}=\dfrac{8,4}{22,4}=0,375\left(mol\right)\)
Gọi \(\left\{{}\begin{matrix}n_A=x\left(mol\right)\\n_B=x\left(mol\right)\end{matrix}\right.\) (theo đề)
\(A+2HCl\rightarrow ACl_2+H_2\)
x---->2x---------------->x
\(2B+6HCl\rightarrow2BCl_3+3H_2\)
x----->3x------------------->1,5x
Theo PTHH có: \(n_{H_2}=\dfrac{1}{2}n_{HCl}=\dfrac{1}{2}.1,25=0,625\left(mol\right)>n_{H_2.thoát.ra.theo.đề}\)
\(\Rightarrow HCl.dư\\ \Rightarrow n_{H_2}=x+1,5x=0,375\\ \Rightarrow x=0,15\)
Có: \(m_{hh.kim.loại}=m_A+m_B=Ax+Bx=x\left(A+B\right)=7,65\) (g)
\(\Rightarrow A+B=\dfrac{7,65}{0,15}=51\left(g/mol\right)\)
Mà A là kim loại hóa trị II, B là kim loại hóa trị III.
\(\Rightarrow\left\{{}\begin{matrix}A=24\left(Mg\right)\\B=27\left(Al\right)\end{matrix}\right.\)

\(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
a
Gọi \(\left\{{}\begin{matrix}n_K=x\left(mol\right)\\n_{Na}=y\left(mol\right)\end{matrix}\right.\)
\(K+H_2O\rightarrow KOH+\dfrac{1}{2}H_2\)
x -------------->x------->0,5x
\(Na+H_2O\rightarrow NaOH+\dfrac{1}{2}H_2\)
y---------------->y---------->0,5y
Có: \(n_{H_2}=0,5x+0,5y=0,1\left(mol\right)\) (1)
\(KOH+HCl\rightarrow KCl+H_2O\)
x--------->x------->x
\(NaOH+HCl\rightarrow NaCl+H_2O\)
y---------->y--------->y
Có: \(m_{hh.muối}=74,5x+58,5y=13,3\left(g\right)\left(2\right)\)
Từ (1), (2) có hệ phương trình: \(\left\{{}\begin{matrix}0,5x+0,5y=0,1\\74,5x+58,5y=13,3\end{matrix}\right.\)
\(\Leftrightarrow\left\{{}\begin{matrix}x=0,1\\y=0,1\end{matrix}\right.\) (bấm máy giải hệ)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Na}=\dfrac{23.0,1.100\%}{23.0,1+39.0,1}=37,1\%\\\%m_K=\dfrac{39.0,1.100\%}{23.0,1+39.0,1}=62,9\%\end{matrix}\right.\)
b
\(n_{HCl}=x+y=0,1+0,1=0,2\left(mol\right)\\ V_{HCl}=\dfrac{n}{CM}=\dfrac{0,2}{0,5}=0,4\left(l\right)\)
c
\(2H_2+O_2\underrightarrow{t^o}2H_2O\)
0,1-->0,05
\(V_{O_2}=0,05.22,4=1,12\left(l\right)\)

a
Gọi \(\left\{{}\begin{matrix}kim.loại.hóa.trị.II:A\\kim.loại.hóa.trị.III:B\end{matrix}\right.\)
\(n_{HCl}=0,17.2=0,34\left(mol\right)\)
\(A+2HCl\rightarrow ACl_2+H_2\)
x ---->2x
\(2B+6HCl\rightarrow2BCl_3+3H_2\)
5x---->15x
Theo PTHH có: \(n_{H_2}=\dfrac{1}{2}n_{HCl}=\dfrac{1}{2}.0,34=0,17\left(mol\right)\)
Theo định luật bảo toàn khối lượng có:
\(m_{muối}=m_{hh.kim.loại}+m_{HCl}-m_{H_2}=4+0,34.36,5-0,17.2=16,07\left(g\right)\)
b
\(V_{H_2}=0,17.22,4=3,808\left(l\right)\)
c
Theo đề gọi \(\left\{{}\begin{matrix}n_B=n_{Al}=5x\left(mol\right)\\n_A=x\left(mol\right)\end{matrix}\right.\)
Có: \(n_{HCl}=2x+15x=0,34\Rightarrow x=0,02\)
\(m_{hh}=m_{Al}+m_A=27.5x+Ax=4\) (g)
\(\Leftrightarrow27.5.0,02+A.0,02=4\\ \Rightarrow A=65\)
Vậy tên kim loại hóa trị II là Zn (kẽm).

`-` Cốc `A:`
`n_{Fe} = (16,8)/(56) = 0,3(mol)`
`PTHH: Fe + 2HCl -> FeCl_2 + H_2`
Theo PT: `n_{H_2} = n_{Fe} = 0,3(mol)`
`-> m_{tăng} = 16,8 - 0,3.2 = 16,2(g)(1)`
`-` Cốc `B:`
`n_{Al} = m/(27) (mol)`
`PTHH: 2Al + 6HCl -> 2AlCl_3 + 3H_2`
Theo PT: `n_{H_2} = 3/2 n_{Al} = 3/2 . m/(27) = m/(18) (mol)`
`-> m_{tăng} = m - 2 . m/(18) = (8m)/9 (g)`
`-> (8m)/9 = 16,2`
`<=> m = 18,225(g)`

Gọi tên kim loại cần tìm là R (n là hóa trị của R, m là hóa trị cao nhất của R với \(m\ge n\))
\(2R+mCl_2\underrightarrow{t^o}2RCl_m\)
4,8 19
Có: \(19.2R=4,8.\left(2R+71m\right)\)
\(\Leftrightarrow38R-9,6R-340,8m=0\\ \Leftrightarrow28,4R=340,8m\\ \Leftrightarrow R=\dfrac{340,8m}{28,4}=12m\)
Với \(m=1\Rightarrow R=12\) (loại)
`m=2` `\Rightarrow R=24` (nhận)
`m=2` `\Rightarrow R=36` (loại)
Vậy kim loại cần tìm là Mg.

`1)`
`n_{H_2} = (10,08)/(22,4) = 0,45(mol)`
`n_{HCl} = 0,5.2 = 1(mol)`
`PTHH:`
`2Al + 6HCl -> 2AlCl_3 + 3H_2`
`Mg + 2HCl -> MgCl_2 + H_2`
Theo PT: `n_{HCl} = 2n_{H_2} = 0,9(mol) < 1(mol)`
`-> HCl` dư, kim loại tan hết
Theo PT:
`n_{AlCl_3} = n_{Al} = a(mol)`
`n_{MgCl_2} = n_{Mg} = b(mol)`
`-> 133,5a + 95b = 40,95(1)`
`n_{H_2} = 3/2 n_{Al} + n_{Mg}`
`-> 1,5a + b = 0,45(2)`
`(1),(2)->a=0,2;b=0,15`
`-> x = 0,2.27+0,15.24=9(g)`
`2)`
`n_{HCl(dư)} = 1 - 0,9 = 0,1(mol)`
`C_{M(HCl)} = (0,1)/(0,5) = 0,2M`
`C_{M(AlCl_3)} = (0,2)/(0,5) = 0,4M`
`C_{M(MgCl_2)} = (0,15)/(0,5) = 0,3M`

sửa đề
Cho Mg tác dụng với 100(g) dung dịch HCL 7,3% vừa đủ. Tính khối lượng Mg và thể tích H2 và khối lượng MgCL2?
giải
\(n_{HCl}=\dfrac{100.7,3}{100}:36,5=0,2\left(mol\right)\\ Mg+2HCl\xrightarrow[]{}MgCl_2+H_2\\ n_{Mg}=n_{H_2}=n_{MgCl_2}=0,2mol\\ m_{Mg}=0,2.24=4,8\left(g\right)\\ V_{H_2}=0,2.22,4=4,48\left(l\right)\\ m_{MgCl_2}=0,2.95=19\left(g\right)\)

\(n_{Al}=\dfrac{0,54}{27}=0,02mol\\ n_{H_2SO_4}=0,07.0,5=0,035mol\\ 2Al+3H_2SO_4->Al_2\left(SO_4\right)_3+3H_2\\ \Rightarrow H_2SO_4:dư\\ V=\dfrac{3}{2}.0,02.22,4=0,672L\\ C_{M\left(H_2SO_4\right)}=\dfrac{0,005}{0,07}=0,071M\\ C_{M\left(Al_2\left(SO_4\right)_3\right)}=\dfrac{0,01}{0,07}=\dfrac{1}{7}\left(M\right)\\ CuO+H_2-t^{^0}->Cu+H_2O\\ n_{H_2}=0,03mol\\ n_{CuO}=\dfrac{6,4}{80}=0,08\Rightarrow CuO:dư\\ m_{rắn}=6,4-16.0,03=5,92g\)



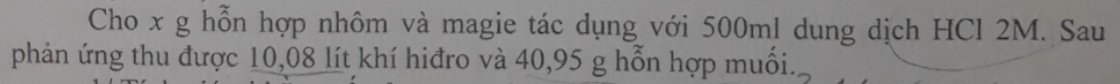

Gọi tên kim loại cần tìm là R.
Khử 6,4 (g) \(R_xO_y\) cần \(n_{H_2}=\dfrac{2,688}{22,4}=0,12\left(mol\right)\)
\(R_xO_y+yH_2\underrightarrow{t^o}xR+yH_2O\) (1)
\(\dfrac{0,12}{y}\)<-0,12->\(\dfrac{0,12x}{y}\)->0,12
\(xR+2yHCl\rightarrow xRCl_{\dfrac{2y}{x}}+yH_2\left(2\right)\)
\(\dfrac{0,08x}{y}\)<------------------------0,08
\(n_{H_2\left(2\right)}=\dfrac{1,792}{22,4}=0,08\left(mol\right)\)
Từ (1), (2) có: \(\dfrac{0,12x}{y}=\dfrac{0,08x}{y}\)
\(\Leftrightarrow\dfrac{x}{y}=\dfrac{0,08x}{y}:0,12=\dfrac{0,08x}{0,12y}=\dfrac{2x}{3y}\)
\(\Rightarrow x=2;y=3\)
\(\Rightarrow\dfrac{6,4}{R_2O_3}=\dfrac{0,12}{y}\\ \Leftrightarrow\dfrac{6,4}{\left(2R+48\right)}=\dfrac{0,12}{3}\)
\(\Rightarrow R=56\)
Vậy tên kim loại là Fe (sắt).