Cho 13g Zn tác dụng dung dịch HCL có chứa 14,6g. hãy tính thể tích khí H2 sinh ra ở đktc
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



a) Na2O + H2O --> 2NaOH
b) \(n_{Na_2O}=\dfrac{6,2}{62}=0,1\left(mol\right)\)
PTHH: Na2O + H2O --> 2NaOH
0,1------------->0,2
=> mNaOH = 0,2.40 = 8 (g)

a)
2K + 2H2O --> 2KOH + H2
Ba + 2H2O --> Ba(OH)2 + H2
b)
Gọi số mol K, Ba là a, b (mol)
=> 39a + 137b = 17,6 (1)
\(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
PTHH: 2K + 2H2O --> 2KOH + H2
a--------------------->0,5a
Ba + 2H2O --> Ba(OH)2 + H2
b------------------------->b
=> 0,5a + b = 0,15 (2)
(1)(2) => a = 0,1 (mol); b = 0,1 (mol)
\(\left\{{}\begin{matrix}\%m_K=\dfrac{0,1.39}{17,6}.100\%=22,159\%\\\%m_{Ba}=\dfrac{0,1.137}{17,6}.100\%=77,841\%\end{matrix}\right.\)
c) dd sau pư là dd bazo nên làm quỳ tím chuyển màu xanh
d)
PTHH: Fe2O3 + 3H2 --to--> 2Fe + 3H2O
0,05<--0,15
=> mFe2O3 = 0,05.160 = 8 (g)

a)
- Dẫn các khí qua ống nghiệm đựng bột CuO nung nóng:
+ Không hiện tượng: O2, CO2, không khí (1)
+ Chất rắn màu đen dần chuyển sang màu đỏ, xuất hiện hơi nước: H2
CuO + H2 --to--> Cu + H2O
- Cho que đóm còn tàn đỏ vào các lọ đựng khí ở (1)
+ Que đóm bùng cháy: O2
+ Que đóm tắt: CO2
+ Que đóm cháy như ban đầu: không khí
b)
- Cho giấy quỳ tím tác dụng với các dd
+ QT chuyển đỏ: HCl
+ QT chuyển xanh: Ca(OH)2
+ QT không chuyển màu: BaCl2
c)
- Hòa tan các chất rắn vào nước có pha sẵn quỳ tím:
+ Chất rắn tan, có khí thoát ra, dd chuyển màu xanh: Na
2Na + 2H2O --> 2NaOH + H2
+ Chất rắn tan, không có khí, dd chuyển màu xanh: Na2O
Na2O + H2O --> 2NaOH
+ Chất rắn tan, không có khí, dd chuyển màu đỏ: P2O5
P2O5 + 3H2O --> 2H3PO4
d)
- Hòa tan các chất rắn vào nước có pha sẵn quỳ tím:
+ Chất rắn tan, có khí thoát ra, dd chuyển màu xanh: K
2K + 2H2O --> 2KOH + H2
+ Chất rắn tan, không có khí, dd chuyển màu xanh: K2O
K2O + H2O --> 2KOH
+ Chất rắn tan, không có khí, dd chuyển màu đỏ: P2O5
P2O5 + 3H2O --> 2H3PO4
+ Chất rắn tan, không có khí, dd trong suốt: KCl
e)
- Hòa tan các chất rắn vào nước có pha sẵn quỳ tím:
+ Chất rắn tan, dd chuyển màu xanh: BaO
BaO + H2O --> Ba(OH)2
+ Chất rắn tan, dd chuyển màu đỏ: P2O5
P2O5 + 3H2O --> 2H3PO4
+ Chất rắn tan, dd trong suốt: NaCl
+ Chất rắn không tan: MgO

\(n_{Al}=\dfrac{5,4}{27}=0,2\left(mol\right)\)
\(n_{H_2SO_4}=\dfrac{49}{98}=0,5\left(mol\right)\)
PTHH: 2Al + 3H2SO4 --> Al2(SO4)3 + 3H2
Xét tỉ lệ: \(\dfrac{0,2}{2}< \dfrac{0,5}{3}\) => Al hết, H2SO4 dư
PTHH: 2Al + 3H2SO4 --> Al2(SO4)3 + 3H2
0,2---------------------------->0,3
=> VH2 = 0,3.22,4 = 6,72 (l)
\(n_{Al}=\dfrac{m}{M}=\dfrac{5,4}{27}=0,2=\left(mol\right)\)
\(n_{H_2SO_4}=\dfrac{m}{M}=\dfrac{49}{98}=0,5\left(mol\right)\)
2Al + 3H2SO4 → Al2(SO4)3 + 3H2
2 3 ( mol )
0,2 0,5 ( mol )
Tỉ lệ: \(\dfrac{0,2}{2}< \dfrac{0,5}{3}\) ⇒ H2SO4 dư
2Al + 3H2SO4 → Al2(SO4)3 + 3H2
0,2 → 0,3 → 0,3 ( mol )\(V_{H_2}=n.22,4=0,3.22,4=6,72\left(l\right)\)
\(n_{Zn}=\dfrac{8,125}{65}=0,125mol\)
\(n_{HCl}=\dfrac{18,25}{36,5}=0,5mol\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
Xét: \(\dfrac{0,125}{1}\) < \(\dfrac{0,5}{2}\) ( mol )
0,125 0,125 ( mol )
\(V_{H_2}=0,125.22,4=2,8l\)

a) Gọi số mol Ca, CaCO3 là a, b (mol)
=> 40a + 100b = 19 (1)
\(m_{HCl}=\dfrac{500.4,38}{100}=21,9\left(g\right)\)
PTHH: Ca + 2HCl --> CaCl2 + H2
a--->2a------->a----->a
CaCO3 + 2HCl --> CaCl2 + CO2 + H2O
b------>2b------>b------>b
=> \(\overline{M}_Y=\dfrac{2a+44b}{a+b}=13,6.2=27,2\left(g/mol\right)\)
=> 25,2a = 16,8b (2)
(1)(2) => a = 0,1 (mol); b = 0,15 (mol)
\(\left\{{}\begin{matrix}m_{Ca}=0,1.40=4\left(g\right)\\m_{CaCO_3}=0,15.100=15\left(g\right)\end{matrix}\right.\)
b)
mdd sau pư = 19 + 500 - 0,1.2 - 0,15.44 = 512,2 (g)
mHCl(dư) = 21,9 - 36,5(2a + 2b) = 3,65 (g)
mCaCl2 = 111(a + b) = 27,75 (g)
\(\left\{{}\begin{matrix}C\%_{CaCl_2}=\dfrac{27,75}{512,2}.100\%=5,418\%\\C\%_{HCl\left(dư\right)}=\dfrac{3,65}{512,2}.100\%=0,713\%\end{matrix}\right.\)

| CTHH | Phân loại | Gọi tên |
| Al2O3 | Oxit | Nhôm oxit |
| SO3 | Oxit | lưu huỳnh trioxit |
| CO2 | Oxit | cacbon đioxit |
| CuO | Oxit | đồng (II) oxit |
| H2SO4 | Axit | axit sunfuric |
| KOH | Bazơ | kali hiđroxit |
| Ba(OH)2 | Bazơ | bari hiđroxit |
| ZnSO4 | Muối | kẽm sunfat |
| Na2SO4 | Muối | natri sunfat |
| NaHCO3 | Muối | natri hiđrocacbonat |
| K2HPO4 | Muối | kali hiđrophotphat |
| Ca(HSO4)2 | Muối | canxi hiđrosunfat |
| H3PO4 | Axit | Axit photphoric |
| CaCl2 | Muối | canxi clorua |
| CTHH | Gọi tên | Phân loại |
| Al2O3 | Nhôm oxit | oxit lưỡng tính |
| SO3 | Lưu huỳnh trioxit | oxit axit |
| CO2 | Cacbon đioxit | oxit axit |
| CuO | Đồng (II) oxit | oxit bazơ |
| H2SO4 | axit sunfuric | axit |
| KOH | Kali hiđroxit | bazơ tan |
| Ba(OH)2 | Bari hiđroxit | bazơ tan |
| ZnSO4 | Kẽm sunfat | muối trung hòa |
| Na2SO4 | Natri sunfat | muối trung hòa |
| NaHCO3 | Natri hiđrocacbonat | muối axit |
| K2HPO4 | Kali hiđrophotphat | muối axit |
| Ca(HSO4)2 | Canxi hiđrosunfat | muối axit |
| H3PO4 | axit photphoric | axit |
| CaCl2 | Canxi clorua | muối trung hòa |



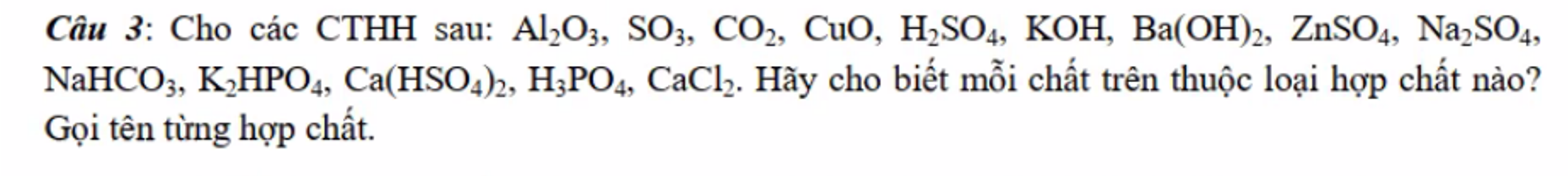
\(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\); \(n_{HCl}=\dfrac{14,6}{36,5}=0,4\left(mol\right)\)
PTHH: Zn + 2HCl --> ZnCl2 + H2
Xét tỉ lệ: \(\dfrac{0,2}{1}=\dfrac{0,4}{2}\) => pư vừa đủ
PTHH: Zn + 2HCl --> ZnCl2 + H2
0,2----------------->0,2
=> VH2 = 0,2.22,4 = 4,48 (l)
nZn=13/65=0,2mol
nHCl=14,6/36,5=0,4mol
Zn+2HCl→ZnCl2+H2
Xét: 0,2 < 0,4 ( mol )
0,4 0,4 ( mol )
VH2=0,4.22,4=8,96