So sánh nhiệt độ sôi và khả năng hòa tan trong nước giữa NH3 và CH4. Giải thích.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Do H2O có liên kết Hidro còn H2S không có nên nhiệt độ sôi của H2O cao hơn H2S.

Liên kết hydrogen < Liên kết cộng hóa trị < Liên kết ion

Liên kết hydrogen là một loại liên kết yếu, được hình thành giữa nguyên tử H (đã liên kết với một nguyên tử có độ âm điện lớn, thường là F, O, N) với một nguyên tử khác có độ âm điện lớn (thường là F, O, N) còn cặp electron hóa trị chưa tham gia liên kết

Nguyên tử bị thiếu bao nhiêu electron thì bỏ ra bấy nhiêu electron để góp chung electron với các nguyên tử khác => Đạt cấu hình eleectron bền vững của khí hiếm
Ví dụ:
- Nguyên tử O cần nhận thêm 2 electron => Bỏ ra 2 electron để góp chung
- Nguyên tử Cl và H cần nhận thêm 1 electron => Mỗi nguyên tử bỏ ra 1 electron để góp chung
- Nguyên tử N cần nhận thêm 3 electron => Bỏ ra 3 electron để góp chung

Liên kết mà các nguyên tử sử dụng chung các electron hóa trị để cùng thỏa mãn quy tắc octet được gọi là liên kết cộng hóa trị

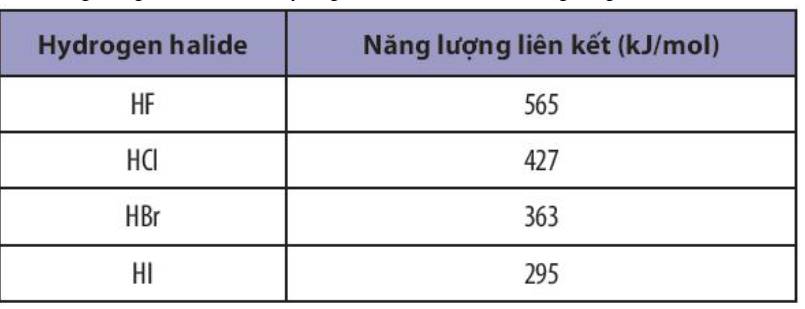
- Sắp xếp theo chiều tăng dần giá trị năng lượng liên kết: HI < HBr < HCl < HF
=> Sắp xếp theo chiều tăng dần độ bền liên kết: HI < HBr < HCl < HF

- Liên kết σ là sự xen phủ trục
- Liên kết п là sự xen phủ bên

Để giải thích sự hình thành liên kết Cl−Cl, có thể dựa vào cấu hình electron của mỗi nguyên tử clo:
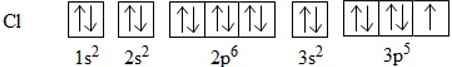
Sự hình thành liên kết giữa hai nguyên tử chlorine là do sự xen phủ giữa hai obitan p chứa electron độc thân của mỗi nguyên tử chlorine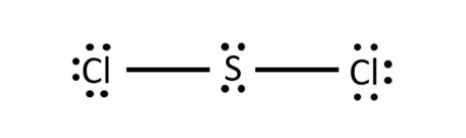
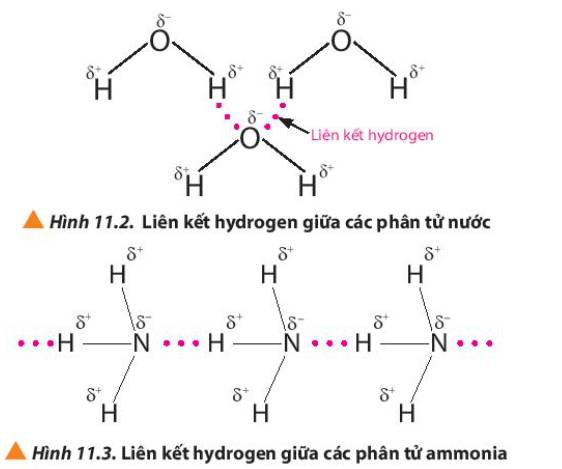

- Phân tử NH3 có khả năng liên kết hydrogen liên phân tử do N có độ âm điện cao
- Phân tử CH4 không có khả năng liên kết hydrogen liên phân tử do C có độ âm điện thấp
=> Phân tử NH3 có nhiệt độ sôi cao hơn và khả năng hòa tan trong nước tốt hơn soi với CH4