Báo cáo học liệu
Mua học liệu
Mua học liệu:
-
Số dư ví của bạn: 0 coin - 0 Xu
-
Nếu mua học liệu này bạn sẽ bị trừ: 2 coin\Xu
Để nhận Coin\Xu, bạn có thể:

Tách kim loại và việc sử dụng hợp kim SVIP
I. Phương pháp tách kim loại
- Trong tự nhiên, kim loại chủ yếu tồn tại ở trong quặng dưới dạng hợp chất như oxide, muối.
- Quy trình tách kim loại từ quặng:
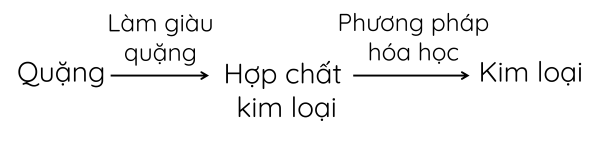
- Các phương pháp hóa học để tách kim loại:
- Điện phân nóng chảy (kim loại hoạt động hóa học mạnh).
- Nhiệt luyện (kim loại hoạt động hóa học trung bình).
- Thủy nhiệt (kim loại hoạt động hóa học yếu).
II. Quá trình tách một số kim loại có nhiều ứng dụng
1. Tách nhôm ra khỏi aluminium oxide bằng phản ứng điện phân
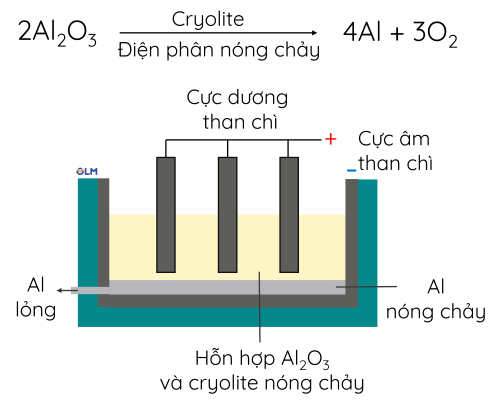
2. Tách sắt ra khỏi iron(III) oxide
Ở nhiệt độ cao, sắt được tách ra khỏi iron(III) oxide bởi carbon monoxide.
Fe2O3 + 3CO \(\underrightarrow{t^o}\) 2Fe + 3CO2
3. Tách kẽm ra khỏi zinc sulfide
- Đốt quặng zinc sulfide trong không khí:
2ZnS + 3O2 \(\underrightarrow{t^o}\) 2ZnO + 2SO2
- Tách kẽm ra khỏi zinc oxide:
ZnO + C \(\underrightarrow{t^o}\) Zn + CO
III. Hợp kim
1. Khái niệm hợp kim
Hợp kim là vật liệu kim loại có chứa ít nhất một kim loại cơ bản và một số kim loại hoặc phi kim khác (kim loại cơ bản chiếm thành phần chính).
2. Ưu điểm của hợp kim
Hợp kim có ưu điểm vượt trội hơn kim loại về độ cứng, độ bền, khả năng chống ăn mòn, gỉ sét,...
3. Một số hợp kim phổ biến
- Gang và thép (hợp kim Fe và C) có ưu điểm về độ cứng, độ đàn hồi, khả năng chịu lực so với kim loại sắt.
- Inox (hợp kim Fe, C, Cr và Ni) có ưu điểm là cứng và khó bị gỉ.
- Đuy-ra (hợp kim Al, Cu, Mn, Mg,...) có ưu điểm là nhẹ nhưng bền và cứng hơn so với nhôm.
IV. Sản xuất gang và thép
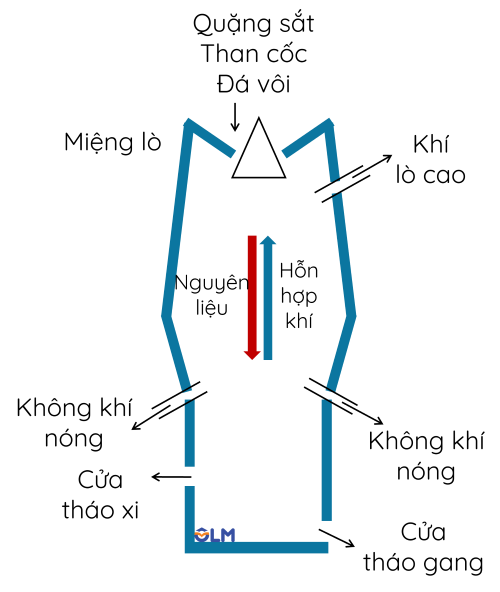
1. Sản xuất gang từ nguồn quặng chứa iron(III) oxide
Nguyên liệu: Quặng sắt, than cốc, chất tạo xỉ.
Các giai đoạn sản xuất gang:
- Phản ứng tạo thành CO:
C + O2 \(\underrightarrow{t^o}\) CO2
C + CO2 \(\underrightarrow{t^o}\) 2CO
- Khí CO phản ứng với oxide sắt:
3CO + Fe2O3 \(\underrightarrow{t^o}\) 2Fe + 3CO2
- Đá vôi phân hủy thành CaO, CaO kết hợp với SiO2 tạo thành xỉ:
CaO + SiO2 \(\underrightarrow{t^o}\) CaSiO3
2. Sản xuất thép
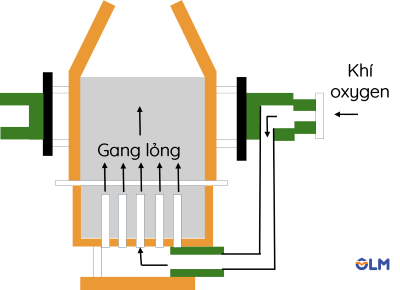
Nguyên liệu: Gang, khí oxygen.
Qúa trình sản xuất: Thổi khí oxygen vào lò đựng gang nóng chảy, tạo thành các oxide dạng khí (CO2, SO2) và các oxide rắn (SiO2, MnO2,...).
1. Các bước cơ bản trong quá trình tách kim loại từ quặng:
2. Một số phương pháp hóa học thường được sử dụng để tách kim loại:
- Phương pháp điện phân nóng chảy.
- Phương pháp nhiệt luyện.
- Phương pháp thủy luyện.
3. Hợp kim là vật liệu kim loại có chứa ít nhất một kim loại cơ bản và một kim loại hoặc phi kim khác. Hợp kim thường có nhiều ưu điểm vượt trội hơn so với kim loại nguyên chất như độ bền, độ cứng cao,...
4. Giai đoạn chính sản xuất gang:
- Tạo CO: C + O2 \(\underrightarrow{t^o}\) CO2; C + CO2 \(\underrightarrow{t^o}\) 2CO
- Tạo gang từ quặng: 3CO + Fe2O3 \(\underrightarrow{t^o}\) 2Fe + 3CO2
- Tạo xỉ, tách xỉ thu được gang: CaO + SiO2 \(\underrightarrow{t^o}\) CaSiO3
5. Quá trình sản xuất thép: Làm giảm các tạp chất C, Si, Mn,... trong gang bằng cách chuyển chúng thành các oxide và loại bỏ chúng để thu được thép.
Bạn có thể đăng câu hỏi về bài học này ở đây