Bài học cùng chủ đề
Báo cáo học liệu
Mua học liệu
Mua học liệu:
-
Số dư ví của bạn: 0 coin - 0 Xu
-
Nếu mua học liệu này bạn sẽ bị trừ: 2 coin\Xu
Để nhận Coin\Xu, bạn có thể:

Lý thuyết SVIP
I. KHÁI NIỆM VÀ DANH PHÁP
1. Khái niệm
Amino axit là những hợp chất hữu cơ tạp chức, phân tử chứa đồng thời nhóm amino (NH2) và nhóm caboxyl (COOH).
Tổng quát: (H2N)n-R-(COOH)m. Ví dụ: H2N-CH2-COOH (Glyxin).
2. Danh pháp
a. Tên thay thế
Tên của amino axit = Axit + số chỉ vị trí nhóm NH2 + amino + tên hệ thống của axit tương ứng với mạch chính.
Ví dụ:
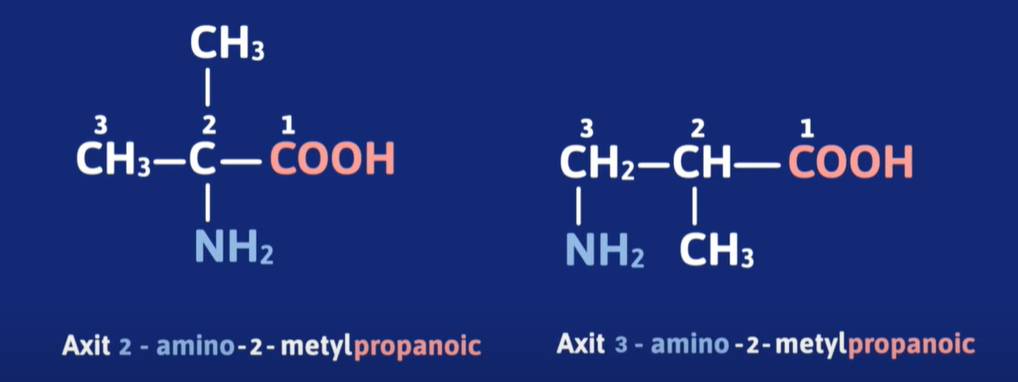
b. Tên bán hệ thống
Tên của amino axit = Axit + kí hiệu chỉ vị trí của nhóm amino(α, β,...) + amino + tên thông thường của của axit tương ứng với mạch chính.
Ví dụ:
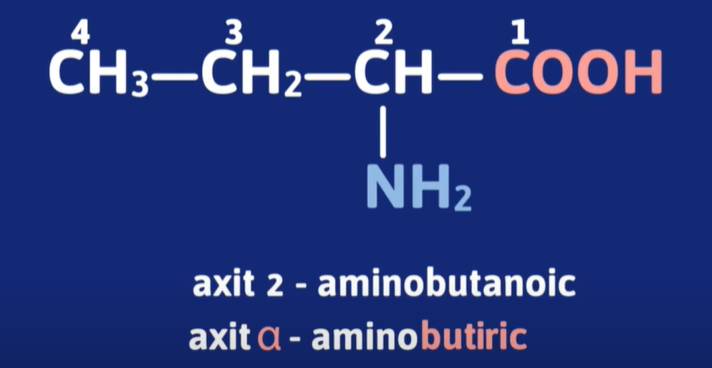
c. Tên thường
Các amino axit có trong tự nhiên (hầu hết là các α-amino axit) thường được gọi bằng tên thường.
| Công thức | Tên thường | Kí hiệu |
| H2N-CH2-COOH | Glyxin | Gly |
| CH3-CH(NH2)-COOH | Alanin | Ala |
| (CH3)2-CH-CH(NH2)-COOH | Valin | Val |
| H2N-[CH2]4-CH(NH2)-COOH | Lysin | Lys |
| HOOC-CH(NH2)-CH2-CH2-COOH | Axit glutamic | Glu |
II. CẤU TẠO PHÂN TỬ VÀ TÍNH CHẤT HÓA HỌC
1. Cấu tạo phân tử
Amino axit tồn tại ở dạng ion lưỡng cực do tương tác của nhóm NH2 với nhóm COOH:
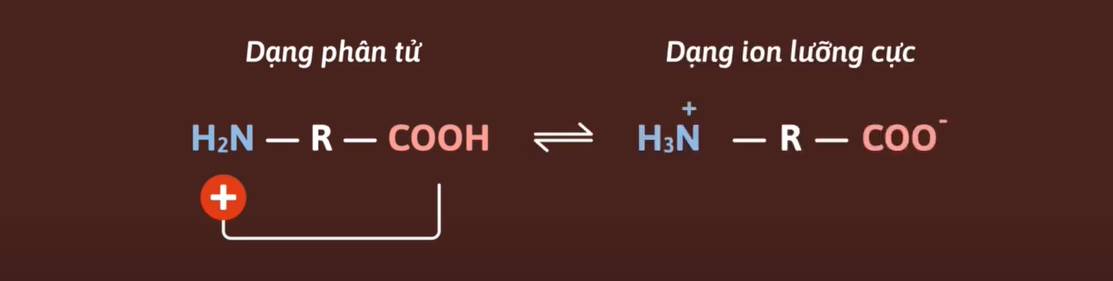
Do amino axit là những hợp chất có cấu tạo lưỡng cực, hút nhau nên ở điều kiện thường chúng là chất rắn, kết tinh, tương đối dễ tan trong nước và có nhiệt độ nóng chảy cao.
2. Tính chất hóa học
Trong phân tử amino axit có đồng thời 2 nhóm chức mang tính axit và bazơ, do đó amino axit thể hiện tính lưỡng tính.
a. Tính chất lưỡng tính
Amino axit vừa phản ứng với axit vô cơ mạnh sinh ra muối (tính chất của nhóm NH2) vừa phản ứng với bazơ sinh ra muối và nước (tính chất của nhóm COOH).
HOOC-CH2-NH2 + HCl → HOOC-CH2-NH3Cl
H2N-CH2COOH + NaOH → H2N-CH2COONa + H2O
b. Tính axit - bazơ của dung dịch amino axit
Tùy thuộc vào số lượng của nhóm NH2 và nhóm COOH trong phân tử mà dung dịch amino axit có những môi trường khác nhau.
| số -COOH > số -NH2 | số -COOH = số -NH2 | số -COOH < số -NH2 | |
| Môi trường | Axit | Trung tính | Bazơ |
| pH | <7 | =7 | >7 |
| Ví dụ | Glu | Gly | Lys |
c. Phản ứng este hóa
Tương tự axit cacboxylic, amoni axit phản ứng với ancol khi có mặt axit vô cơ mạnh sinh ra este. Ví dụ:
H2N-CH2-COOH + C2H5OH ![]() H2N-CH2-COOC2H5 + H2O
H2N-CH2-COOC2H5 + H2O
Vì phản ứng xảy ra trong môi trường axit nên sản phẩm cuối cùng là este dạng muối ClH3N-CH2-COOC2H5.
d. Phản ứng trùng ngưng
Phản ứng trùng ngưng là phản ứng cộng hợp liên tiếp nhiều phân tử nhỏ (monome) tạo thành phân tử lớn hơn (polime) đồng thời giải phóng nhiều phân tử nhỏ khác (H2O, NH3,...).
Khi đun nóng, các ϵ - hoặc ω - amino axit tham gia phản ứng trùng ngưng tạo ra polime thuộc loại poliamit. Khi đó, OH của nhóm COOH ở phân tử amino axit này kết hợp với H của nhóm NH2 ở phân tử amino axit kia giải phóng ra nước và sinh ra polime do các gốc amino axit kết hợp với nhau. Ví dụ:
nH2N-[CH2]5-COOH \(\underrightarrow{t^o}\) -(-NH-[CH2]5-CO-)-n (policaproamit) + nH2O
III. ỨNG DỤNG
- Các amino axit thiên nhiên là những hợp chất cơ sở để kiến tạo nên các protein của cơ thể sống.
- Muối mononatri của axit glutamic là thành phần của bột ngọt hay mì chính.
- Axit glutamic là thuốc hỗ trợ thần kinh, methionin là thuốc bổ gan.
- Methionin là thuốc bổ gan.
- Các axit ϵ - amonicaproic và ω - aminoenantoic là nguyên liệu để sản xuất tơ nilon - 6 và nilon - 7,...
Trong quá trình học tập, nếu có bất kỳ thắc mắc nào, các em hãy để lại câu hỏi ở mục hỏi đáp để cùng thảo luận và trả lời nhé. Chúc các em học tốt!
Bạn có thể đăng câu hỏi về bài học này ở đây
