Bài học cùng chủ đề
Báo cáo học liệu
Mua học liệu
Mua học liệu:
-
Số dư ví của bạn: 0 coin - 0 Xu
-
Nếu mua học liệu này bạn sẽ bị trừ: 2 coin\Xu
Để nhận Coin\Xu, bạn có thể:

Lý thuyết SVIP
I. ĐƠN CHẤT
1. Đơn chất là gì?
Đơn chất là những chất được tạo nên từ một nguyên tố hóa học. Đơn chất có thể chứa một hoặc nhiều nguyên tử của cùng một nguyên tố hóa học.
Ví dụ: khí hiđro tạo nên từ nguyên tử H, khí oxi tạo nên từ nguyên tử O, kim loại sắt tạo nên từ nguyên tử Fe,...
Có 2 loại đơn chất là đơn chất kim loại và đơn chất phi kim.
- Đơn chất kim loại: có ánh kim, dẫn được điện, nhiệt.
- Đơn chất phi kim: không có ánh kim, không dẫn điện, nhiệt.

2. Đặc điểm cấu tạo
Trong đơn chất kim loại các nguyên tử sắp xếp khít nhau và theo một trật tự xác định.
Trong đơn chất phi kim các nguyên tử thường liên kết với nhau theo một số nhất định và thường là 2.
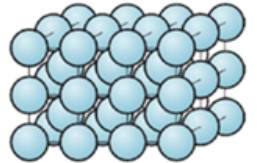

Mô hình liên kết của kim loại và hidro.
II. HỢP CHẤT
1. Hợp chất là gì ?
Nước có công thức hóa học là H2O được tạo nên từ 2 nguyên tố hóa học là H và O, muối ăn có công thức hóa học NaCl được tạo nên từ 2 nguyên tố Na và Cl, axit sunfuric H2SO4 được tạo nên từ 3 nguyên tố H, S, O... Những chất này được gọi là hợp chất.
Vậy, hợp chất là những chất được tạo nên từ hai nguyên tố trở nên.
Có 2 loại hợp chất trong hóa học là hợp chất vô cơ và hợp chất hữu cơ, những chất kể trên là hợp chất vô cơ. Những hợp chất như khí metan (CH4), etilen (C2H4), đường (C12H22O11),... là hợp chất hữu cơ sẽ đề cập ở 2 chương cuối sách giáo khoa lớp 9.

2. Đặc điểm cấu tạo
Trong hợp chất , nguyên tử của các nguyên tố liên kết với nhau theo một tỉ lệ và một thứ tự nhất định.
III. PHÂN TỬ
1. Định nghĩa
Phân tử hạt là đại diện cho chất, gồm một số nguyên tử liên kết với nhau và thể hiện đầy đủ tính chất hóa học của chất.
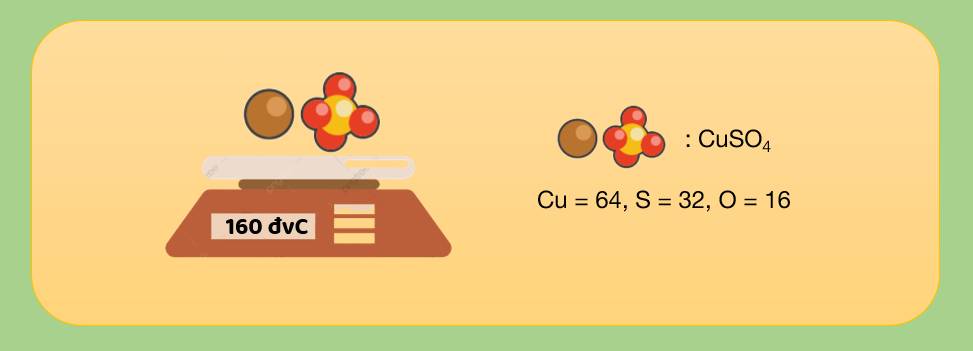
2. Phân tử khối
Phân tử khối là khối lượng của một phân tử tính bằng đơn vị cacbon.
Phân tử khối của một chất bằng tổng nguyên tử khối của các nguyên tử có trong phân tử chất đó.
Ví dụ:
Phân tử khối của H2O = 2.1 + 16 = 18 đvC.
Phân tử khối của muối ăn NaCl = 23 + 35,5 = 58,5 đvC.
IV. TRẠNG THÁI CỦA CHẤT
Mỗi mẫu chất là một tập hợp vô cùng lớn những nguyên tử (đơn chất) hay những phân tử (hợp chất). Tùy vào điều kiện về nhiệt độ và áp suất, thường một chất có thể tồn tại ở ba trạng thái: rắn, lỏng và khí (hay hơi).
Ví dụ: nước đá (rắn), nước lỏng và hơi nước (khí).
Khi các chất ở trạng thái rắn, các hạt (nguyên tử hay phân tử) sắp xếp khít nhau và dao động tại chỗ. | Ở trạng thái lỏng, các hạt ở gần sát nhau và chuyển động trượt lên nhau. | Ở trạng thái khí, các hạt ở rất xa nhau và chuyển động nhanh hơn, về nhiều phía khác nhau |
.gif) | .gif) | .gif) |
1. Đơn chất là những chất tạo nên từ một nguyên tố hóa học.
2. Hợp chất là những chất tạo nên từ hai nguyên tố hóa học trở nên.
3. Phân tử là hạt đại diện cho chất, gồm một số nguyên tử liên kết với nhau và thể hiện đầy đủ tính chất hóa học của chất.
4. Phân tử khối là khối lượng của một phân tử tính bằng đơn vị cacbon, bằng tổng nguyên tử khối của các nguyên tử trong phân tử.
5. Mỗi mẫu chất là một tập hợp vô cùng lớn những hạt là phân tử hay nguyên tử. Tùy điều kiện, một chất có thể ở ba trạng thái: rắn, lỏng, khí. Ở trạng thái khí các hạt ở rất xa nhau.
Trong quá trình học tập, nếu có bất kỳ thắc mắc nào, các em hãy để lại câu hỏi ở mục hỏi đáp để cùng thảo luận và trả lời nhé. Chúc các em học tốt!
Bạn có thể đăng câu hỏi về bài học này ở đây
