Bài học cùng chủ đề
Báo cáo học liệu
Mua học liệu
Mua học liệu:
-
Số dư ví của bạn: 0 coin - 0 Xu
-
Nếu mua học liệu này bạn sẽ bị trừ: 2 coin\Xu
Để nhận Coin\Xu, bạn có thể:

Thành phần của nguyên tử SVIP
I. CÁC LOẠI HẠT CẤU TẠO NÊN NGUYÊN TỬ
Thành phần cấu tạo của nguyên tử gồm:
- Hạt nhân: ở tâm của nguyên tử, chứa các proton mang điện tích dương và các neutron không mang điện.
- Vỏ nguyên tử: chứa các electron mang điện tích âm, chuyển động rất nhanh xung quanh hạt nhân.
| Hạt | Kí hiệu | Khối lượng (kg) | Khối lượng (amu) | Điện tích (C) | Điện tích tương đối |
| Proton | p | 1,672.10-27 | ≃ 1 | 1,602.10-19 | +1 |
| Neutron | n | 1,675.10-27 | ≃ 1 | 0 | 0 |
| Electron | e | 9,109.10-31 | ≃ 0,00055 | -1,602.10-19 | -1 |
Khối lượng, điện tích của các loại hạt cấu tạo nên nguyên tử
- Trong nguyên tử, số proton bằng số electron nên nguyên tử trung hoà về điện.
- Khối lượng electron rất nhỏ, không đáng kể so với khối lượng của proton hay neutron nên khối lượng nguyên tử tập trung hầu hết ở hạt nhân.
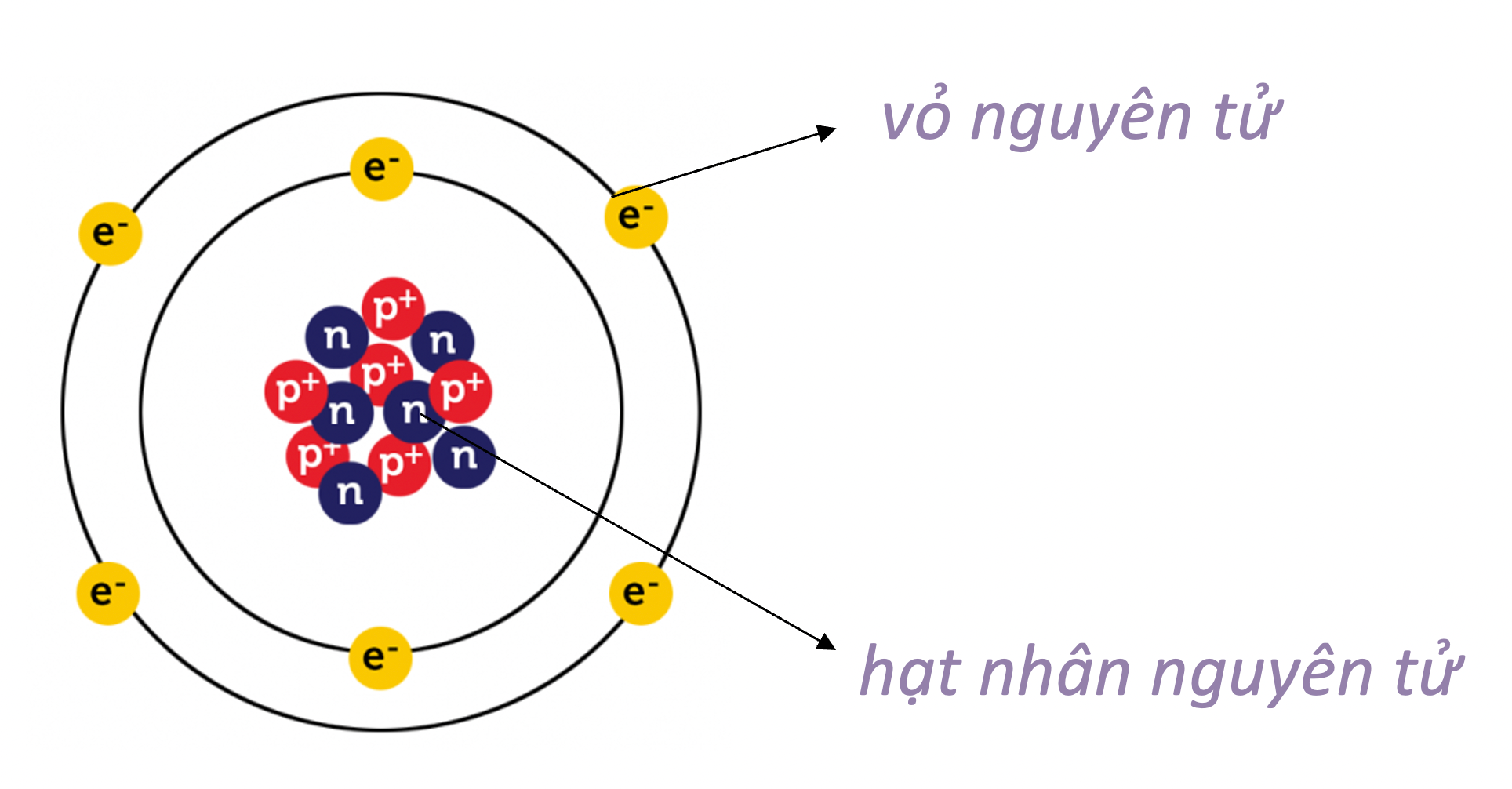
Sơ đồ cấu tạo nguyên tử
II. KÍCH THƯỚC VÀ KHỐI LƯỢNG CỦA NGUYÊN TỬ
1. Kích thước
- Kích thước của nguyên tử là khoảng không gian tạo bởi sự chuyển động của electron.
- Các nguyên tử khác nhau có số electron khác nhau nên có kích thước khác nhau.
- Nếu coi nguyên tử như một khối cầu thì đường kính của nó chỉ khoảng 10-10 m.
- Hạt nhân nguyên tử có kích thước nhỏ hơn rất nhiều so với kích thước nguyên tử.

So sánh kích thước của nguyên tử với một số vật thể
2. Khối lượng
- Khối lượng nguyên tử bằng tổng khối lượng các hạt proton, neutron và electron có trong nguyên tử.
- Một lượng chất rất nhỏ cũng chứa tới hàng tỉ tỉ nguyên tử, nên để biểu thị khối lượng nguyên tử người ta sử dụng đơn vị amu.
1 amu ≃ 1,661.10-27 kg
Ví dụ 1: Một nguyên tử oxygen có khối lượng là 2,656.10-26 kg.
1 amu ≃ 1,661.10-27 kg nên khối lượng một nguyên tử oxygen là 15,990 amu.
III. ĐIỆN TÍCH HẠT NHÂN VÀ SỐ KHỐI
- Số proton trong hạt nhân nguyên tử bằng số đơn vị điện tích hạt nhân, kí hiệu là Z.
Ví dụ 2: Hạt nhân nguyên tử Na có 11 proton nên số đơn vị điện tích hạt nhân là Z = 11.
- Tổng số proton và neutron trong hạt nhân của một nguyên tử được gọi là số khối (hay số nucleon), kí hiệu là A.
A = Z + số neutron
Ví dụ 3: Hạt nhân nguyên tử Na có số proton là 11 và số neutron là 12 nên số khối của hạt nhân nguyên tử Na là
A = 11 + 12 = 23
1. Nguyên tử vô cùng nhỏ nhưng được tạo thành từ những hạt nhỏ hơn, gồm hạt nhân (chứa proton mang điện tích dương và neutron không mang điện) và vỏ nguyên tử (chứa các electron mang điện tích âm). Nguyên tử trung hoà về điện vì có số proton bằng số electron.
2. Khối lượng nguyên tử tập trung ở hạt nhân (do khối lượng của electron rất nhỏ so với khối lượng của proton và neutron).
3. Hạt nhân nguyên tử có kích thước vô cùng nhỏ so với nguyên tử.

Bạn có thể đánh giá bài học này ở đây