Báo cáo học liệu
Mua học liệu
Mua học liệu:
-
Số dư ví của bạn: 0 coin - 0 Xu
-
Nếu mua học liệu này bạn sẽ bị trừ: 2 coin\Xu
Để nhận Coin\Xu, bạn có thể:

Ester - Lipid SVIP
I. ESTER
1. Khái niệm và danh pháp
a. Khái niệm
Ester được tạo thành khi nhóm -OH trong nhóm -COOH (carboxyl) bị thay thế bằng nhóm -OR'.
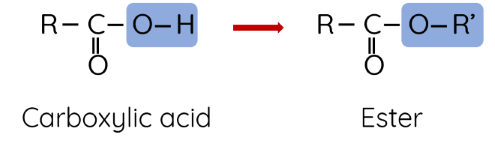
Công thức chung của ester đơn chức là RCOOR'. Trong đó R là gốc hydrocarbon hoặc H, R' là gốc hydrocarbon.
Ví dụ: CH3COOCH3, C6H5COOCH2CH3,...
Câu hỏi:
@202742691997@
b. Danh pháp
Tên gọi của ester đơn chức: Tên gốc R' + Tên gốc RCOO (tên gốc RCOO được hình thành bằng cách thay thế đuôi ic trong carboxylic acid thành đuôi ate).
Ví dụ:
HCOOCH2CH3 ethyl formate hoặc ethyl methanonate.
CH3COOC2H5 ethyl acetate hoặc ethyl ethanonate.
2. Tính chất vật lí
Ester thường là chất lỏng hoặc rắn, có mùi thơm và nhẹ hơn nước.
Nhiệt độ sôi của ester thấp hơn alcohol và carboxylic acid cùng số nguyên tử carbon.
Do không tạo được liên kết hydrogen với nước nên ester ít tan trong nước, một số ester có phân tử khối nhỏ có thể bị hòa tan một phần. Ngoài ra, ester còn là dung môi hòa tan các chất hữu cơ.

CH3[CH2]2COOC2H5 có mùi thơm của dứa chín
Câu hỏi:
@202742124381@
3. Tính chất hóa học
Ester bị thủy phân trong môi trường acid tạo thành alcohol (phenol) và carboxylic acid tương ứng.
Ester bị thủy phân trong môi trường base (NaOH, KOH) tạo thành muối carboxylate và alcohol.
Ví dụ: Ethyl acetate bị thủy phân trong môi trường acid tạo thành acetic acid và ethylic alcohol (phản ứng thuận nghịch).
\(CH_3COOCH_2CH_3+H_2O\overset{H^{+},t^{o}}{\rightleftharpoons}CH_3COOH+CH_3CH_2OH\)
Ví dụ: Ethyl acetate bị thủy phân trong môi trường kiềm tạo thành muối của acetic acid và ethylic alcohol (phản ứng xà phòng hóa).
\(CH_3COOCH_2CH_3+NaOH\overset{t^{o}}{\rarr}CH_3COONa+CH_3CH_2OH\)
@202742703338@
4. Ứng dụng và điều chế
a. Ứng dụng
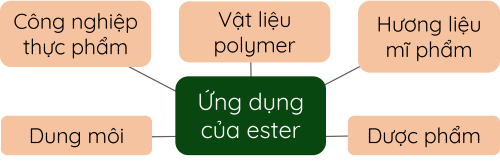
b. Điều chế
Ester hình thành từ phản ứng giữa carboxylic acid và alcohol, có xúc tác là H2SO4 đặc.
\(RCOOH+R^{^{\prime}}OH\overset{H_2SO_4đ,t^{o}}{\rightleftharpoons}RCOOR^{^{\prime}}+H_2O\)
Câu hỏi:
@202742707664@
II. LIPID
1. Khái niệm và danh pháp
Lipid là các hợp chất hữu cơ có trong tế bào sống, không tan trong nước nhưng tan trong dung môi không phân cực.
Chất béo là triester của glycerol với acid béo (carboxylic acid đơn chức, mạch dài, không phân nhánh, thường có số nguyên tử carbon chẵn. Gốc hydrocarbon có thể no hoặc không no).
Công thức tổng quát của chất béo:

Chất béo thường gặp là ester của các acid béo sau:
Phân loại | Acid béo thường gặp |
Acid béo no | Palmitic acid: CH3(CH2)14COOH Stearic acid: CH3(CH2)16COOH |
Acid béo không no | Oleic acid: CH3(CH2)7CH=CH(CH2)7COOH Linoleic acid: CH3(CH2)4CH=CHCH2CH=CH(CH2)7COOH |
Câu hỏi:
@202742284231@
2. Tính chất vật lí
Chất béo no thường tồn tại ở trạng thái rắn (mỡ lợn, mỡ bò,...), chất béo không no thường tồn tại ở trạng thái lỏng (dầu vừng, dầu lạc, dầu cá,...).
Chất béo nhẹ hơn nước và không tan trong nước nhưng tan tốt trong dung môi ít phân cực.
3. Tính chất hóa học
Chất béo là ester nên có thể bị thủy phân.
Chất béo không no có thể hydrogen hóa thành chất béo no dạng rắn và dễ bị oxi hóa tạo ra mùi khó chịu.
a. Phản ứng hydrogen hóa
Chất béo không no có thể phản ứng với hydrogen tạo thành chất béo no.
Ví dụ:
\(\left(C_{15}H_{33}COO\right)_3C_3H_5+3H_2\overset{t^{o},xt,p}{\rarr}\left(C_{15}H_{35}COO\right)_3C_3H_5\)
b. Phản ứng oxi hóa bằng oxygen không khí
Các gốc acid béo không no chứa liên kết đôi kém bền nên dễ bị oxi hóa chậm bởi oxygen trong không khí tạo ra các chất có mùi khó chịu, gây ôi thiu.
Câu hỏi:
@202742290740@
4. Ứng dụng
Chất béo đóng vai trò cung cấp, dự trữ năng lượng cho cơ thể. Acid béo omega-3 và omega-6 có vai trò quan trọng đối với cơ thể.
Ngoài ra, chất béo còn là nguyên liệu trong sản xuất thực phẩm, xà phòng, glycerol,...

Các thực phẩm chứa nhiều omega-3
Câu hỏi:
@202742335358@
Bạn có thể đăng câu hỏi về bài học này ở đây
