Báo cáo học liệu
Mua học liệu
Mua học liệu:
-
Số dư ví của bạn: 0 coin - 0 Xu
-
Nếu mua học liệu này bạn sẽ bị trừ: 2 coin\Xu
Để nhận Coin\Xu, bạn có thể:

Định luật tuần hoàn. Ý nghĩa bảng tuần hoàn hóa học SVIP

Lưu ý: Ở điểm dừng, nếu không thấy nút nộp bài, bạn hãy kéo thanh trượt xuống dưới.
Bạn phải xem đến hết Video thì mới được lưu thời gian xem.
Để đảm bảo tốc độ truyền video, OLM lưu trữ video trên youtube. Do vậy phụ huynh tạm thời không chặn youtube để con có thể xem được bài giảng.
Nội dung này là Video có điểm dừng: Xem video kết hợp với trả lời câu hỏi.
Nếu câu hỏi nào bị trả lời sai, bạn sẽ phải trả lời lại dạng bài đó đến khi nào đúng mới qua được điểm dừng.
Bạn không được phép tua video qua một điểm dừng chưa hoàn thành.
Dữ liệu luyện tập chỉ được lưu khi bạn qua mỗi điểm dừng.
Nội dung bài học:
- Định luật tuần hoàn:
Tính chất của các nguyên tố và đơn chất, cũng như thành phần và tính chất của các hợp chất tạo nên từ các nguyên tố đó biến đổi tuần hoàn theo chiều tăng của điện tích hạt nhân nguyên tử.
- Ý nghĩa của bảng tuần hoàn hóa học:
Từ vị trí của một nguyên tố trong bảng tuần hoàn, có thể dự đoán được tính chất của đơn chất và hợp chất tạo nên từ nguyên tố đó.
Nguyên tố potassium (Z=19) có cấu hình nguyên tử là 1s22s22p63s23p64s1. Xác định vị trí của potassium trong bảng tuần hoàn.
Các nguyên tố trong bảng tuần hoàn được sắp xếp theo chiều tăng dần
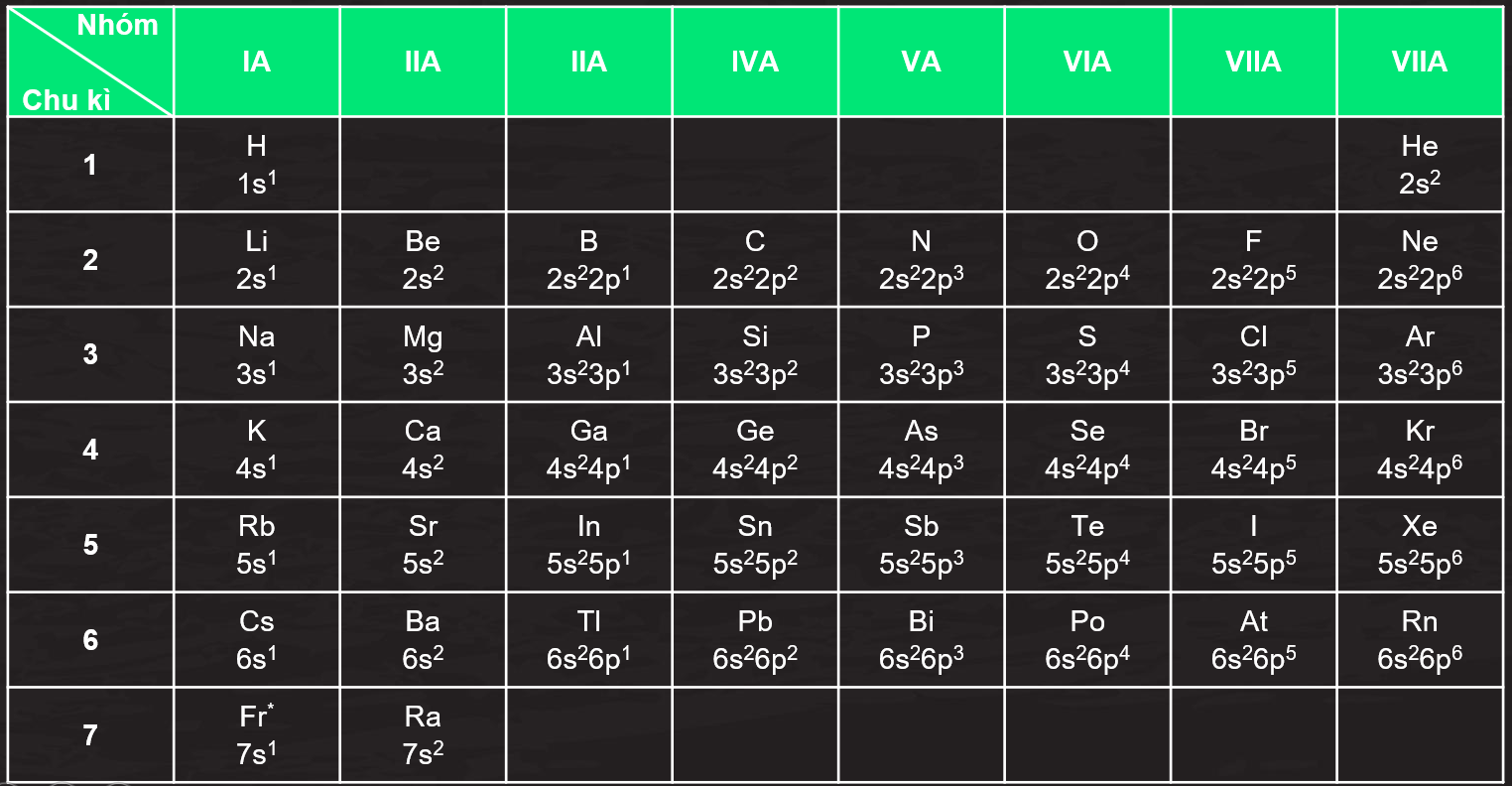
Quan sát bảng sau và cho biết cấu hình electron lớp ngoài cùng của các nguyên tử nguyên tố nhóm A biến đổi như thế nào trong chu kì và nhóm.
Văn bản dưới đây là được tạo ra tự động từ nhận diện giọng nói trong video nên có thể có lỗi
- Xin chào các em đã đến với khóa học khóa
- học 10 của olm.vn để tiếp tục tìm hiểu
- về bảng tuần hoàn chúng ta cùng đến với
- bài học ngày hôm nay định luật tuần hoàn
- ý nghĩa của bảng tuần hoàn hóa học nội
- dung bài học gồm có 2 phần 1 định luật
- tuần hoàn 2 ý nghĩa của bảng tuần hoàn
- hóa học trước khi vào bài Chúng ta cùng
- đến với mục Em có biết chiếc slide của
- cô là Flora được dùng là chất oxy hóa
- cho nhiên liệu lỏng dùng trong tên lửa
- floride có ký hiệu là F là nguyên tố hóa
- học có số hiệu nguyên tử bằng 9 thuộc
- chu kì 2 nhóm 7A từ vị trí của Fly trong
- bảng tuần hoàn có thể dự đoán được tính
- chất hóa học cơ bản của fran không và
- khả năng phản ứng của Fly như thế nào
- cũng chính những câu hỏi này mà các nhà
- khoa học đã tìm ra các định luật tuần
- hoàn để dự đoán tính chất hóa học của
- các nguyên tố trong bảng tuần hoàn Giúp
- cho việc tìm ra các tính chất cũng như
- là việc làm thí nghiệm sẽ diễn ra chính
- xác và nhanh hơn vậy định luật tuần hoàn
- là gì chúng ta cùng tìm hiểu phần 1 định
- luật hệ tuần hoàn trên slide của cô là
- bảng cấu hình electron lớp ngoài cùng
- của các nguyên tử nhóm A tương tự như
- các bài trước chúng ta sẽ cùng quan sát
- bảng và trả lời cho cô biết sự biến đổi
- của số electron lớp ngoài cùng các
- nguyên tử nhóm A trong một nhóm và trong
- một chu kỳ diễn ra như thế nào
- Câu trả lời của các em rất chính xác ta
- thấy rằng sau mỗi chu kỳ cấu hình
- electron lớp ngoài cùng của nguyên tử
- các nguyên tố nhóm A được lặp đi lặp lại
- một cách tuần hoàn và ở trong bài xu
- hướng biến đổi một số tính chất của
- nguyên tử các nguyên tố trong một nhóm
- mà trong một chu kỳ cô đã Giảng rất chi
- tiết các em có thể theo dõi lại như thế
- thì ta thấy được rằng là cái sự biến đổi
- tuần hoàn về cấu hình electron lớp ngoài
- cùng của nguyên tử các nguyên tố khi
- điện tích hạt nhân tăng dần chính là
- nguyên nhân của sự biến đổi tuần hoàn về
- tính chất của các nguyên tố cũng như là
- hợp chất các nguyên tố đó vậy định luật
- tuần hoàn sẽ được kết luận như sau tính
- chất của các nguyên tố và đơn chất cũng
- như thành phần và tính chất của các hợp
- chất tạo nên từ các nguyên tố đó biến
- đổi tuần hoàn theo chiều tăng dần của
- điện tích hạt nhân nguyên tử và Chính vì
- có định luật tuần hoàn dẫn đến sự phát
- triển và hoàn thiện của bảng tuần hoàn
- các nguyên tố hóa học hiện nay như vậy
- thì dựa vào sự biến đổi tuần hoàn ta có
- thể dự đoán được tính chất của các chất
- khác nhau Bây giờ các em Hãy trả lời câu
- hỏi nhỏ sau các nguyên tố trong bảng
- tuần hoàn được sắp xếp theo chiều tăng
- dần a khối lượng nguyên tử b bán kính
- nguyên tử C số hiệu nguyên tử và D số âm
- điện của nguyên tử
- rất dễ dàng để có thể trả lời được câu
- hỏi này các nguyên tố trong bảng tuần
- hoàn được sắp xếp theo chiều tăng của
- điện tích hạt nhân vậy Thế thì ở đây cô
- không có câu nào là điện tích hạt nhân
- cả nhưng mà chúng ta phải hiểu được rằng
- là số hiệu nguyên tử của chúng ta cũng
- chính bằng điện tích hạt nhân vậy đáp án
- đúng của cô ở trong câu hỏi này sẽ là
- câu c cô và các em đã tìm hiểu xong định
- luật tuần hoàn bây giờ chúng ta hãy cùng
- tìm hiểu về ý nghĩa của bảng tuần hoàn
- nguyên tố hóa học trên slide của cô là
- bảng tuần hoàn 118 nguyên tố ví dụ của
- cô như sau nguyên tố sunfua ở ô số 16
- nhóm 6A chu kỳ 3 Thế thì khi mà mình
- nhìn vào bảng tuần hoàn nguyên tố hóa
- học nguyên tố sunfua có số thứ tự vị trí
- của chu kỳ và nhóm thì sẽ cho chúng ta
- biết điều gì thì bây giờ ta cùng phân
- tích ta thấy rằng nguyên tử sunfua có 16
- proton 16 electron do số proton bằng số
- electron và bằng số Z có 3 lớp electron
- do số lớp electron bằng số thứ tự chu kỳ
- và có 6 electron lớp ngoài cùng
- lớp ngoài cùng bằng với số thứ tự nhóm A
- ngoài ra cấu hình electron của sunfua là
- một S2 2s2 2v6 3s2 3 B4 ta dễ dàng thấy
- được rằng là sunfua là nguyên tố phi kim
- cũng như oxit cao nhất của sunfua là SO3
- và axit tương ứng là H2SO4 như vậy thì
- các em thấy rằng khi mà mình biết vị trí
- nguyên tố trong bảng tuần hoàn ta có thể
- suy ra được cấu hình electron và từ đó
- ta có thể suy ra được tính chất của
- nguyên tố đó Bây giờ các em hãy làm câu
- hỏi tương tác sau của cô nguyên tố
- potassium có Z = 19 cấu hình nguyên tử
- 1s2 2s2 hai b63 S2 3b6 và 4s1 hãy xác
- định vị trí của potatium trong bảng tuần
- hoàn câu hỏi này sẽ khó hơn một chút Bởi
- vì cô đang cho các em cấu hình electron
- nguyên tử
- Tuy rằng câu hỏi này cô có hỏi khác đi
- một chút nhưng các em làm rất tốt thai
- Cùng phân tích như ví dụ trên ta thấy Z
- của potatium bằng 19 như vậy ta suy ra
- butadium thuộc ô số 19 trong bảng tuần
- hoàn trước khi 4 ra lớp electron lớp
- ngoài cùng bằng số thứ tự chu kỳ nhóm 1A
- do số electron lớp ngoài cùng bằng số
- thứ tự của nhóm A ngoài ra cô còn cung
- cấp thêm cho các em mochachium có ký
- hiệu là k và là nguyên tố kim loại oxit
- cao nhất là K2O là bazơ Oxit Bazơ tương
- ứng của butadium sẽ là KOH Đây là một
- bazơ mạnh vậy thì mình sẽ có thêm một
- kết luận nữa đó chính là từ cấu hình
- electron nguyên tử chúng ta có thể suy
- ra vị trí của nguyên tố trong bảng tuần
- hoàn và cũng suy ra được tính chất của
- nguyên tố đó như vậy thì vị trí của
- nguyên tố trong bảng tuần hoàn các
- nguyên tố hóa học cho biết cấu hình
- electron nguyên tử cấu hình electron
- nguyên tử thì lại quyết định tính chất
- của nguyên tố đặc chúng sẽ có sự tương
- tác qua lại với nhau ngoài ra cô mở rộng
- thêm cho các em dựa vào định luật tuần
- hoàn có thể so sánh được tính chất của
- một nguyên tố với các nguyên tố xung
- quanh thế thì Câu hỏi đặt ra Hãy so sánh
- tính phi kim của phosphorit Z = 15 với
- natron z bằng 7 và sunfua Z = 16 khi ta
- đã học về ý nghĩa của bảng tuần hoàn ta
- biết được rét ta có thể viết được cấu
- hình electron của các nguyên tố trên như
- vậy dễ dàng có thể viết được cấu hình
- của phosperis Nike
- khi nhìn vào cấu hình ta nhận xét ph
- phosphorit và Nike
- lớp ngoài cùng nên tính phi kim của Nike
- lớn hơn phosphorit phần này chúng ta đã
- biết trong một nhóm tính phi kim sẽ
- Motion từ trên xuống tiếp theo ta quan
- sát thấy phosphorit và sunfua cùng một
- chu kỳ vì chúng có cùng số lớp electron
- nên tính phi kim của phosphorit sẽ nhỏ
- hơn sunfua nhắc lại trong một nhóm tính
- phi kim sẽ tăng dần từ trái qua phải sau
- khi cô phân tích cái ví dụ này thì ta
- càng khẳng định được dựa vào định luật
- tuần hoàn ta có thể so sánh được tính
- chất của một nguyên tố với các nguyên tố
- xung quanh và để kết thúc bài giảng Ngày
- hôm nay chúng ta cùng đến với phần kết
- luận bài học chúng ta đã học về định
- luật tuần hoàn tính chất của các nguyên
- tố và đơn chất cũng như thành phần và
- tính chất của hợp chất tạo nên từ các
- nguyên tố đó biến đổi tuần hoàn theo
- chiều tăng của điện tích hạt nhân nguyên
- tử 2 ý nghĩa của bảng tuần hoàn từ vị
- trí của một nguyên tố trong bảng tuần
- hoàn có thể dự đoán được tính chất của
- đơn chất và hợp chất tạo nên từ nguyên
- tố đó các em hãy ghi chép nội dung chính
- của bài khoa học và vợ và bài học ngày
- hôm nay của chúng ta đã kết thúc tại đây
- Cảm ơn các em đã theo dõi các em hãy
- truy cập vào trang web online.vn để
- luyện tập và tương tác trực tiếp đừng
- quên nhấn kênh theo dõi hoặc trực tuyến
- online
- và hẹn gặp lại các em trong các video
- bài giảng tiếp theo
Bạn có thể đăng câu hỏi về bài học này ở đây
