Báo cáo học liệu
Mua học liệu
Mua học liệu:
-
Số dư ví của bạn: 0 coin - 0 Xu
-
Nếu mua học liệu này bạn sẽ bị trừ: 2 coin\Xu
Để nhận Coin\Xu, bạn có thể:
CHÚC MỪNG
Bạn đã nhận được sao học tập

Chú ý:
Thành tích của bạn sẽ được cập nhật trên bảng xếp hạng sau 1 giờ!
Biến thiên enthalpy trong các phản ứng hóa học (phần 2) SVIP

Nếu video không chạy trên Zalo, bạn vui lòng Click vào đây để xem hướng dẫn
Lưu ý: Ở điểm dừng, nếu không thấy nút nộp bài, bạn hãy kéo thanh trượt xuống dưới.
Bạn phải xem đến hết Video thì mới được lưu thời gian xem.
Để đảm bảo tốc độ truyền video, OLM lưu trữ video trên youtube. Do vậy phụ huynh tạm thời không chặn youtube để con có thể xem được bài giảng.
Nội dung này là Video có điểm dừng: Xem video kết hợp với trả lời câu hỏi.
Nếu câu hỏi nào bị trả lời sai, bạn sẽ phải trả lời lại dạng bài đó đến khi nào đúng mới qua được điểm dừng.
Bạn không được phép tua video qua một điểm dừng chưa hoàn thành.
Dữ liệu luyện tập chỉ được lưu khi bạn qua mỗi điểm dừng.
Lưu ý: Ở điểm dừng, nếu không thấy nút nộp bài, bạn hãy kéo thanh trượt xuống dưới.
Bạn phải xem đến hết Video thì mới được lưu thời gian xem.
Để đảm bảo tốc độ truyền video, OLM lưu trữ video trên youtube. Do vậy phụ huynh tạm thời không chặn youtube để con có thể xem được bài giảng.
Nội dung này là Video có điểm dừng: Xem video kết hợp với trả lời câu hỏi.
Nếu câu hỏi nào bị trả lời sai, bạn sẽ phải trả lời lại dạng bài đó đến khi nào đúng mới qua được điểm dừng.
Bạn không được phép tua video qua một điểm dừng chưa hoàn thành.
Dữ liệu luyện tập chỉ được lưu khi bạn qua mỗi điểm dừng.
Theo dõi OLM miễn phí trên Youtube và Facebook:
Nội dung bài học gồm:
- Phản ứng tỏa nhiệt, phản ứng thu nhiệt.
- Biến thiên enthalpy.
- Tính biến thiên của phản ứng theo nhiệt tạo thành.
- Tính biến thiên của phản ứng theo năng lượng liên kết.
Đây là bản xem trước câu hỏi trong video.
Hãy
đăng nhập
hoặc
đăng ký
và xác thực tài khoản để trải nghiệm học không giới hạn!
Câu 1 (1đ):
Cho biết năng lượng liên kết trong phân tử O2, N2 và NO lần lượt là 494 kJ/mol, 945 kJ/mol và 607 kJ/mol. Tính biến thiên chuẩn của phản ứng:
N2(g) + O2(g) to 2NO(g)
-832 kJ.
-225 kJ.
225 kJ.
832 kJ.
Câu 2 (1đ):
Từ số liệu bảng nhiệt tạo thành của các chất, hãy xác định biến thiên enthlapy chuẩn của phản ứng cháy ethane:
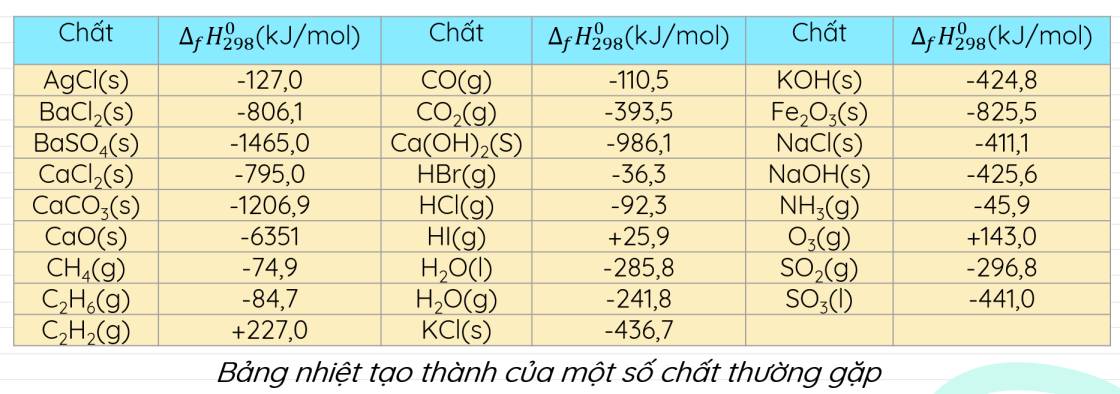
+1644,4 kJ/mol.
-1559,7 kJ/mol.
+1559,7 kJ/mol.
-1729,1 kJ/mol.
Văn bản dưới đây là được tạo ra tự động từ nhận diện giọng nói trong video nên có thể có lỗi
- Chào mừng các em đã quay trở lại với
- khóa học khóa học 10 cõi là m.vn để tìm
- hiểu tiếp tục về bài biến thiên mmp
- trong các phản ứng hóa học chúng ta cùng
- đến với phần 2 phần 2 chúng ta tìm hiểu
- nốt về mục 3 và 4 là tính biến thiên bi
- của phản ứng theo nhiệt tạo thành và
- tính biến thiên .me của phản ứng theo
- năng lượng liên kết ở phần khởi động cô
- có trên các vỏ hộp thực phẩm thường ghi
- các giá trị năng lượng vậy giá trị năng
- lượng là gì năng lượng là do một thực
- phẩm định cung cấp khi chuyển hóa hoàn
- toàn và cơ thể bất kỳ một sản phẩm khi
- chúng ta ăn vào trong cơ thể đều sẽ có
- giá trị năng lượng Vậy để tìm hiểu một
- giá trị mới chúng ta phải hiểu được giá
- trị đó như thế nào như vậy Đầu tiên
- chúng ta cần hiểu về khái niệm và mục 3
- là tính biến thiên ety của phản ứng theo
- nhiệt tạo thành Vậy nhiệt tạo thành là
- gì nhiệt tạo thành của một chất là biến
- thiên ethanbi của phản ứng tạo thành một
- mol chất đó từ đơn chất ở dạng bền vững
- nhất ở một điều kiện nhất định nhiệt tạo
- thành chuẩn của chúng ta nên tạo fh0 298
- nhiệt tạo thành của đơn chất ở dạng bền
- vững nhất sẽ bằng không Ví dụ như nhiệt
- tạo thành của hidrozen ở trạng thái khí
- thì sẽ là không kj/mon và ví dụ của cô
- như sau nước lỏng được tạo thành từ khí
- hidrogen và khí oxygen Ta có phương
- trình hóa học hidrogen cộng với 1/2
- option tạo thành phân tử nước và ở điều
- kiện thường cứ một mol nước tạo thành từ
- 1 mol hidrogen và 1/2 mol option sẽ giải
- phóng ra
- 285,8 kj
- của cô là Bảng Nhập tạo thành của một số
- chất thường gặp các em có thể sử dụng đó
- để tra cứu và tính toán
- ethanbi của phản ứng nhiệt tạo thành vậy
- Thế thì chúng ta đã tìm hiểu xong về
- khái niệm rồi bây giờ chúng ta cùng đến
- với phần 2 tính biến thiên ethanbi của
- phản ứng theo nhiệt tạo thành biến thiên
- etampy của phản ứng được xác định bằng
- Hiệu số giữa tổng như tạo thành của các
- chất sản phẩm và tổng nhiệt tạo thành
- của chất Ban Đầu Cô có ký hiệu và biểu
- thức như trên slide lưu ý trong quá
- trình tính toán các em cần quan tâm đến
- hệ số cân bằng của phương trình và cô có
- ví dụ sau Các mẹ quan sát xác định biến
- thiên A của phản ứng sau ở điều kiện
- chuẩn khi biết nhận tạo thành của các
- chất FeS2 ở trạng thái rắn Fe2O3 ở trạm
- này rắn và SO2 ở trạng thái khí như vậy
- chúng ta cùng Nhìn vào phương trình hóa
- học ta thấy rằng 4 FeS + 11 oxi tạo
- thành 2 Fe2O3 + 8so2 như vậy Chất đầu
- của chúng ta có FeS và O2 sản phẩm của
- chúng ta có Fe2O3 và SO2 áp dụng công
- thức ở trên slide ta sẽ lắp các số thứ
- tự vào để tính toán đầu tiên ta có tổng
- nhiệt giá thành của chất đầu là
- cô tính được bằng âm
- 711,6 kj thứ hai tổng như tạo thành sản
- phẩm là cô tính được là
- -4.025,4 kg như vậy ta sẽ lấy tổng nhiệt
- tạo thành của sản phẩm trừ đi tổng nhiệt
- tạo thành của chất đầu ta sẽ ra nhiệt
- tạo thành của phản ứng vậy ta có biến
- thiên etany của phản ứng sẽ bằng âm
- 3.313,8 kg tương tự như thế các em hãy
- làm cho cô câu hỏi tương tác sau từ số
- liệu bảng nhiệt tạo thành của các chất
- Hãy xác định biến thiên ethan bi chuẩn
- của phản ứng cháy ethan
- câu trả lời của các em rất chính xác
- tương tự như bài trước chúng ta cũng sẽ
- áp dụng công thức nhân tạo fh0 298
- cho rằng tổng như tạo thành sản phẩm trừ
- đi tẩm nhiệt tạo thành chất đầu Vậy thì
- ta cũng sẽ phải tính tổng nhiệt tạo
- thành chất đầu và tổng nhiệt tạo thành
- sản phẩm cô lần lượt tính được là âm
- 84,7 kg và âm
- 1644,4 kg như vậy
- etapi của phản ứng cô Tính ra được bằng
- âm
- 1559,7 kg cuối cùng bài của chúng ta sẽ
- đến với mục 4 tính biến thiên et của
- phản ứng theo năng lượng liên kết phản
- ứng hóa học của chúng ta là quá trình
- phá vỡ liên kết chất đầu và hình thành
- liên kết mới để tạo thành sản phẩm sự
- phá vỡ liên kết cần cung cấp năng lượng
- trong khi sự hình thành liên kết lại
- giải phóng năng lượng vậy biến thiên
- ethanbi của phản ứng mà các chất ở thể
- khí sẽ được tính bằng biến thiên erbi
- của phản ứng mà các chất đều ở thể khí
- bằng Hiệu số giữa tổng năng lượng
- chúng ta cũng có một liên kết cl nối với
- Cl cuối cùng là phân tử HCl ta có một
- liên kết h và Cl nhưng trong quá trình
- cân bằng thì ta có 2 phân tử HCl Vậy thì
- trên công thức của cô ở đây sẽ bằng năng
- lượng liên kết h và H cộng với năng
- lượng liên kết cl với Cl trừ đi 2 lần
- năng lượng liên kết của H với Cl và cô
- Tính toán được
- ethanbi của phản ứng sẽ bằng âm 185 kj
- câu hỏi tương tác của cô như sau cho
- biết năng lượng liên kết của phân tử
- Oxyz
- 494 kg/mon
- 945kg/mon và 607 kg/mon tính biến thiên
- ethanbi chuẩn của phản ứng N2 + O2 bằng
- 2 no
- câu trả lời của các em rất chính xác
- ta cũng áp dụng công thức trên slide của
- cô đúng không Thế thì ta sẽ lần lượt
- phân tích đầu tiên trong phân tử N2 có
- những liên kết nào và trong phân tử no
- có những liên kết nào chúng ta phải phân
- tích lần lượt từng phân tử Thế thì ta
- thấy được rằng là
- eth của cô sẽ tính bằng một liên kết N
- và n cộng 1 liên kết o với O trừ đi 2
- liên kết no Thế thì cô sẽ tính được
- trang bị của phản ứng bằng 225 kg trên
- mol Cô thấy rằng lớp chúng ta đã làm các
- bài tập tính toán rất tốt Cuối cùng
- chúng ta cần phải nhớ kiến thức của cả
- hai phần như sau
- phản ứng tỏa nhiệt là phản ứng xảy ra
- kèm theo sự truyền nhiệt từ chất phản
- ứng ra môi trường phản ứng thu nhiệt thì
- ngược lại là phản ứng xảy ra kèm theo sự
- truyền nhiệt từ môi trường vào chất phản
- ứng biến trên ethanbi của phản ứng là
- nhiệt lượng tỏa ra hay thu vào của một
- phản ứng ở một điều kiện xác định và
- chúng ta có thể xác định của phản ứng ở
- điều kiện chuẩn thông qua hai công thức
- 1 theo nhiệt tạo thành 2 theo năng lượng
- liên kết lưu ý chỉ ở các chất khí và các
- em hãy ghi các công thức tính biến thiên
- etan be ở trên slide vào nhớ rằng nhiệt
- tạo thành ta sẽ lấy sản phẩm trừ đi chất
- đầu năng lượng liên kết ta sẽ lấy chất
- đầu trừ đi sản phẩm bài học ngày hôm nay
- của chúng ta đã kết thúc tại đây Cảm ơn
- các em đã theo dõi các em hãy truy cập
- vào trang web online.vn để luyện tập và
- tương tác trực tiếp đừng quên nhấn theo
- dõi kênh hoặc trực tuyến online trên
- YouTube Xin chào và hẹn gặp lại các em
- trong các video bài giảng tiếp theo
K
Khách
Bạn có thể đăng câu hỏi về bài học này ở đây
Chưa có câu hỏi thảo luận nào về bài giao này
OLMc◯2022
