Một nguyên tổ R mà oxyde cao nhất của nó chứa 60% oxyde theo khối lượng. Hợp chất khí của R với hydrogen có tỉ khối hơi so với khí hydrogen bằng 17. Xác định R, công thức oxyde của R và công chức hợp chất khí của R với hydrogen.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Để giải quyết bài toán này, ta cần phân tích các thông tin đã cho:
-
Nguyên tố R là phi kim thuộc nhóm A trong bảng tuần hoàn. Điều này cho biết R có thể tạo ra oxyde cao nhất RO và hợp chất khí với hydrogen là HR.
-
Tỉ lệ giữa phần trăm nguyên tố R trong oxyde cao nhất và phần trăm R trong hợp chất khí với hydrogen bằng 0,5955. Điều này cho ta biết:
- Trong oxyde RO, phần trăm R là: M® / (M® + M(O)) = M® / (M® + 16)
- Trong hợp chất khí HR, phần trăm R là: M® / (M® + M(H)) = M® / (M® + 1)
- Vì tỉ lệ giữa hai phần trăm này bằng 0,5955, ta có: [M® / (M® + 16)] / [M® / (M® + 1)] = 0,5955
Giải phương trình trên, ta tìm được M® = 14, vậy R là nguyên tố Nitơ (N).
-
Cho 4,05 gam kim loại M chưa rõ hoá trị tác dụng hết với đơn chất R thì thu được 40,05 gam muối. Điều này cho ta biết:
- Lượng muối tạo thành là 40,05 - 4,05 = 36 gam.
- Vì muối tạo thành từ phản ứng giữa M và N2, công thức của muối sẽ là M(NH2)x với x là số hóa trị của M.
- Vì muối tạo thành từ 4,05 gam M và 36 gam muối, ta có: 4,05 / M(M) = 36 / [M(M) + x * M(NH2)]
- Với M(NH2) = M(N) + 2 * M(H) = 14 + 2 = 16
Giải phương trình trên với x = 2 (vì hầu hết các kim loại có hóa trị 2), ta tìm được M(M) = 27, vậy M là nguyên tố Nhôm (Al).
Vậy, nguyên tố R là Nitơ (N) và nguyên tố M là Nhôm (Al).

-
A và B cùng thuộc một nhóm trong bảng tuần hoàn và A có 6 electron ở lớp ngoài cùng, vậy A là Oxy (O) và B là Lưu huỳnh (S). Hợp chất của A với Hydrogen có phần trăm khối lượng Hydrogen bằng 5,88% nên hợp chất đó là nước (H2O).
-
B tạo với X (nhóm VIIA) một hợp chất XzB trong đó chiếm 81,61% khối lượng. Vì B là Lưu huỳnh (S) và X thuộc nhóm VIIA nên X có thể là Flo (F), Clo (Cl), Brom (Br), Iot (I) hoặc Astatin (At). Tuy nhiên, chỉ có Clo (Cl) tạo ra hợp chất với Lưu huỳnh (S) có phần trăm khối lượng là 81,61% (hợp chất đó là SCl2).
-
Phân tử XY có tổng diện tích hạt nhân là 26 và X và Y cùng một chu kì ở hai nhóm liên tiếp. Vậy X có thể là Nhôm (Al) và Y là Silic (Si) vì tổng số hạt nhân của chúng là 26 và chúng cùng thuộc chu kì 3 trong bảng tuần hoàn. Vậy công thức phân tử là AlSi.

Gọi CT chung của 2 muối là NaZ.
Ta có: \(n_{NaZ}=\dfrac{31,84}{23+M_Z}\left(mol\right)\)
\(n_{AgZ}=\dfrac{57,34}{108+M_Z}\left(mol\right)\)
BTNT Z, có: \(n_{NaZ}=n_{AgZ}\Rightarrow\dfrac{31,84}{23+M_Z}=\dfrac{57,34}{108+M_Z}\)
\(\Rightarrow M_Z\approx83,133\left(g/mol\right)\)
Mà: X, Y thuộc 2 chu kì kế tiếp của nhóm VIIA.
→ Br, I

a, \(n_{H_2}=0,09\left(mol\right)\)
BT e, có: 2nX = 2nH2 ⇒ nX = 0,09 (mol)
\(\Rightarrow\overline{M}_X=\dfrac{2,64}{0,09}=29,33\left(g/mol\right)\)
Mà: A, B thuộc 2 chu kì liên tiếp.
→ Mg và Ca.
Ta có: \(\left\{{}\begin{matrix}24n_{Mg}+40n_{Ca}=2,64\\2n_{Mg}+2n_{Ca}=0,09.2\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}n_{Mg}=0,06\left(mol\right)\\n_{Ca}=0,03\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Mg}=\dfrac{0,06.24}{2,64}.100\%\approx54,55\%\\\%m_{Ca}\approx45,45\%\end{matrix}\right.\)
b, BTNT H, có: \(n_{H_2SO_4}=n_{H_2}=0,09\left(mol\right)\Rightarrow V_{ddH_2SO_4}=\dfrac{0,09}{2}=0,045\left(l\right)\)
BTNT Mg: nMgSO4 = nMg = 0,06 (mol)
\(\Rightarrow C_{M_{MgSO_4}}=\dfrac{0,06}{0,045}=\dfrac{4}{3}\left(M\right)\)

Gọi chung 2 KL cần tìm là A.
PT: \(2A+2HCl\rightarrow2ACl+H_2\)
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
Theo PT: \(n_A=2n_{H_2}=0,6\left(mol\right)\)
\(\Rightarrow\overline{M}_A=\dfrac{18,6}{0,6}=31\left(g/mol\right)\)
Mà: 2 KL ở 2 chu kì kế tiếp nhau.
→ Na và K

a, Ta có: P + N + E = 34
Mà: P = E (Do nguyên tử trung hòa về điện.)
⇒ 2P + N = 34 (1)
Theo đề, số hạt mang điện nhiều hơn số hạt không mang điện là 10.
⇒ 2P - N = 10 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}P=E=11=Z\\N=12\end{matrix}\right.\) ⇒ A = 11 + 12 = 23
→ KH: \(^{23}_{11}X\)
b, Cấu hình e: 1s22s22p63s1
Cấu hình e theo orbital:
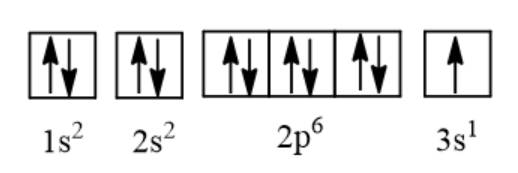
c, X có 1 e hóa trị → tính kim loại
d, - Z = 11 → ô số 11
- Có 3 lớp e → chu kỳ 3
- e cuối cùng phân bố ở phân lớp s, có 1 e hóa trị → nhóm IA
Vậy: X thuộc ô số 11, chu kỳ 3, nhóm IA
Đầu tiên, ta xác định nguyên tố R. Theo đề bài, oxyde cao nhất của R chứa 60% oxy theo khối lượng. Do đó, khối lượng của R chiếm 40%. Ta có công thức tính khối lượng nguyên tố trong hợp chất như sau:
MR=M0×4060
Trong đó, M0 là khối lượng phân tử của Oxy (16 đvC). Thay số vào công thức trên, ta được:
MR=16×4060=10.67≈11
Vậy nguyên tố R có khối lượng phân tử gần với 11 đvC, nên R có thể là nguyên tố Natri (Na).
Tiếp theo, ta xác định công thức của oxyde cao nhất của R. Vì oxyde cao nhất của Natri là Na2O, nên công thức của oxyde là Na2O.
Cuối cùng, ta xác định công thức của hợp chất khí của R với hydrogen. Theo đề bài, tỉ khối hơi của hợp chất này so với khí hydrogen là 17. Do đó, khối lượng phân tử của hợp chất này là 17 lần khối lượng phân tử của hydrogen. Ta có công thức tính khối lượng phân tử của hợp chất như sau:
MRH=17×MH
Trong đó, MH là khối lượng phân tử của Hydrogen (2 đvC). Thay số vào công thức trên, ta được:
MRH=17×2=34
Vì khối lượng phân tử của Natri là 23 đvC và khối lượng phân tử của Hydrogen là 1 đvC, nên công thức của hợp chất khí của R với hydrogen là NaH.
Vậy, R là Natri (Na), công thức oxyde của R là Na2O và công thức hợp chất khí của R với hydrogen là NaH.