Giúp em vs ạ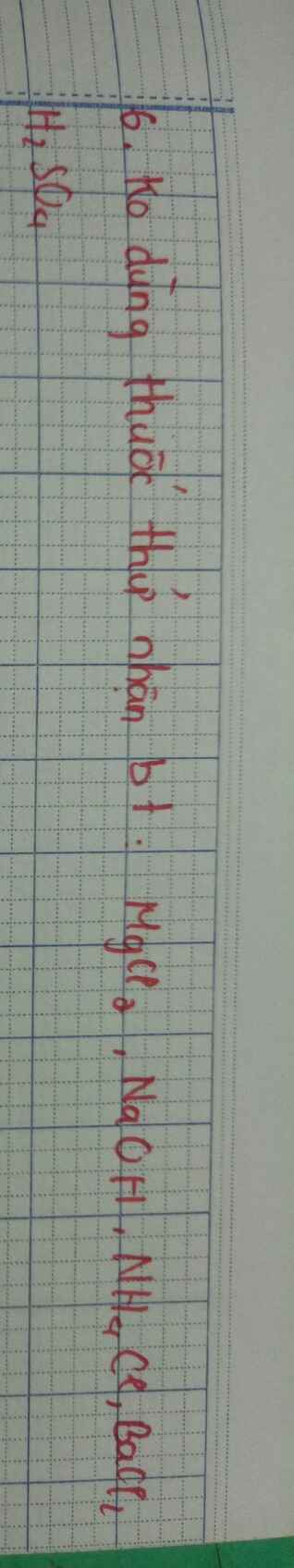
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


PTHH:
`Mg + CuSO_4 -> MgSO_4 + Cu(1)`
`Mg + FeSO_4 -> MgSO_4 + Fe(2)`
`TN_1:` dd chứa 3 muối
`=>` Ở Phản ứng (1) `CuSO_4` dư
Theo PT (1): `n_{CuSO_4(pư)} = n_{Mg} = c (mol)`
`=> a > c`
`TN_2:` dd chứa 2 muối
`=>` Ở phản ứng (1) CuSO4, có thể xảy ra phản ứng (2) và FeSO4 dư
Theo (1): `n_{Mg(pư)} = n_{CuSO_4} = a (mol)`
`=>` \(c\ge a\)
`=> n_{Mg(dư)} = c - a (mol)`
Theo (2): `n_{FeSO_4(pư)} = n_{Mg (dư)} = c - a (mol)`
`=> n_{FeSO_4(dư)} = b - (c - a) = a + b - c (mol)`
`=> a + b - c > 0 <=> a + b > c`
`TN_3:` dd sau phản ứng chứa 1 muối
`=>` Mg dư hoặc đủ, `CuSO_4, FeSO_4` hết
Theo (1), (2): `n_{Mg(pư)} = n_{CuSO_4} + n_{FeSO_4} = a + b (mol)`
`=>` \(c\ge a+b\)

$M : Al ; B : AlCl_3 ; C : NaAlO_2 ; D : Al(OH)_3 ; X : KOH ; Y : CO_2 ; Z : H_2O$
$E : Al_2O_3$
$2Al + 6HCl \to 2AlCl_3 + 3H_2$
$2Al + 2NaOH + 2H_2O \to 2NaAlO_2 + 3H_2$
$AlCl_3 + 3KOH \to Al(OH)_3 + 3KCl$
$NaAlO_2 + CO_2 + 2H_2O \to Al(OH)_3 + NaHCO_3$
$2Al(OH)_3 \xrightarrow{t^o} Al_2O_3 + 3H_2O$
$2Al_2O_3 \xrightarrow{dpnc} 4Al + 3O_2$

$n_{Al_2(SO_4)_3} = \dfrac{3,42}{342} = 0,01(mol)$
$n_{Al(OH)_3} = \dfrac{0,78}{78} = 0,01(mol)$
TH1 : $Al_2(SO_4)_3$ dư
$Al_2(SO_4)_3 + 6NaOH \to 2Al(OH)_3 + 3Na_2SO_4(1)$
Theo PTHH :
$n_{NaOH} = 3n_{Al(OH)_3} = 0,03(mol)$
$C_{M_{NaOH}} = \dfrac{0,03}{0,05} = 0,6M$
TH2 : Kết tủa bị hoà tan
$Al(OH)_3 + NaOH \to NaAlO_2 + 2H_2O$
Theo PTHH :
$n_{NaOH(1)} = 6n_{Al_2(SO_4)_3} = 0,06(mol)$
$n_{Al(OH)_3(1)} = 2n_{Al_2(SO_4)_3} = 0,02(mol)$
$\Rightarrow n_{NaOH(2)} = n_{Al(OH)_3(2)} = 0,02 - 0,01 = 0,01(mol)$
$\Rightarrow n_{NaOH} = 0,06 + 0,01 = 0,07(mol)$
$C_{M_{NaOH}} = \dfrac{0,07}{0,05} = 1,4M$

Câu 91:
A: Ca(OH)2
B: CaCl2
C: Ca(NO3)2
D: Ca3(PO4)2
E: H2O
G: HCl
H: AgNO3
I: K2CO3
K: H3PO4
L: HNO3
Viết các PTHH lần lượt từ trái qua phải, trên xuống dưới bạn nhé
(1) \(CaCO_3\xrightarrow[]{t^o}CaO+CO_2\uparrow\)
(2) \(CaO+2HCl\rightarrow CaCl_2+H_2O\)
(3) \(CaCl_2+2AgNO_3\rightarrow2AgCl\downarrow+Ca\left(NO_3\right)_2\)
(4) \(Ca\left(NO_3\right)_2+K_2CO_3\rightarrow CaCO_3\downarrow+2KNO_3\)
(5) \(3CaCO_3+2H_3PO_4\rightarrow Ca_3\left(PO_4\right)_2\downarrow+3CO_2\uparrow+3H_2O\)
(6) \(Ca_3\left(PO_4\right)_2+6HNO_3\rightarrow3Ca\left(NO_3\right)_2+2H_3PO_4\)
Câu 92:
A: SO3
B: BaS
(1) \(S+O_2\xrightarrow[]{t^o}SO_2\)
(2) \(2SO_2+O_2\xrightarrow[V_2O_5]{t^o}2SO_3\)
(3) \(SO_3+H_2O\rightarrow H_2SO_4\)
(4) \(H_2SO_4+BaCl_2\rightarrow BaSO_4\downarrow+2HCl\)
(5) \(S+Ba\xrightarrow[]{t^o}BaS\)
(6) \(BaS+H_2SO_4\rightarrow BaSO_4\downarrow+H_2S\uparrow\)
(1): \(S+O_2\rightarrow SO_2\)
(2)\(SO_2+H_2O\rightarrow H_2SO_3\)
(3): \(2H_2SO_3+O_2\rightarrow2H_2SO_4\)
(4): \(H_2SO_4+BaCl_2\rightarrow BaSO_4+HCl\)

97.
(1) \(Cu+2AgNO_3\rightarrow Cu\left(NO_3\right)_2+2Ag\downarrow\)
(2) \(CuO+2HNO_3\rightarrow Cu\left(NO_3\right)_2+H_2O\)
(3) \(2Cu\left(NO_3\right)_2\xrightarrow[]{t^o}2CuO+4NO_2\uparrow+O_2\uparrow\)
(4) \(Cu\left(NO_3\right)_2+2KOH\rightarrow Cu\left(OH\right)_2\downarrow+2KNO_3\)
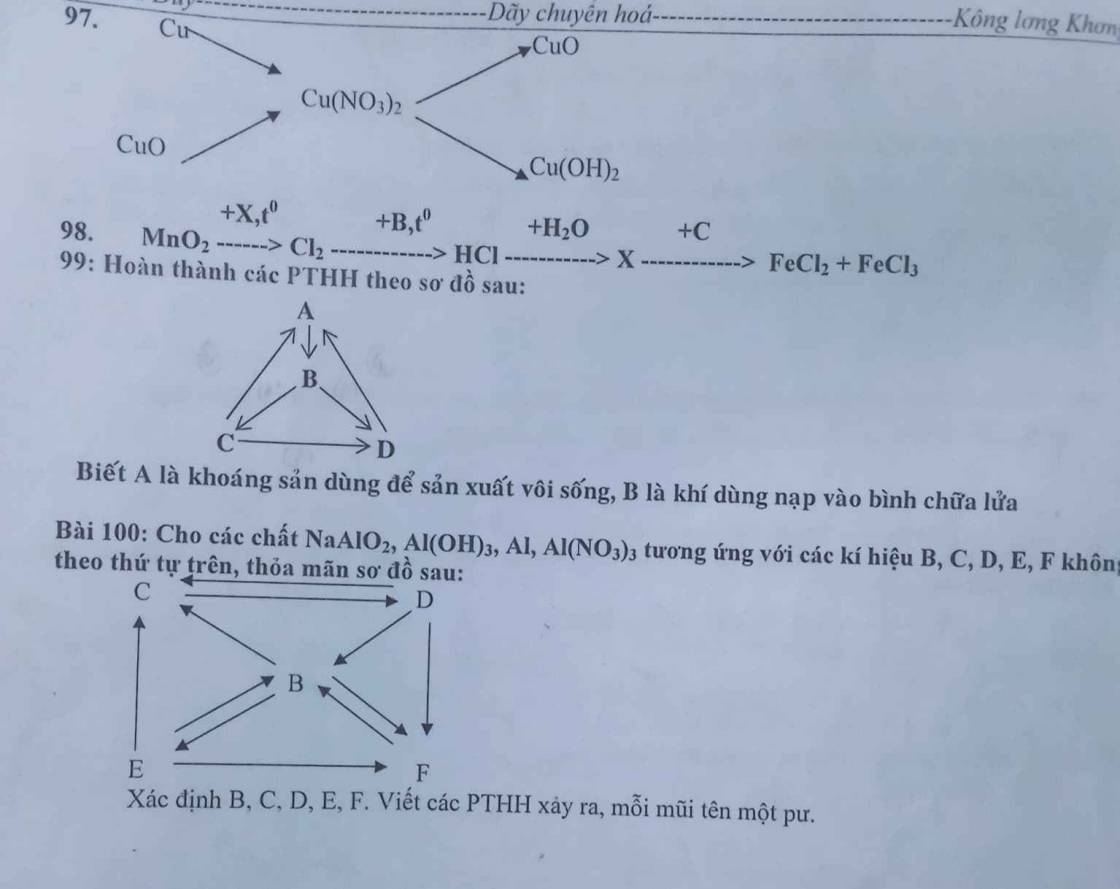
98.
X: dd HCl
B: H2
C: Fe3O4
Các PT lần lượt từ trái qua phải nhé
(1) \(MnO_2+4HCl_đ\xrightarrow[]{t^o}MnCl_2+Cl_2\uparrow+2H_2O\)
(2) \(Cl_2+H_2\xrightarrow[]{t^o}2HCl\)
(3) Khí HCl tác dụng với nước thu được dd HCl (không có PT)
(4) \(8HCl+Fe_3O_4\rightarrow FeCl_2+2FeCl_3+4H_2O\)
99.
A: CaCO3
B: Ca(HCO3)2
C: CO2
D: NaHCO3
A -> B: \(CaCO_3+CO_2+H_2O\rightarrow Ca\left(HCO_3\right)_2\)
B -> C: \(Ca\left(HCO_3\right)_2\xrightarrow[]{t^o}CaCO_3\downarrow+CO_2\uparrow+H_2O\)
C -> D: \(CO_2+NaOH\rightarrow NaHCO_3\)
B -> D: \(Ca\left(HCO_3\right)_2+Na_2CO_3\rightarrow CaCO_3\downarrow+2NaHCO_3\)
C -> A: \(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3\downarrow+H_2O\)
D -> A: \(2NaHCO_3+Ca\left(OH\right)_2\rightarrow CaCO_3\downarrow+Na_2CO_3+2H_2O\)
100. Đề chỉ cho 4 chất NaAlO2, Al(OH)3, Al, Al(NO3)3 nhưng tại sao lại có tới 5 kí hiệu B, C, D, E, F bạn nhỉ?

\(Đặt:n_{CO\left(p.ứ\right)}=a\left(mol\right)\left(a>0\right)\\PTHH:FeO+CO\rightarrow \left(t^o\right)Fe+CO_2\\ Fe_2O_3+3CO\rightarrow\left(t^o\right)2Fe+3CO_2\\ hh.khí:CO\left(dư\right),CO_2\\ n_{CO_2}=n_{CO\left(p.ứ\right)}=a\left(mol\right)\\ m_{hh.khí}=18\left(g\right)\\ \Leftrightarrow28.\left(0,5-a\right)+44a=18\\ \Leftrightarrow a=0,25\left(mol\right)\\ \Rightarrow X:\%m_{CO_2}=\dfrac{0,25.44}{18}.100\%\approx61,111\%\\ \Rightarrow\%m_{CO\left(dư\right)}\approx38,889\%\\ b,m_{Fe}=m_{oxit}+m_{CO\left(p.ứ\right)}-m_{CO_2}=15,2+0,25.28-0,25.44=11,2\left(g\right)\\ Đặt:n_{FeO}=t\left(mol\right);n_{Fe_2O_3}=n\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}72t+160n=15,2\\t+3n=0,25\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}t=0,1\\n=0,05\end{matrix}\right.\\ \Rightarrow m_{FeO}=72t=7,2\left(g\right);m_{Fe_2O_3}=160n=8\left(g\right)\)

a)
$3Cu + 8HNO_3 \to 3Cu(NO_3)_2 + 2NO + 4H_2O$
$Fe_3O_4 + 10HNO_3 \to 3Fe(NO_3)_3 + NO + 5H_2O$
$2Fe(NO_3)_3 + Cu \to Cu(NO_3)_2 + 2Fe(NO_3)_2$
b) $n_{NO} = \dfrac{1,68}{22,4} = 0,075(mol)$
Gọi $n_{Cu\ pư} = a(mol) ; n_{Fe_3O_4} = b(mol)$
$\Rightarrow 64a + 232b + 1,2 = 30,6(1)$
Bảo toàn electron : $2n_{Cu\ pư} = 2n_{Fe_3O_4} + 3n_{NO}$
$\Rightarrow 2a = 2b + 0,075.3(2)$
Từ (1)(2) suy ra a = 0,1875 ; b = 0,075
$n_{Fe(NO_3)_2} = 3n_{Fe_3O_4} = 0,225(mol)$
$n_{Cu(NO_3)_2} = n_{Cu\ pư} = 0,1875(mol)$
Bảo toàn N : $n_{HNO_3} = 2n_{Fe(NO_3)_2} + 2n_{Cu(NO_3)_2} + n_{NO} = 0,9(mol)$
$C_{M_{HNO_3}} = \dfrac{0,9}{0,5} = 1,8M$
\(a,\) \(3Cu+8HNO_3\rightarrow Cu\left(NO_3\right)_2+2NO+4H_2O\) \(\left(1\right)\)
\(Molx\rightarrow\dfrac{8x}{3}\rightarrow\dfrac{2x}{3}\)
\(3Fe_3O_4+28HNO_3\rightarrow9Fe\left(NO_3\right)_3+NO+14H_2O\) \(\left(2\right)\)
\(Moly\rightarrow\dfrac{28y}{3}\rightarrow3y\rightarrow\dfrac{y}{3}\)
\(2Fe\left(NO_3\right)_3+Cu\rightarrow Cu\left(NO_3\right)_2+2Fe\left(NO_3\right)_2\) \(\left(3\right)\)
Có 1,2 gam kim loại ko tan nên \(Cu\) dư chuyển \(Fe^{3+}\) hết thành \(Fe^{2+}\)
\(b,\) Gọi số mol \(Cu\) phản ứng 1 là x mol, số mol \(Fe_3O_4\) là y mol \(nNO=\dfrac{1,68}{22,4}=0,075mol\)
Theo PT và ĐB ta có
\(\left\{{}\begin{matrix}\dfrac{2x}{3}+\dfrac{y}{3}=0,075\\64\left(x+\dfrac{3y}{2}\right)+232y=30,6-1,2\\\end{matrix}\right.\) ↔ \(\left\{{}\begin{matrix}x=0,075\\y=0,075\end{matrix}\right.\)
Số mol \(HNO_3\) đã dùng là \(\left(\dfrac{8x}{3}+\dfrac{28y}{3}\right)=0,9mol\)
\(\Rightarrow CM\) \(HNO_3=0,9:0,5=1,8M\)
\(#Hoctotnha\)


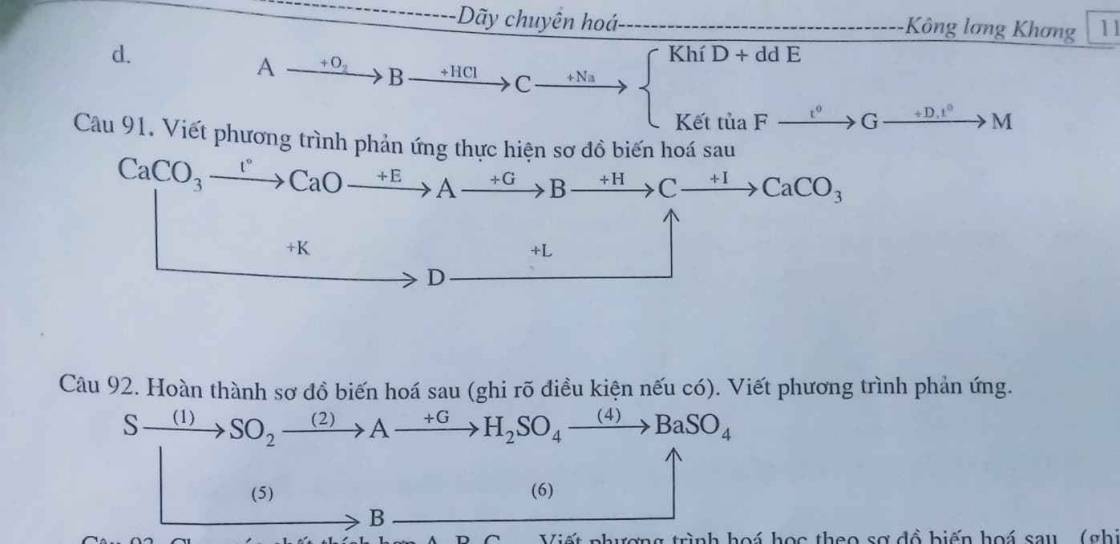
Trích mẫu thử
Cho các mẫu thử tác dụng lần lượt với nhau :
Mẫu thử nào tạo 1 khí 1 kết tủa là $NaOH$
Mẫu thử nào tạo 1 khí là $NH_4Cl$
Mẫu thử nào tạo 1 kết tủa là $MgCl_2,BaCl_2,H_2SO_4$
$NH_4Cl + NaOH \to NH_3 + NaCl + H_2O$
$MgCl_2 + 2NaOH \to Mg(OH)_2 + 2NaCl$
$BaCl_2 + H_2SO_4 \to BaSO_4 + 2HCl$
Cho dung dịch $NaOH$ mới nhận được cho vào hai mẫu thử trên :
- mẫu thử nào tạo kết tủa là $MgCl_2$
Nhỏ một ít dung dịch $NaOH$ vào hai mẫu thử còn, sau đó thêm dung dịch $MgCl_2$ vào
- mẫu thử không hiện tượng là $H_2SO_4$ :
$2NaOH + H_2SO_4 \to Na_2SO_4 + 2H_2O$
- mẫu thử xuất hiện kết tủa trắng là $BaCl_2$
- Trích mẫu thử, có đánh số thứ tự
- Cho lần lượt các mẫu thử này tác dụng với các mẫu thử còn lại, ta có kết quả ở bảng sau:
Từ kết quả bảng trên, ta rút ra kết quả:
+ Mẫu thử tạo một lần kết tủa trắng: `MgCl_2, BaCl_2, H_2SO_4 (1)`
+ Mẫu thử tạo một lần kết tủa trắng, một khí không màu, mùi khai: `NaOH`
+ Mẫu thử tạo một lần khí không màu, mùi khai: `NH_4Cl`
`NaOH + NH_4Cl -> NaCl + NH_3 + H_2O`
`2NaOH + MgCl_2 -> Mg(OH)_2 + 2NaCl`
`2NaOH + H_2SO_4 -> Na_2SO_4 + 2H_2O`
`BaCl_2 + H_2SO_4 -> BaSO_4 + 2HCl`
- Cho dd `NaOH` vào các mẫu thử (1), nếu thấy:
+ Mẫu thử có kết tủa trắng: `MgCl_2`
+ Mẫu thử không có hiện tượng: `BaCl_2, H_2SO_4 (2)`
- Vớt kết tủa `Mg(OH)_2` cho vào các mẫu thử `(2)`, nếu thấy:
+ Mẫu thử làm kết tủa tan: `H_2SO_4`
`Mg(OH)_2 + H_2SO_4 -> MgSO_4 + 2H_2O`
+ Mẫu thử không hiện tượng: `BaCl_2`
- Dán nhãn