Cho `48,5g` hỗn hợp gồm `CuO` và `ZnO` cho phản ứng với `400ml` dung dịch `HCl` có nồng độ `3M` xảy ra hoàn toàn
`a. PTHH?`
`b.` Khối lượng Oxit trong hỗn hợp?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



Sửa đề: 7,2% → 7,3%
a, \(Fe+2HCl\rightarrow FeCl_2+H_2\)
b, \(n_{Fe}=\dfrac{2,8}{56}=0,05\left(mol\right)\)
\(m_{HCl}=100.7,3\%=7,3\left(g\right)\Rightarrow n_{HCl}=\dfrac{7,3}{36,5}=0,2\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,05}{1}< \dfrac{0,2}{2}\), ta được HCl dư.
Theo PT: \(\left\{{}\begin{matrix}n_{FeCl_2}=n_{H_2}=n_{Fe}=0,05\left(mol\right)\\n_{HCl\left(pư\right)}=2n_{Fe}=0,1\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow m_{FeCl_2}=0,05.127=6,35\left(g\right)\)
\(m_{H_2}=0,05.2=0,1\left(g\right)\)
\(n_{HCl\left(dư\right)}=0,2-0,1=0,1\left(mol\right)\Rightarrow m_{HCl\left(dư\right)}=0,1.36,5=3,65\left(g\right)\)

\(n_{Zn}=0,1\left(mol\right)\)
\(n_{Mg}=0,2\left(mol\right)\)
\(n_{CuSO_4}=0,2.0,5=0,1\left(mol\right)\)
\(n_{AgNO_3}=0,2.0,3=0,06\left(mol\right)\)
\(Mg+2Ag^+\rightarrow Mg^{2+}+2Ag\)
0,03____0,06___________0,06 (mol)
\(Mg+Cu^{2+}\rightarrow Mg^{2+}+Cu\)
0,1_____0,1____________0,1 (mol)
→ A gồm: Ag: 0,06 (mol), Cu: 0,1 (mol), Zn: 0,1 (mol), Mg: 0,2 - 0,03 - 0,1 = 0,07 (mol)
⇒ mA = 21,06 (g)

\(n_{HCl}=0,4\left(mol\right)\)
\(n_{CuSO_4}=0,16\left(mol\right)\)
Hỗn hợp KL gồm Cu và Fe dư.
BTNT H, có: nH2 = 1/2nHCl = 0,2 (mol)
\(\Rightarrow V_{H_2}=0,2.22,4=4,48\left(l\right)=x\)
BTNT Cl: nFeCl2 = 1/2nHCl = 0,2 (mol)
BTNT S, có: nFeSO4 = nCuSO4 = 0,16 (mol)
BTKL, có: mFe + mHCl + mCuSO4 = mFeCl2 + mFeSO4 + mH2 + m hh KL
⇒ a + 14,6 + 25,6 = 0,2.127 + 0,16.152 + 0,2.2 + 0,7a
⇒ a ≃ 33,067 (g)

1. Ta có: \(n_{Fe}=\dfrac{5,6}{56}=0,1\left(mol\right)\)
PT: \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
a, \(n_{FeSO_4}=n_{Fe}=0,1\left(mol\right)\Rightarrow m_{FeSO_4}=0,1.152=15,2\left(g\right)\)
b, \(n_{H_2SO_4}=n_{Fe}=0,1\left(mol\right)\Rightarrow C_{M_{FeSO_4}}=\dfrac{0,1}{0,5}=0,2\left(M\right)\)
2. \(n_{Al}=\dfrac{2,7}{27}=0,1\left(mol\right)\)
PT: \(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
a, \(n_{Al_2\left(SO_4\right)_3}=\dfrac{1}{2}n_{Al}=0,05\left(mol\right)\)
\(\Rightarrow m_{Al_2\left(SO_4\right)_3}=0,05.342=17,1\left(g\right)\)
b, \(n_{H_2SO_4}=\dfrac{3}{2}n_{Al}=0,15\left(mol\right)\)
\(\Rightarrow m_{H_2SO_4}=0,15.98=14,7\left(g\right)\)
\(\Rightarrow a=C\%_{H_2SO_4}=\dfrac{14,7}{98}.100\%=15\%\)

a)
Khi để lâu trong không khí thì chuyển sang màu vàng nâu => Sản phẩm có sự tạo thành nước Bromine
4HBr + O2 → 2Br2 + 2H2O
b)
Hydrobromic acid được bảo quản trong các lọ tối màu, nếu để nơi có ánh sáng hoặc trong bình sáng thì khí oxygen sẽ được tạo ra do thành phần của acid HBrO
=> HBr bị oxi hóa bởi oxygen

\(4H\mathop {Cl}\limits^{ - 1} {\text{ }} + {\text{ }}\mathop {Mn}\limits^{ + 4} {O_2} \to {\mathop {Cl}\limits^0 _2} + {\text{ }}\mathop {Mn}\limits^{ + 2} C{l_2} + {\text{ }}2{H_2}O\)
a)
\(\mathop {Mn}\limits^{ + 4} + 2e \to \mathop {Mn}\limits^{ + 2} \) => MnO2 là chất oxi hóa
\(\mathop {2Cl}\limits^{ - 1} \to \mathop {C{l_2}}\limits^0 + 2e\) => HCl là chất khử
b) HI có tính khử mạnh hơn HCl
=> HI có thể phản ứng được với MnO2
4HI + MnO2 → I2 + MnI2 + 2H2O

- Trích mẫu thử.
- Nhỏ vài giọt từng mẫu thử vào giấy quỳ tím.
+ Quỳ hóa xanh: NaOH
+ Quỳ hóa đỏ: HCl
+ Quỳ không đổi màu: NaCl, Na2SO4 (1)
- Cho mẫu thử nhóm (1) pư với dd BaCl2
+ Có tủa trắng: Na2SO4
PT: \(BaCl_2+Na_2SO_4\rightarrow2NaCl+BaSO_4\)
+ Không hiện tượng: NaCl
- Dán nhãn.

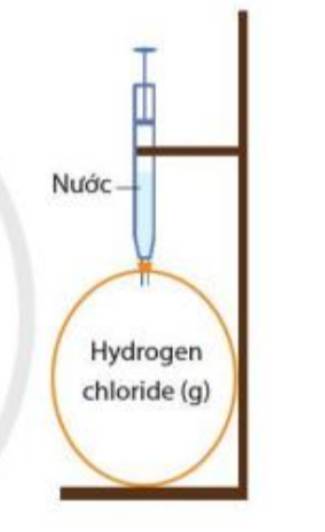
Khí hydrogen chloride tan nhiều trong nước tạo thành dung dịch hydrochloric acid
=> Khi bơm nước vào, khí hydrogen chloride bị hòa tan hết
=> Quả bóng bị xẹp vào

Nhiệt độ sôi của hydrogen bromide cao hơn nhiệt độ sôi của hydrogen chloride được giải thích như sau:
+ Khối lượng phân tử HBr (81) cao hơn khối lượng phân tử HCl (36,5)
+ Br có bán kính nguyên tử lớn, có nhiều electron hơn Cl => Tăng khả năng lưỡng cực HX => Làm tăng tương tác van der Waals giữa các phân tử