Dung dịch A chứa Na+ 0,1 mol , Mg2+ 0,05 mol , SO42- 0,04 mol còn lại là Cl- . Tính khối lượng muối trong dung dịch
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Ta có: \(\left\{{}\begin{matrix}n_{H^+}=n_{HNO_3}=\dfrac{20.31,5\%}{63}=0,1\left(mol\right)\\n_{OH^-}=2n_{Ba\left(OH\right)_2}=0,5.0,2.2=0,2\left(mol\right)\end{matrix}\right.\)
PTHH: \(H^++OH^-\rightarrow H_2O\)
0,1--->0,1
`=>` \(n_{OH^-\left(dư\right)}=0,2-0,1=0,1\left(mol\right)\)
Đề thiếu Vdd HNO3 nên không tính được Vdd sau phản ứng , không tìm được pH

\(n_{H_2SO_4}=\dfrac{2,45}{98}=0,025\left(mol\right)\Rightarrow n_{H^+}=0,025\cdot2=0,05\left(mol\right)\)
\(n_{NaOH}=0,3\cdot0,15=0,045=n_{OH^-}\)
PT ion RG: \(H^++OH^-\rightarrow H_2O\)
0,045 ← 0,045
\(\Rightarrow n_{H^+\text{ (dư)}}=0,05-0,045=0,005\left(mol\right)\)
\(\Rightarrow\left[H^+\right]_{\text{(dư)}}=\dfrac{0,005}{0,35+0,15}=0,01\left(M\right) \)
\(\Rightarrow pH=-\log0,01=2\)


`(1) 4NO_2 + 2H_2O + O_2 -> 4HNO_3`
`(2) HNO_3 + CuO -> Cu(NO_3)_2 + H_2O`
`(3) Cu(NO_3)_2 + 2KOH -> Cu(OH)_2 + 2KNO_3`
`(4) Cu(OH)_2 + 2HNO_3 -> Cu(NO_3)_2 + 2H_2O`
$(5) 2Cu(NO_3)_2 \xrightarrow{t^o} 2CuO + 4NO_2 + O_2$
$(6) CuO + CO \xrightarrow{t^o} Cu + CO_2$

Câu 2:
a)
`2NH_3 + 3Cl_2 -> N_2 + 6HCl`
`NH_3 + HCl -> NH_4Cl`
$3CuO + 2NH_3 \xrightarrow{t^o} 3Cu + N_2 + 3H_2O$
$2NH_3 + 3O_2 \xrightarrow{t^o} 2N_2 + 6H_2O$
`3NH_3 + H_3PO_4 -> (NH_4)_3PO_4`
`NH_3 + CH_3COOH -> CH_3COONH_4`
b)
`- AlCl_3:`
`AlCl_3 + 3NH_3 + 3H_2O -> Al(OH)_3 + 3NH_4Cl`
`Al^{3+} + 3NH_3 + 3H_2O -> Al(OH)_3 + 3NH_4^{+}`
`- Cu(NO_3)_2:`
`Cu(NO_3)_2 + 2NH_3 + 2H_2O -> Cu(OH)_2 + 2NH_4NO_3`
`Cu(OH)_2 + 4NH_3 -> [Cu(NH_3)_4](OH)_2`
`Cu^{2+} + 2NH_3 + 2H_2O -> Cu(OH)_2 + NH_4^{+}`
`Cu(OH)_2 + 4NH_3 -> [Cu(NH_3)_4]^{2+} + 2OH^{-}`
`- H_2SO_4:`
`2NH_3 + H_2SO_4 -> (NH_4)_2SO_4`
`NH_3 + H^{+} -> NH_4^{+}`
`- FeSO_4:`
`Fe^{2+} + 2NH_3 + 2H_2O -> Fe(OH)_2 + 2NH_4^{+}`
Câu 3:
a)
`(1) Al_2(SO_4)_3 + 6NH_3 + 6H_2O -> 2Al(OH)_3 + 3(NH_4)_2SO_4`
$(2) (NH_4)_2SO_4 \xrightarrow{t^o} 2NH_3 + H_2SO_4$
`(3) Zn(NO_3)_2 + 2NH_3 + 2H_2O -> Zn(OH)_2 + 2NH_4NO_3`
`(4) Zn(OH)_2 + 4NH_3 -> [Zn(NH_3)_4](OH)_2`
b)
$(1)NH_4NO_2 \xrightarrow{t^o} N_2 + 2H_2O$
$(2) N_2 + 3H_2 \xrightarrow{t^o, p, xt} 2NH_3$
`(3) 2NH_3 + H_2SO_4 -> (NH_4)_2SO_4`
`(4)(NH_4)_2SO_4 + Ba(NO_3)_2 -> BaSO_4 + 2NH_4NO_3`
`(5)NH_4NO_3 + KOH -> KNO_3 + NH_3 + H_2O`
`(6) 2NH_3 + 3Cl_2 -> N_2 + 6HCl`
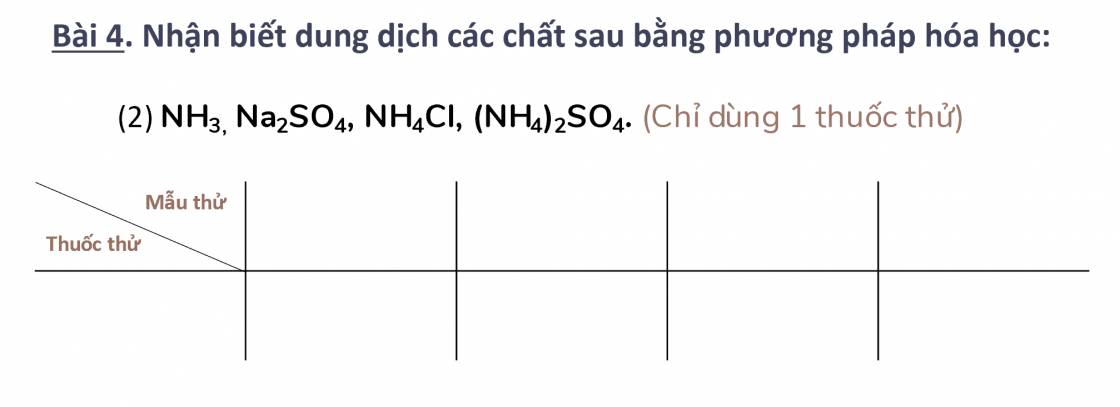
Câu 4:
a) $3CuO + 2NH_3 \xrightarrow{t^o} 3Cu + N_2 + 3H_2O$
b) `NH_3 + HCl -> NH_4Cl`
`NH_4NO_3 + KOH -> KNO_3 + NH_3 + H_2O`
c) `Zn(OH)_2 + 4NH_3 -> [Zn(NH_3)_4](OH)_2`
Câu 5:
a)
| `NaNO_3` | `NH_4NO_3` | `Fe(NO_3)_3` | `Mg(NO_3)_2` | `Al(NO_3)_3` | |
| dd `KOH` dư | `-` Không hiện tượng | `-` \(\uparrow\) không màu, mùi khai | `-` \(\downarrow\) nâu đỏ | `-` \(\downarrow\) trắng | `-` \(\downarrow\) trắng, sau đó tan |
`NH_4NO_3 + KOH -> KNO_3 + NH_3 + H_2O`
`Fe(NO_3)_3 + 3KOH -> Fe(OH)_3 + 3KNO_3`
`Mg(NO_3)_2 + 2KOH -> Mg(OH)_2 + 2KNO_3`
`Al(NO_3)_3 + 3KOH -> Al(OH)_3 + 3KNO_3`
`Al(OH)_3 + KOH -> KAlO_2 + 2H_2O`
b)
| `CuCl_2` | `K_2SO_3` | `(NH_4)_2SO_4` | `Al(NO_3)_3` | `Na_2S` | |
| dd `HCl` | `-` Không hiện tượng | `-` \(\uparrow\) không màu, mùi hắc | `-` Không hiện tượng | `-` Không hiện tượng | `-` \(\uparrow\) không màu, mùi trứng thối |
| dd `KOH` dư | `-` \(\downarrow\) xanh lơ | `-` \(\uparrow\) không màu, mùi khai | `-` \(\downarrow\) trắng, sau đó tan |
`K_2SO_3 + 2HCl -> 2KCl + SO_2 + H_2O`
`Na_2S + 2HCl -> 2NaCl + H_2S`
`CuCl_2 + 2KOH -> Cu(OH)_2 + 2KCl`
`(NH_4)_2SO_4 + 2KOH -> K_2SO_4 + 2NH_3 + 2H_2O`
`Al(NO_3)_3 + 3KOH -> Al(OH)_3 + 3KNO_3`
`Al(OH)_3 + KOH -> KAlO_2 + 2H_2O`
c)
| `Mg(NO_3)_2` | `K_2S` | `(NH_4)_2SO_4` | `NH_4NO_3` | `BaCl_2` | |
| dd `H_2SO_4` | `-` Không hiện tượng | `-` \(\uparrow\) không màu, mùi trứng thối | `-` Không hiện tượng | `-` Không hiện tượng | `-` \(\downarrow\) trắng |
| dd `Ba(OH)_2` | `-` \(\downarrow\) trắng | `-` \(\downarrow\) trắng, \(\uparrow\) không màu, mùi trứng thối | `-` \(\uparrow\) không màu, mùi trứng thối |
`K_2S + H_2SO_4 -> K_2SO_4 + H_2S`
`BaCl_2 + H_2SO_4 -> BaSO_4 + 2HCl`
`Ba(OH)_2 + Mg(NO_3)_2 -> Mg(OH)_2 + Ba(NO_3)_2`
`(NH_4)_2SO_4 + Ba(OH)_2 -> BaSO_4 + 2NH_3 + 2H_2O`
`2NH_4NO_3 + Ba(OH)_2 -> Ba(NO_3)_2 + 2NH_3 + 2H_2O`
d)
| `ZnSO_4` | `NH_4Cl` | `Ba(NO_3)_2` | `Na_2CO_3` | `(NH_4)_2CO_3` | |
| dd `Ba(OH)_2` dư | `-` \(\downarrow\) trắng, sau đó tan ra 1 phần | `-` \(\uparrow\) không màu, mùi khai | `-` Không hiện tượng | `-` \(\downarrow\) trắng | `-` \(\downarrow\) trắng, \(\uparrow\) không màu, mùi khai |
`Ba(OH)_2 + ZnSO_4 -> BaSO_4 + Zn(OH)_2`
`Ba(OH)_2 + Zn(OH)_2 -> BaZnO_2 + 2H_2O`
`Ba(OH)_2 + 2NH_4Cl -> BaCl_2 + 2NH_3 + 2H_2O`
`Ba(OH)_2 + Na_2CO_3 -> BaCO_3 + 2NaOH`
`Ba(OH)_2 + (NH_4)_2CO_3 -> BaCO_3 + 2NH_3 + 2H_2O`
Câu 6:
a)
| `(NH_4)_2SO_4` | `NH_4Cl` | `Na_2SO_4` | `NaCl` | |
| dd `Ba(OH)_2` dư | `-` \(\downarrow\) trắng, \(\uparrow\) không màu, mùi khai | `-` \(\uparrow\) không màu, mùi khai | `-` \(\downarrow\) trắng | `-` Không hiện tượng |
`(NH_4)_2SO_4 + Ba(OH)_2 -> BaSO_4 + 2NH_3 + 2H_2O`
`2NH_4Cl + Ba(OH)_2 -> BaCl_2 + 2NH_3 + 2H_2O`
`Na_2SO_4 + Ba(OH)_2 -> BaSO_4 + 2NaOH`
b)
| `ZnSO_4` | `NH_4Cl` | `Ba(NO_3)_2` | `Na_2CO_3` | `NaNO_3` | |
| dd `KOH` dư | `-` \(\downarrow\) trắng, sau đó tan | `-` \(\uparrow\) không màu, mùi khai | `-` Không hiện tượng | `-` Không hiện tượng | `-` Không hiện tượng |
| dd `H_2SO_4` | `-` \(\downarrow\) trắng | `-` \(\uparrow\) không màu, không mùi | `-` Không hiện tượng |
`ZnSO_4 + 2KOH -> Zn(OH)_2 + K_2SO_4`
`Zn(OH)_2 + 2KOH -> K_2ZnO_2 + 2H_2O`
`NH_4Cl + KOH -> KCl + NH_3 + H_2O`
`Ba(NO_3)_2 + H_2SO_4 -> BaSO_4 + 2HNO_3`
`Na_2CO_3 + H_2SO_4 -> Na_2SO_4 + CO_2 + H_2O`
c)
| `HCl` | `H_2SO_4` | `NaCl` | `NH_3` | `NH_4Cl` | |
| quỳ tím | `-` đỏ | `-` đỏ | `-` không đổi màu | `-` xanh | `-` đỏ |
| dd `Ba(OH)_2` | `-` không hiện tượng | `-` \(\downarrow\) trắng | `-` \(\uparrow\) không màu, mùi khai |
`Ba(OH)_2 + 2HCl -> BaCl_2 + 2H_2O`
`Ba(OH)_2 + H_2SO_4 -> BaSO_4 + 2H_2O`
`Ba(OH)_2 + 2NH_4Cl -> BaCl_2 + 2NH_3 + 2H_2O`
d)
| `Na_2CO_3` | `CuSO_4` | `Fe_2(SO_4)_3` | `BaCl_2` | `KCl` | |
| dd `KOH` | `-` không hiện tượng | `-` \(\downarrow\) xanh lơ | `-` \(\downarrow\) nâu đỏ | `-` không hiện tượng | `-` không hiện tượng |
| dd `H_2SO_4` | `-` \(\uparrow\) không màu, không mùi | `-` \(\downarrow\) trắng | `-` không hiện tượng |
`CuSO_4 + 2KOH -> Cu(OH)_2 + K_2SO_4`
`Fe_2(SO_4)_3 + 6KOH -> 2Fe(OH)_3 + 3K_2SO_4`
`H_2SO_4 + Na_2CO_3 -> Na_2SO_4 + CO_2 + H_2O`
`BaCl_2 + H_2SO_4 -> BaSO_4 + 2HCl`
Câu 8:
a) - Có hỗn hợp kết tủa xanh lơ và trắng xuất hiện, màu xanh của dd nhạt dần, kết tủa tăng lên đến cực đại rồi kết tủa bị hòa tan, tạo dd phức màu xanh
`CuSO_4 + 2NH_3 + 2H_2O -> Cu(OH)_2 + (NH_4)_2SO_4`
`ZnCl_2 + 2NH_3 + 2H_2O -> Zn(OH)_2 + 2NH_4Cl`
`Cu(OH)_2 + 4NH_3 -> [Cu(NH_3)_4](OH)_2`
`Zn(OH)_2 + 4NH_3 -> [Zn(NH_3)_4](OH)_2`
b) - Có kết tủa keo trắng xuất hiện, kết tủa tăng lên đến cực đại
`Al(NO_3)_3 + 3NH_3 + 3H_2O -> Al(OH)_3 + 3NH_4NO_3`
Câu 9:
a)
`- NH_4Cl:`
Mẩu Bari nóng chảy tạo thành khối hình cầu, chạy nhanh trên bề mặt của dd, tan dần, có sủi bọt khí không màu, không mùi, sau đó có khí mùi khai thoát ra
`Ba + 2H_2O -> Ba(OH)_2 + H_2`
`Ba(OH)_2 + 2NH_4Cl -> BaCl_2 + 2NH_3 + 2H_2O`
`- NaCl:`
Mẩu Bari nóng chảy tạo thành khối hình cầu, chạy nhanh trên bề mặt của dd, tan dần, có sủi bọt khí không màu, không mùi
`Ba + 2H_2O -> Ba(OH)_2 + H_2`
`- (NH_4)_2CO_3:`
Mẩu Bari nóng chảy tạo thành khối hình cầu, chạy nhanh trên bề mặt của dd, tan dần, có sủi bọt khí không màu, không mùi, sau đó có kết tủa trắng đồng thời có khí không màu, mùi khai thoát ra
`Ba + 2H_2O -> Ba(OH)_2 + H_2`
`Ba(OH)_2 + (NH_4)_2CO_3 -> BaCO_3 + 2NH_3 + 2H_2O`
b)
$NH_4Cl \xrightarrow{t^o} NH_3 + HCl$
$(NH_4)_2CO_3 \xrightarrow{t^o} 2NH_3 + CO_2 + H_2O$
$NH_4NO_2 \xrightarrow{t^o} N_2 + 2H_2O$
$NH_4NO_3 \xrightarrow{t^o} N_2O + 2H_2O$

Ta có: \(\left\{{}\begin{matrix}n_{Ba\left(OH\right)_2}=0,5.0,1=0,05\left(mol\right)\\n_{KOH}=0,1.0,5=0,05\left(mol\right)\end{matrix}\right.\)
`=>` \(\sum n_{OH^-}=0,05.2+0,05=0,15\left(mol\right)\)
Lại có: \(n_{H^+}=2n_{H_2SO_4}=0,1.1.2=0,2\left(mol\right)\)
PTHH: \(H^++OH^-\rightarrow H_2O\)
0,15<---0,15
`=>` \(\left[H^+\right]=\dfrac{0,2-0,15}{0,1+0,1+0,1}=\dfrac{1}{6}M\)
`=>` \(pH=-\text{log}\left(\dfrac{1}{6}\right)\approx0,778\)

Câu 10:
Ta có: \(n_{NH_3}=\dfrac{6,8}{17}=0,4\left(mol\right)\)
PTHH: \(N_2+3H_2\xrightarrow[]{t^o,p,xt}2NH_3\)
1------------------->2
`=>` \(H=\dfrac{0,4}{2}.100\%=20\%\)
Câu 11:
Ta có: \(\left\{{}\begin{matrix}n_{N_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\\n_{H_2}=\dfrac{39,2}{22,4}=1,75\left(mol\right)\\n_{NH_3}=\dfrac{3,4}{17}=0,2\left(mol\right)\end{matrix}\right.\)
PTHH: \(N_2+3H_2\xrightarrow[]{t^o,p,xt}2NH_3\)
0,1<-0,3<---------0,2
Xét tỉ lệ: \(\dfrac{0,5}{1}< \dfrac{1,75}{3}\Rightarrow\) Hiệu suất phản ứng tính theo N2
`=>` \(H=\dfrac{0,1}{0,5}.100\%=20\%\)
Câu 12:
Gọi \(n_{N_2}=a\left(l\right)\left(ĐK:0< a< 2\right)\)
PTHH: \(N_2+3H_2\xrightarrow[]{t^o,p,xt}2NH_3\)
a----->3a--------->2a
Sau phản ứng có: \(\left\{{}\begin{matrix}n_{N_2}=2-a\left(l\right)\\n_{H_2}=8-3a\left(l\right)\\n_{NH_3}=2a\left(l\right)\end{matrix}\right.\)
`=> 2 - a + 8 - 3a + 2a = 9`
`=> a = 0,5 (l) (TM)`
`=>` \(V_{NH_3}=2.0,5=1\left(l\right)\)
b) Xét tỉ lệ: \(\dfrac{2}{1}< \dfrac{8}{3}\Rightarrow\) Hiệu suất phản ứng tính theo N2
`=>` \(H=\dfrac{0,5}{2}.100\%=25\%\)


ta có
nNa++nMg2+=nSO42-+nCl-
=>0,1+2.0,05=0,04.2+nCl-
=>nCl-=0,12 mol
=>m muối=0,1.23+0,05.24+0,04.96+0,12.35,5
=11,6g