Trong tự nhiên, các nguyên tố halogen tồn tại ở dạng hợp chất. Viết công thức một vài hợp chất của halogen thường được dùng trong thực tế.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) Khi 2 nguyên tử halogen liên kết với nhau, mỗi nguyên tử sẽ góp 1 electron tạo thành 1 cặp electron dùng chung
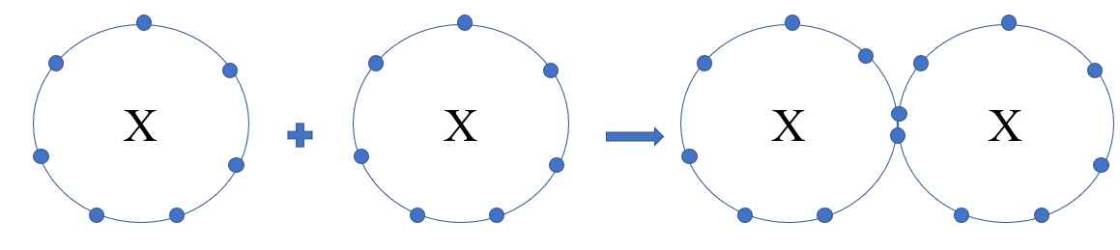
b)
- Trong phân tử halogen, liên kết hình thành giữa 2 nguyên tử giống nhau
=> Hiệu độ âm điện = 0, cặp electron dùng chung không bị hút lệch về phía nguyên tử nào
=> Liên kết cộng hóa trị không phân cực
c)
- Độ dài liên kết là khoảng cách giữa 2 hạt nhân của 2 nguyên tử
- Đi từ F đến I, bán kính nguyên tử tăng dần
=> Khoảng cách giữa 2 hạt nhân tăng dần
=> Độ dài liên kết trong dãy các phân tử halogen tăng dần

Nguyên tử | Lớp electron ngoài cùng | Bán kính nguyên tử | Độ âm điện |
Fluorine | 2s22p6 | 73 | 3,98 |
Chlorine | 3s23p6 | 103 | 3,16 |
Bromine | 4s24p6 | 119 | 2,96 |
Iodine | 5s25p6 | 142 | 2,66 |
a)
- Nguyên tử halogen có 7 electron ở lớp ngoài cùng, dễ nhận thêm 1 electron để đạt được cấu hình electron bền cùng khí hiếm gần nhất.
+ Khi nguyên tử halogen liên kết với kim loại => Khi đó kim loại sẽ nhường electron và nguyên tử halogen sẽ nhận 1 electron để trở thành ion mang điện tích âm
+ Khi nguyên tử halogen liên kết với phi kim => 2 phi kim kết hợp với nhau tạo thành phân tử, chúng sẽ góp electron để tạo thành các cặp electron dùng chung => Halogen sẽ góp chung 1 electron để đạt cấu hình electron bền vững
b)
- Bán kính nguyên tử: Đi từ trên xuống dưới, số lớp electron tăng => Lực hút giữa hạt nhân và lớp electron ngoài cùng giảm dần => Bán kính tăng dần
- Độ âm điện: Đi từ trên xuống dưới, số lớp electron tăng => Lực hút giữa hạt nhân với các electron lớp ngoài cùng giảm nên độ âm điện giảm
- Từ F đến I, độ âm điện giảm dần => Khả năng hút (nhận) electron giảm dần => Tính oxi hóa giảm dần
c)
- Nguyên tử fluorine có 7 electron ở lớp ngoài cùng và có độ âm điện lớn nhất
=> Khi tham gia liên kết hóa học, fluorine chỉ nhận 1 electron từ các nguyên tử khác
=> Fluorine chỉ có số oxi hóa -1 trong các hợp chất


Trong tự nhiên, halogen chỉ tồn tại ở dạng hợp chất là bởi vì halogen là những chất có khả năng oxy hóa mạnh nên phản ứng với các chất trong tự nhiên để tạo ra hợp chất
HALOGEN LÀ CHẤT CÓ KHẢ NĂNG OXI HÓA CAO NÊN PỨ ĐỂ TẠO RA HỢP CHẤT TRONG TỤ NHIÊN

\(V_{45}=0.068\)
=>\(2^3\cdot0.017=0.068\)
=>Cần giảm nhiệt độ xuống 15 độ C để tốc độ phản ứng là 0,017mol/(L.min)

Chuẩn bị: 2 ống nghiệm, 2 kẹp gỗ, 1 đèn cồn, 4 gam Zn hạt và dung dịch H2SO4 loãng 0,1 M.
Tiến hành:
- Cho vào 2 ống nghiệm, mỗi ống 5mL H2SO4 0,1M
- Cho cùng một lượng (2 gam) zinc dạng viên vào ống nghiệm (1) và (2).
- Đun nóng 1 ống nghiệm
Kết quả: Ống nghiệm dược đun nóng sẽ thoát khí nhanh hơn.

a) Đồ thị em vẽ mãi không được a tham khảo tí nhé :v
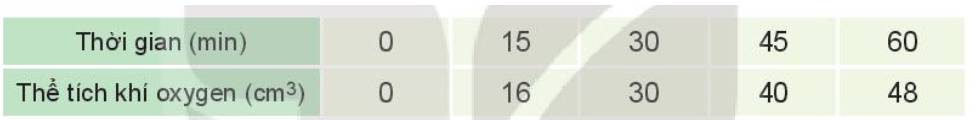
Đồ thị mô tả sự phụ thuộc của thể tích khí oxygen theo thời gian: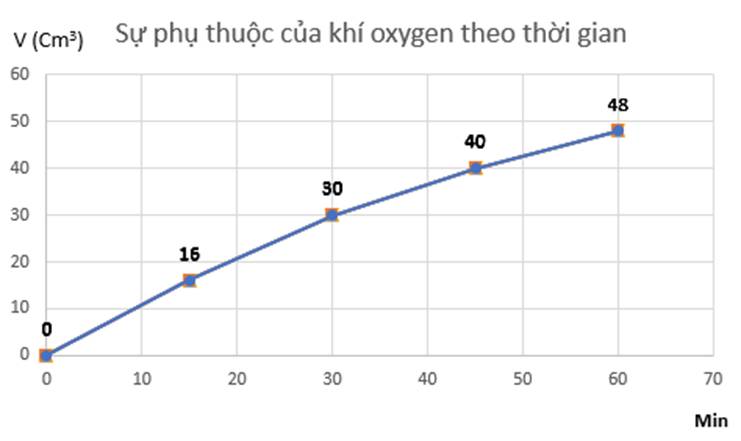 b)
b)
Ta có công thức tính vận tốc trung bình: \(V_{tb}=\dfrac{S_1+S_2....}{t_1+t_2....}\)
Tốc độ trung bình của phản ứng từ 0 - 15 phút là:
\(V_{tb_1}=\dfrac{16-0}{15-0}=1,0666....\approx1,067\) (cm3/min)
Tốc độ trung bình của phản ứng từ 15 - 30 phút là:
\(V_{tb_2}=\dfrac{30-16}{30-15}=0,9333....\approx0,933\) (cm3/min)
Tốc độ trung bình của phản ứng từ 30 - 45 phút là:
\(V_{tb_3}=\dfrac{40-30}{45-30}=0,66666.....\approx0,667\) (cm3/min)
Tốc độ trung bình của phản ứng từ 45 - 60 phút là:
\(V_{tb_4}=\dfrac{48-40}{60-45}=0,5333.....\approx0,533\) (cm3/min)
Ta thấy \(V_{tb_1}>V_{tb_2}>V_{tb_3}>V_{tb_4}\)
=> Tốc độ trung bình của phản ứng giảm dần theo thời gian.

a: Tốc độ phản ứng tăng lên do bề mặt tiếp xúc tăng lên
b: Tốc độ phản ứng giảm xuống do nồng độ giảm
c: Tốc độ phản ứng tăng lên do nhiệt độ tăng
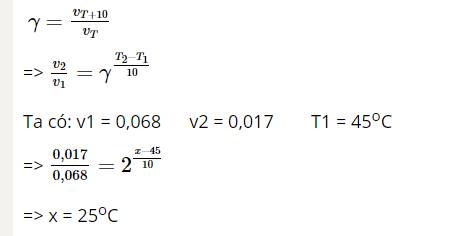
NaCl,NaF,AgBr,NaClO
NACL,CACL\(_2\),KCL,MGCL\(_2\),....