I. Viết phương trình điện li của các chất sau:
1. HNO3, Ba(OH)2, NaOH, H2SO4, Ca(OH)2, Na2CO3, BaCl2, NaHCO3, H2S;
2. CuSO4, Na2SO4, Fe2(SO4)3, Na2HPO4, Mg(OH)2, CH3COOH, H3PO4, HF.
II. Viết phương trình phân tử và ion rút gọn của các phản ứng (nếu có) khi trộn lẫn các chất sau:
1. Dung dịch HNO3 và dung dịch CaCO3; 2. Dung dịch KOH và dung dịch FeCl3;
3. Dung dịch H2SO4 và dung dịch NaOH; 4. Dung dịch Ca(NO3)2 và dung dịch Na2CO3;
5. Dung dịch NaOH và dung dịch Al(OH)3; 6. Dung dịch Al2(SO4)3 và dung dịch NaOHvừa đủ;
7. Dung dịch NaOH và dung dịch Zn(OH)2; 8. Dung dịch FeS và dung dịch HCl;
9. Dung dịch CuSO4 và dung dịch H2S; 10. Dung dịch NaOH và dung dịch NaHCO3;
11. Dung dịch NaHCO3 và dung dịch HCl; 12. Dung dịch Ca(HCO3)2 và dung dịch HCl.
III. Nhận biết các dung dịch sau bằng phương pháp hoá học
1. NH4NO3, (NH4)2CO3, Na2SO4, NaCl
2. NaOH, NaCl, Na2SO4, NaNO3
3. NaOH, H2SO4, BaCl2, Na2SO4, NaNO3 (chỉ dùng thêm quỳ tím)
IV. Viết phương trình phân tử ứng với phương trình ion thu gọn của các phản ứng sau
1. Ba2+ + CO32- → BaCO3↓ 2. NH4+ + OH- → NH3↑ + H2O
3. S2- + 2H+ → H2S↑ 4. Fe3+ + 3OH- → Fe(OH)3↓
5. Ag+ + Cl- → AgCl↓ 6. H+ + OH- → H2O
V. Viết phương trình dạng phân tử và ion rút gọn của các phản ứng trong dung dịch theo sơ đồ sau:
1. Pb(NO3)2 + ... → PbCl2 + ...
2. FeCl3 + ... → Fe(OH)3 + ...
3. BaCl2 + ... → BaSO4↓ + ...
4. HCl + ... → ... + CO2↑ + H2O
5. NH4NO3 + ... → ... + NH3↑ + H2O
6. H2SO4 + ... → ... + H2O
VI. Tính nồng độ các ion trong dung dịch sau:
1. Dung dịch NaOH 0,1M
2. Dung dịch BaCl2 0,2M
3. Dung dịch Ba(OH)2 0,1M
VII. Hoà tan 20 gam NaOH vào 500ml nước thu được dung dịch A
1. Tính nồng độ các ion trong dung dịch A
2. Tính thể tích dung dịch HCl 2M để trung hoà dung dịch A
VIII. Trộn 100ml dung dịch NaOH 2M với 200ml dung dịch KOH 0,5M thu được dung dịch C
1. Tính nồng độ các ion trong dung dịch C
2. Trung hoà dung dịch C bằng 300ml dung dịch H2SO4 CM. Tính CM
IX. Trộn 100ml dung dịch HCl 1M với 100ml dung dịch H2SO4 0,5M thu được dung dịch D.
1. Tính nồng độ các ion trong dung dịch D
2. Cho dung dịch D tác dụng với dung dịch BaCl2 dư thu được m gam kết tủa. Tính m.
X. Tính pH của các dung dịch sau:
1. NaOH 0,001M 2. HCl 0,001M
3. Ca(OH)2 0,0005M 4. H2SO4 0,0005M
XI. Trộn 200ml dung dịch NaOH 0,1M với 300ml dung dịch HCl 0,2M thu được dung dịch A
1. Tính nồng độ các ion trong dung dịch A
2. Tính pH của dung dịch A
XII. Trộn 100ml dung dịch NaOH 0,1M vào 100ml KOH 0,1M thu được dung dịch D
1. Tính nồng độ các ion trong dung dịch D
2. Tính pH của dung dịch D
3. Trung hoà dung dịch D bằng dung dịch H2SO4 1M. Tính thể tích dung dịch H2SO4 1M cần dùng
XIII. Hỗn hợp dung dịch X gồm NaOH 0,1M và KOH 0,1M. Trộn 100ml dung dịch X với 100ml dung dịch H2SO4 0,2M thu được dung dịch A
1. Tính nồng độ các ion trong dung dịch A
2. Tính pH của dung dịch A
XIV. Dung dịch X chứa 0,01 mol Fe3+; 0,02 mol NH4+; 0,02 mol SO42- và x mol NO3-
1. Tính x
2. Trộn dung dịch X với 100ml dung dịch Ba(OH)2 0,3M thu được m gam kết tủa và V lít khí (đktc). Tính m và V.
XV. Trộn 100ml dung dịch FeCl3 0,1M với 500ml dung dịch NaOH 0,1M thu được dung dịch D và m gam kết tủa
1. Tính nồng độ các ion trong D
2. Tính m
XVI. Trộn 50ml dung dịch NaOH 0,4M với 50ml dung dịch HCl 0,2M được dung dịch A. Tính pH của dung dịch A.
XVII. Trộn lẫn 100ml dung dịch HCl 0,03M với 100ml dung dịch NaOH 0,01M được dung dịch A
1. Tính pH của dung dịch A.
2. Tính thể tích dung dịch Ba(OH)2 1M đủ để trung hoà dung dịch A.
XVIII. Trộn lẫn 100ml dung dịch K2CO3 0,5M với 100ml dung dịch CaCl2 0,1M.
1. Tính khối lượng kết tủa thu được
2. Tính CM các ion trong dung dịch sau phản ứng
XIX. Trộn 50ml dung dịch HCl với 50ml dung dịch NaOH có pH = 13 thu được dung dịch X có pH = 2. Số mol của dung dịch HCl ban đầu là bao nhiêu?
XX. Chia 19,8 gam Zn(OH)2 thành hai phần bằng nhau
1. Cho 150ml dung dịch H2SO4 1M vào phần một. Tính khối lượng muối tạo thành
2. Cho 150ml dung dịch NaOH 1M vào phần hai. Tính khối lượng muối tạo thành
XXI. Cho 100ml dung dịch hỗn hợp A gồm H2SO4 0,015M; HCl 0,03M; HNO3 0,04M. Tính thể tích dung dịch NaOH 0,2M để trung hoà hết 200ml dung dịch A.
XXII. Cho 100ml dung dịch X gồm Ba(OH)2 0,015M; NaOH 0,03M; KOH 0,04M. Tính thể tích dung dịch HCl 0,2M để trung hoà dung dịch X.
XXIII. Cho dung dịch A gồm 2 chất HCl và H2SO4. Trung hoà 1000ml dung dịch A thì cần 400ml dung dịch NaOH 0,5M. Cô cạn dung dịch tạo thành thì thu được 12,95 gam muối.
1. Tính nồng độ mol/l của các ion trong dung dịch A.
2. Tính pH của dung dịch A.
XXIV. Cho 200ml dung dịch gồm MgCl2 0,3M; AlCl3 0,45M và HCl 0,55M tác dụng hoàn toàn với V lít dung dịch C gồm NaOH 0,02M và Ba(OH)2 0,01M. Hãy tính thể tích V để được kết tủa lớn nhất và kết tủa nhỏ nhất? Tính lượng kết tủa đó?
XXV. Trộn 250ml dung dịch hỗn hợp gồm HCl 0,08mol/l và H2SO4 0,01mol/l với 250ml dung dịch NaOH a mol/l, thu được 500ml dung dịch có pH = 12. Tính a.
XXVI. Để trung hoà 500ml dung dịch X chứa hỗn hợp HCl 0,01M và H2SO4 0,3M cần bao nhiêu ml dung dịch hỗn hợp gồm NaOH 0,3M và Ba(OH)2 0,2M?
Các bạn giải hết đề cương ôn thi giữa học kì I đề từ câu I đến câu XXVI dùm mình nhé. Cảm ơn các bạn rất nhiều.

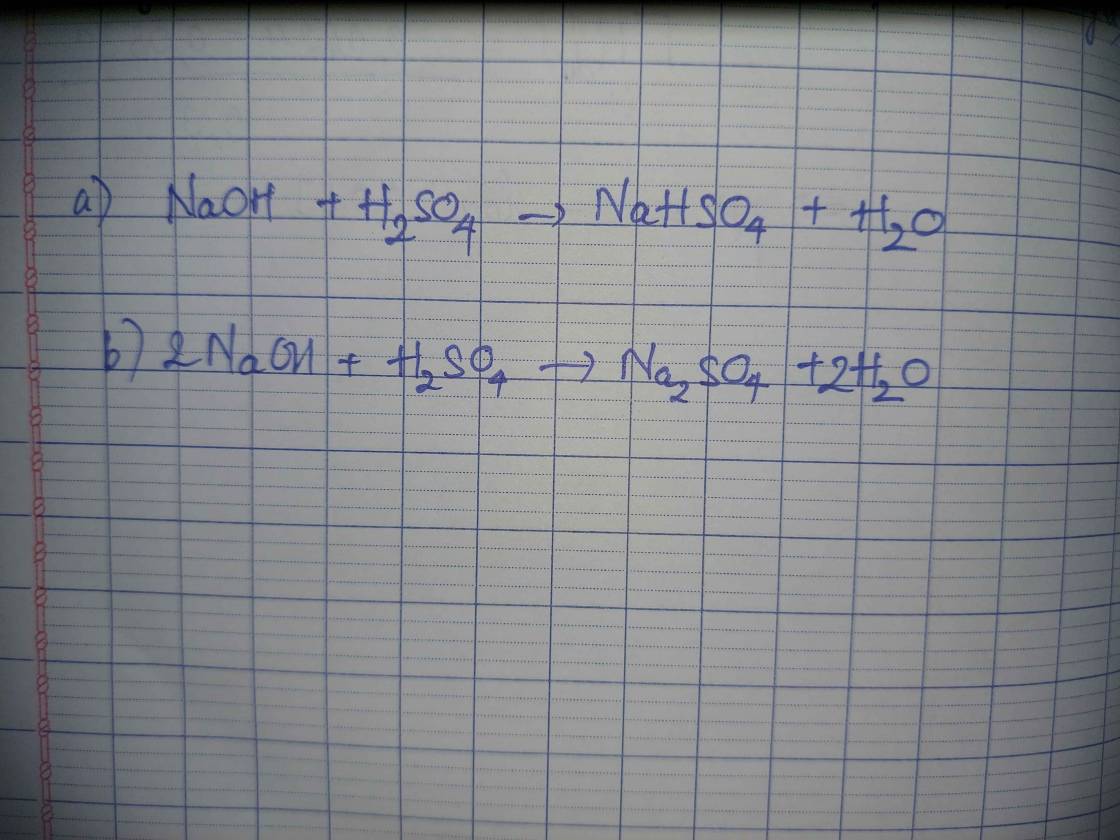
Em chia nhỏ ra đăng bài lên để các bạn dễ làm nhé
(1) \(2HNO_3+CaCO_3\rightarrow Ca\left(NO_3\right)_2+H_2O+CO_2\uparrow\)
(2) \(3KOH+FeCl_3\rightarrow Fe\left(OH\right)_3\downarrow+3KCl\)
(5) \(NaOH+Al\left(OH\right)_3\rightarrow NaAlO_2+2H_2O\)
(6) \(Al_2\left(SO_4\right)_3+6NaOH\xrightarrow[]{}2Al\left(OH\right)_3\downarrow+3Na_2SO_4\)
(9) \(CuSO_4+H_2S\xrightarrow[]{}CuS\downarrow+H_2SO_4\)
(10) \(NaOH+NaHCO_3\xrightarrow[]{}Na_2CO_3+H_2O\)