
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(3.\\ n_{ZnO}=\dfrac{8,1}{81}=0,1mol\\ Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,1 0,2 0,1 0,1
\(m_{ZnCl_2}=0,1.136=13,6g\\ C_{\%HCl}=\dfrac{0,2.36,5}{120}\cdot100\%=6,08\%\\ 4.\\ n_K=\dfrac{7,8}{39}=0,2mol\\ 2K+2H_2O\rightarrow2KOH+H_2\)
0,2 0,2 0,2 0,1
\(KOH+HCl\rightarrow KCl+H_2O\)
0,2 0,2 0,2 0,2
\(m_{KCl}=0,2.74,5=14,9\\ C_{\%HCl}=\dfrac{0,2.36,5}{200}\cdot100\%=3,65\%\)

Ta có \(n_{O_2}=\dfrac{V}{24,79}=\dfrac{4,958}{24,79}=0,2\left(mol\right)\)
\(\Rightarrow m_{O_2}=n.M=0,2.32=6,4\left(g\right)\)
=> Chọn A

\(n_{Fe}=\dfrac{2,8}{56}=0,05mol\\
n_{HCl}=\dfrac{14,6}{36,5}=0,4mol\\
Fe+2HCl\rightarrow FeCl_2+H_2\\
\dfrac{0,05}{1}< \dfrac{0,4}{2}\Rightarrow HCl.dư\\
Fe+2HCl\rightarrow FeCl_2+H_2\)
0,05 0,1 0,05 0,05
\(n_{HCl.dư}=0,4-0,1=0,3mol\\
m_{HCl.dư}=0,3.36,5=10,95g\\
b)V_{H_2}=0,05.24,79=1,2395l\\
c)Fe+2HCl\rightarrow FeCl_2+H_2\)
0,2 0,4 0,2 0,2
\(m_{Fe.pư}=0,2.56=11,2g\\ m_{Fe.thêm}=11,2-2,8=8,4g\)

\(n_{H_2}=\dfrac{17,6}{24,79}\approx0,7mol\\ n_{Zn}=a;n_{Al}=b\\ a)Zn+2HCl\rightarrow ZnCl_2+H_2\\ a.....2a.......a........a\\ 2Al+6HCl\rightarrow2AlCl_3+3H_2\\ b......3b.......b........1,5b\\ \Rightarrow\left\{{}\begin{matrix}65a+27b=17,3\\a+1,5b=0,7\end{matrix}\right.\\ \Rightarrow\left\{{}\begin{matrix}a=0,1\\b=0,4\end{matrix}\right.\\ b)\%m_{Zn}=\dfrac{0,1.65}{17,3}\cdot100\%=37,57\%\\ \%m_{Al}=100\%-37,57\%=62,43\%\\ c)m_{dd}=17,3+400-0,7.2=415,9g\\ C_{\%ZnCl_2}=\dfrac{136.0,1}{415,9}\cdot1005=3,27\%\\ \%m_{AlCl_3}=\dfrac{133,5.0,4}{415,9}\cdot100\%=12,84\%\)

\(a)n_{Al}=\dfrac{32,4}{27}=1,2g\\ n_{O_2}=\dfrac{23,8}{24,79}\approx0,93mol\\ 4Al+3O_2\xrightarrow[]{t^0}2Al_2O_3\)
\(\Rightarrow\dfrac{1,2}{4}< \dfrac{0,93}{3}\Rightarrow O_2.dư\\ 4Al+3O_2\xrightarrow[t^0]{}2Al_2O_3\\ 1,2.....0,9........0,6\\
n_{O_2.dư}=0,93-0,9=0,03mol\\
m_{O_2.dư}=0,03.32=0,96g\\
b)m_{Al_2O_3}=0,6.102=61,2g\\
c)2Al+6HCl\rightarrow2AlCl_3+3H_2\)
1,2 3,6 1,2 1,8
\(V_{H_2}=1,8.24,79=44,622l\)

\(CH_4+2O_2\xrightarrow[]{t^o}CO_2+2H_2O\)
\(n_{CH_4}=\dfrac{12,395}{24,79}=0,5\left(mol\right)\)
Theo PTHH: \(n_{O_2}=2n_{CH_4}=2\cdot0,5=1\left(mol\right)\)
\(\Rightarrow V_{O_2}=1\cdot24,79=24,79\left(l\right)\)
Theo PTHH: \(n_{CO_2}=n_{CH_4}=0,5\left(mol\right)\)
\(\Rightarrow V_{CO_2}=0,5\cdot24,79=12,395\left(l\right)\)


a) Gọi CTPT chung của A là \(C_xH_y\)
\(n_{CO_2}=\dfrac{2,64}{44}=0,06mol\\ \Rightarrow m_C=12.0,06=0,72g\\ n_{H_2O}=\dfrac{1,44}{18}=0,08mol\\ \Rightarrow m_H=2.0,08=0,16g\\ n_X=\dfrac{0,448}{22,4}=0,02mol\\ m_X=0,02.44=0,88g\)
Ta có tỉ lệ
\(\dfrac{12x}{0,72}=\dfrac{y}{0,16}=\dfrac{44}{0,88}\\ \Rightarrow x=3;y=8\)
Vậy CTPT của A là \(C_3H_8\)
\(b)CTCT:CH_3-CH_2-CH_3\\ PỨĐT:\)
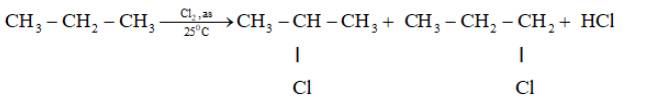
hihi