Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án: Nguyên tử X là Magie (Mg).
Giải thích (theo chương trình lớp 7, không lập phương trình):
- Một nguyên tử gồm ba loại hạt: proton, electron và neutron.
- Đề cho biết số hạt proton = electron = neutron, và tổng cả ba loại là 36 hạt.
- Khi ba nhóm số hạt bằng nhau, mỗi nhóm chiếm một phần ba tổng số hạt, tức là mỗi loại có 36 : 3 = 12 hạt.
- Số proton trong nguyên tử chính là số hiệu nguyên tử. Vậy X có số hiệu nguyên tử = 12.
- Trong bảng tuần hoàn, nguyên tố có số hiệu 12 là Magie (Mg)

Gọi proton, notron, electron lần lượt là p,n,e
Vì tổng số hạt là 116 nên ta có pt : p+n+e=116
Vì số hạt mang điện nhiều hơn số hạt không mang điện là 24 nên ta có :(p+e)−n=24Vì e=p nên ta có:⇒{p+e+n=116
(p+e)-n=24
⇒p=n=35;n=46
Vậy p=n=35;n=46

Số electron : 12
Số đơn vị điện tích hạt nhân : + 12
Số hạt electron lớp ngoài cùng : 2
Số electron : 12
Số đơn vị điện tích hạt nhân : + 12
Số hạt electron lớp ngoài cùng : 2

`#3107.101107`
a.
Gọi số hạt proton, neutron, electron trong nguyên tử X lần lượt là `p, n, e`
Tổng số hạt trong nguyên tử X là `48`
`=> p + n + e = 48`
Mà trong nguyên tử, số `p = e`
`=> 2p + n = 48`
Mà số hạt `p = n`
`=> 3p = 48`
`=> p = 48 \div 3`
`=> p = 16`
Vậy, số `p = n = e = 16`
b.
Khối lượng nguyên tử X là: `16 + 16 = 32` (amu)
c.
Bạn tham khảo mô hình NT X:
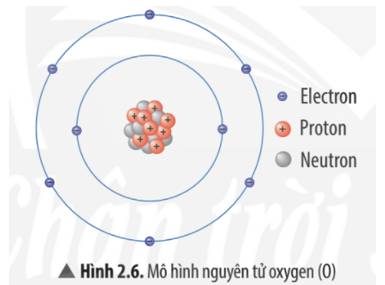
- X có `3` lớp electron
- X có `6` electron lớp ngoài cùng.

Bài 34:
Nguyên tử A có tổng số hạt là 60, trong hạt nhân số hạt mang điện bằng số hạt không mang điện.
- Hạt mang điện trong hạt nhân là proton, hạt không mang điện là neutron.
- Vì bằng nhau: \(p = n\) và trong hạt nhân \(p + n = 60 - e\).
- Số hạt electron \(e = p = n\) (nguyên tử trung hòa).
Vậy:
\(p + n + e = 60 , p = n = e\) \(3 p = 60 \Rightarrow p = n = e = 20\)
Đ/s: Số hạt: 20 proton, 20 neutron, 20 electron.
Bài 35:
Nguyên tử A có tổng số hạt là 28, số hạt không mang điện = \(\frac{10}{9}\) số hạt mang điện dương.
- Hạt mang điện dương = proton = p
- Hạt không mang điện = neutron = n = \(\frac{10}{9} p\)
- Electron = số hạt mang điện dương = p
Tổng số hạt: \(p + n + e = 28 \Rightarrow p + \frac{10}{9} p + p = 28\)
\(p + p + \frac{10}{9} p = \frac{28}{?}\)
Tính cẩn thận: \(p + p + \frac{10}{9} p = 2 p + \frac{10}{9} p = \frac{18}{9} p + \frac{10}{9} p = \frac{28}{9} p\)
\(\frac{28}{9} p = 28 \Rightarrow p = 9\)
- Neutron: \(n = \frac{10}{9} \times 9 = 10\)
- Electron: \(e = p = 9\)
Khối lượng nguyên tử ≈ số hạt trong hạt nhân = p + n = 9 + 10 = 19 u.
Khối lượng nguyên tử: 19 u
Đ/S: 19u
Bài 36:
Nguyên tử R có tổng số hạt là 52, số hạt không mang điện nhiều hơn số hạt mang điện là 1.
- Gọi p = số proton = e (nguyên tử trung hòa), n = số neutron
- Theo đề: n = p + 1
- Tổng số hạt: p + n + e = p + (p + 1) + p = 3p + 1 = 52
\(3 p + 1 = 52 \Rightarrow 3 p = 51 \Rightarrow p = 17\)
- Neutron: n = p + 1 = 17 + 1 = 18
- Electron: e = p = 17
Đ/S: Số hạt: 17 proton, 18 neutron, 17 electron.

Gọi p là số proton
Gọi n là số nơ tron
Gọi e là số electron
Theo đề bài ta có :
p+n+e=58 và p+n<40
Ta thấy p+n=39<40 (số khối hay Khối lượng nguyên tử) ⇒ n=58-39=19 electron (lớp 1 : 2 electron; lớp 2 : 8 electron; lớp 3: 8 electron; lớp 4 : 1 electron)
⇒ Nguyên tử đó có 4 lớp electron và lớp ngoài cùng có 1 electron ⇒ Thuộc chu kỳ 4 và Nhóm IA
Vậy nguyên tử đó là K (Protassium) và số hiệu nguyên tử là 19

Electron nhỏ hơn nguyên tử mà bạn?
nhưng tại sao họ lại ko cho điều đó đúng