Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Công thức phân tử của hợp chất A :
Số mol các sản phẩm của phản ứng :
n SO 2 = 0,1 mol; n H 2 O = 0,1 mol
Khối lượng của hiđro có trong 0,1 mol H 2 O (2 g.0,1 = 0,2 g) và khối lượng của lưu huỳnh có trong 0,1 mol SO 2 (32 g.0,1 = 3,2 g) đúng bằng khối lượng của hợp chất A đem đốt (3,4 g).
Vậy thành phần của hợp chất A chỉ có 2 nguyên tố là H và S.
- Tỉ lệ giữa số mol nguyên tử H và số mol nguyên tử S là :
n H : n S = 0,1.2 : 0,1 = 2 : 1
Công thức phân tử của hợp chất A là : H 2 S

Nồng độ phần trăm của các chất trong dung dịch :
Biết số mol NaOH (0,3 mol) nhiều hơn 2 lần số mol SO 2 (0,1 mol) vậy sản phẩm là muối Na 2 SO 3 . Ta có PTHH :
SO 2 + 2NaOH → Na 2 SO 3 + H 2 O
- Khối lượng của dung dịch sau phản ứng :
m dd = 146,6 + 3,4 = 150 (g)
- Khối lượng các chất có trong dung dịch sau phản ứng :
m Na 2 SO 3 = 126.0,1 = 12,6g
m NaOH dư = 40.(0,3 - 0,2) = 4g
- Nồng độ phần trăm các chất trong dung dịch sau phản ứng :
C % Na 2 SO 3 = 12,6/150 x 100% = 8,4%
C % NaOH dư = 4/150 x 100% = 2,67%

Xác định công thức phân tử của hợp chất A
nSO2 = 1,344 / 22,4 = 0,06 mol → mS = 0,06 x 32 = 1,92g
nH2O = 1,08 / 18 = 0,06 mol → mH = 0,06 x 2 = 0,12g.
Như vậy hợp chất A chỉ có nguyên tố S và H.
Đặt công thức phân tử hợp chất là HxSy.
Ta có tỉ lệ: x : y = 0,06 : 0,12 = 1: 2.
Vậy công thức phân tử của A và là H2S.
Phương trình hóa học của phản ứng:
nH2S = 2,04 / 34 = 0,06 mol.
3H2S + H2O → 4S + 4H2O.
nS = 4/3 nH2S = 0,08 mol.
mS = 0,08 × 32 = 2,56g.
Xác định công thức phân tử của hợp chất A
nSO2 = 1,344 / 22,4 = 0,06 mol → mS = 0,06 x 32 = 1,92g
nH2O = 1,08 / 18 = 0,06 mol → mH = 0,06 x 2 = 0,12g.
Như vậy hợp chất A chỉ có nguyên tố S và H.
Đặt công thức phân tử hợp chất là HxSy.
Ta có tỉ lệ: x : y = 0,06 : 0,12 = 1: 2.
Vậy công thức phân tử của A và là H2S.
Phương trình hóa học của phản ứng:
nH2S = 2,04 / 34 = 0,06 mol.
3H2S + H2O \(\rightarrow\) 4S + 4H2O.
nS = 4/3 nH2S = 0,08 mol.
mS = 0,08 × 32 = 2,56g.

Theo đề bài cho, bột S dư nên Fe và Zn tác dụng hết với S.
a) Phương trình hóa học của phản ứng:
Zn + S \(\rightarrow\) ZnS
Fe + S \(\rightarrow\) FeS
ZnS + H2SO4 \(\rightarrow\) ZnSO4 + H2S
FeS + H2SO4 \(\rightarrow\)H2S + FeSO4
nZn = x mol.
nFe = y mol.
nH2S = 1,344 / 22,4 = 0,06 mol.
mhh = 65x + 56y = 3,27g.
nH2S = x + y = 0,06 mol.
Giải hệ phương trình trên ta được:
x = 0,04 mol, y = 0,02 mol.
mZn = 65 × 0,04 = 2,6g
mFe = 56 × 0,02 = 1,12g

Các bạn ơi giúp mình với. Chuyên đề này sáng mai mình phải nộp rồi! Cảm ơn các bạn nhiều!

Chọn A
Cách 1:
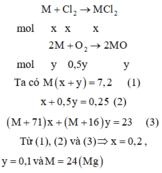
Cách 2:
Gọi số mol của Cl2 và O2 phản ứng lần lượt là x và y mol
→ nkhí = 0,25 mol → x + y = 0,25 (1)
Bảo toàn khối lượng có mkhí= 23 – 7,2= 15,8 gam
→ 71x + 32y = 15,8 (2)
Từ (1) và (2) → x = 0,2 và y = 0,05
Bảo toàn electron có:
2.nM = 2.nCl2 + 4.nO2 → nM= 0,3 → MM = 7,2 : 0,3 = 24 (g/mol)
Vậy kim loại M là Mg.

Đáp án A
mrắn sau − mM = mX ⇒ 71nCl2 + 32nO2 = 23 − 7,2 = 15,8 g (1)
⇒nkhí = nCl2 +nO2 = 0,25 mol (2)
Giải hệ (1) và (2) ⇒nCl2 = 0,2; nO2 = 0,05 mol
Gọi hóa trị của M là x
Bảo toàn e

M = ![]() = 12x, x = 2 => M = 24 (Mg)
= 12x, x = 2 => M = 24 (Mg)

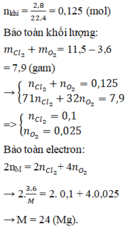
PTHH của phản ứng đốt cháy H 2 S
2 H 2 S + 3 O 2 → 2 H 2 O + 2 SO 2