Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) vì 13p +13e mà 13e =13amu nên kq là 13amu
b)vì 13p +13e mà 13e =13amu nên kq là 13amu
c)

a) Dùng không khó nén có nồng độ oxi cao và không khí đã nóng sẵn thổi vào lò cao nên tốc độ phản ứng tăng.
b) Lợi dụng yếu tố nhiệt độ (tăng nhiệt độ).
c) Lợi dụng yếu tố điện tích tiếp xúc (tăng điện tích tiếp xúc của nguyên liệu)
|
a) Lợi dụng yếu tố áp xuất và nhiệt độ ( tăng áp suất và nhiệt độ) b) Lợi dụng yếu tố nhiệt độ (tăng nhiệt độ) c) Lợi dụng yếu tố diện tích tiếp xúc bề mặt (tăng diện tích bề mặt tiếp xúc của nguyên liệu) |

Khi tan trong nước, các halogen tác dụng với nước, flo phản ứng mãnh liệt với nước giải phóng oxi.
2F2 + 2H2O \(\rightarrow\) 4HF + O2.
Với brom và clo thì phản ứng xảy ra theo hướng khác, brom tác dụng với nước chậm hơn.
Br2 + H2O ⇆ HBr + HBrO.
Cl2 + H2O ⇆ HCl + HClO
Iot không phản ứng với nước

- Khí Cl2 oxi hóa KI thành I2, Cl2 và I2 tan tong nước, do đó xuất hiện dung dịch màu vàng nâu.
Cl2 + KI \(\rightarrow\) 2KCl + I2
- Sau đó dung dịch vàng nâu chuyển sang màu xanh do iot tác dụng với hồ tinh bột.do m
- Do thêm dần dần nước clo, nên màu xanh của hồ tinh bột và iot cũng bị mất màu, do một phần khí Cl2 tác dụng với nước tạo ra axit HClO có tính oxi hóa mạnh, axit này làm mất màu xanh của tinh bột và iot.
Cl2 + H2O ⇌⇌ HCl + HClO

Theo đề bài cho, bột S dư nên Fe và Zn tác dụng hết với S.
a) Phương trình hóa học của phản ứng:
Zn + S \(\rightarrow\) ZnS
Fe + S \(\rightarrow\) FeS
ZnS + H2SO4 \(\rightarrow\) ZnSO4 + H2S
FeS + H2SO4 \(\rightarrow\)H2S + FeSO4
nZn = x mol.
nFe = y mol.
nH2S = 1,344 / 22,4 = 0,06 mol.
mhh = 65x + 56y = 3,27g.
nH2S = x + y = 0,06 mol.
Giải hệ phương trình trên ta được:
x = 0,04 mol, y = 0,02 mol.
mZn = 65 × 0,04 = 2,6g
mFe = 56 × 0,02 = 1,12g

a) Tính chất hóa học của nước Gia- ven
- Nước Gia-ven là hỗn hợp muối NaCl và NaClO là muối của axit yếu, trong không khí tác dụng với CO2 cho HClO không bền có tính oxi hóa mạnh.
NaClO + CO2 + H2O → NaHCO3 + HClO
2HClO → 2HCl + O2
- Nước Gia- ven không để được lâu, có tính oxi hóa mạnh.
b) Tính chất hóa học của clorua vôi
- Clorua có tính oxi hóa mạnh, khi tác dụng với dung dịch HCl giải phóng khí Clo:
CaOCl2 + 2HCl \(\rightarrow\) CaCl2 + Cl2\(\uparrow\) + H2O
- Trong không khí ẩm, clorua vôi tác dụng với CO2
2CaOCl2 + CO2 + H2O \(\rightarrow\) CaCO3 \(\downarrow\)+ CaCl2 + 2HClO
c) Ứng dụng của nước Gia-ven và clorua vôi
- Ứng dụng của nước Gia-ven
Dùng để tẩy trắng sợi vải, giấy. Nó cũng được dùng để khử mùi,sát trùng khi tẩy uế nhà vệ sinh hoặc những khu vực bị ô nhiễm khác.
- Ứng dụng của clorua vôi:
Cũng dùng để tẩy trắng sợi vải, giấy, để tẩy uế các hố rác, cống rãnh. Do khả năng tác dụng nhiều với chất hữu cơ, clorua vôi dùng để xử lí các chất độc. Một lượng lớn clorua vôi được dùng trong việc tinh chế dầu mỏ
a) Tính chất hóa học của nước Gia- ven
– Nước Gia-ven là hỗn hợp muối NaCl và NaClO là muối của axit yếu, trong không khí tác dụng với CO2 cho HClO không bền có tính oxi hóa mạnh.
NaClO + CO2 + H2O → NaHCO3 + HClO
2HClO → 2HCl + O2
– Nước Gia- ven không để được lâu, có tính oxi hóa mạnh.
b) Tính chất hóa học của clorua vôi
– Clorua có tính oxi hóa mạnh, khi tác dụng với dung dịch HCl giải phóng khí Clo:
CaOCl2 + 2HCl \(\rightarrow\) CaCl2 + Cl2\(\uparrow\) + H2O
– Trong không khí ẩm, clorua vôi tác dụng với CO2
2CaOCl2 + CO2 + H2O \(\rightarrow\) CaCO3 \(\downarrow\) + CaCl2 + 2HClO
c) Ứng dụng của nước Gia-ven và clorua vôi
– Ứng dụng của nước Gia-ven
Dùng để tẩy trắng sợi vải, giấy. Nó cũng được dùng để khử mùi,sát trùng khi tẩy uế nhà vệ sinh hoặc những khu vực bị ô nhiễm khác.
– Ứng dụng của clorua vôi:
Cũng dùng để tẩy trắng sợi vải, giấy, để tẩy uế các hố rác, cống rãnh. Do khả năng tác dụng nhiều với chất hữu cơ, clorua vôi dùng để xử lí các chất độc. Một lượng lớn clorua vôi được dùng trong việc tinh chế dầu mỏ
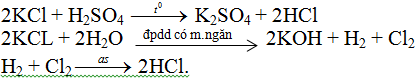
a) Thu nhiệt
b) Tỏa nhiệt
c) Thu nhiệt
d) Tỏa nhiệt
e) Thu nhiệt
f) Tỏa nhiệt
g) Tỏa nhiệt
i) Thu nhiệt