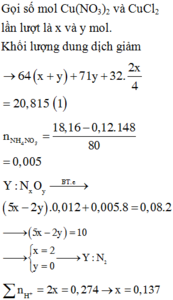Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
Ta có CM HNO3 = CM Cu(NO3)2
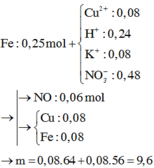
Vì thanh Fe còn dư ⇒ sản phẩm cuối cùng là Fe2+.
Ta có các pứ: 3Fe + 8HNO3 → 3Fe(NO3)2 + 2NO + 4H2O.
Sau đó: Fe + Cu(NO3)2 → Fe(NO3)2 + Cu↓.
Ta có: mGiảm = mFe – mCu = 56×( 3 a + a 8 + a) – 64a = 1,04.
<=> 13a = 1,04 <=> a = 0,08 mol.
⇒ nHNO3 = 0,08 ∑ne trao đổi = 0,08 mol ⇒ t = 0 , 08 × 96500 2 = 3860 giây.

Chọn đáp án A.
Phương trình điện phân:
Catot: Cu2+ + 2e → Cu
2H2O + 2e → H2 + 2OH-
Anot: 2Cl- → Cl2 + 2e
2H2O → 4H+ + O2 + 4e
Fe + dung dịch sau điện phân → NO
=> Chứng tỏ dung dịch chứa H+, ở anot đã xảy ra điện phân nước.
![]()
=> Chứng tỏ Cu2+ chưa bị điện phân hết


Đáp án A
Khối lượng dung dịch giảm gồm CuCl2: 0,075 mol và CuO : 14 , 125 - 0 , 075 . ( 64 + 71 ) 80 = 0,05 mol
Dung dịch Y chứa CuSO4 : 0,2- 0,075- 0,05 = 0,075 mol, H2SO4 : 0,125 mol ( bảo toàn nhóm SO42-)
Khi cho 15 gam bột Fe thì xảy ra phản ứng
Fe + H2SO4 → FeSO4 + H2
Fe + CuSO4 → FeSO4 + Cu
Khối lượng chất rắn thu được gồm Cu : 0,075 mol và Fe dư: 15- 0,075. 56- 0,125. 56 = 3,8 gam.
⇒ m = 0,075. 64 +3,8 = 8,6 gam