Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Tính chất giống nhau
- Đều có tính oxi hoá
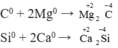
- Đều có tính khử
Tác dụng với phi kim
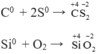
Tác dụng với hợp chất:
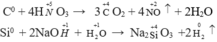

Axit nitric và axit sunfuric đặc đều có tính oxi hóa mạnh.
Ví dụ: 3FeO +10HNO3 —> 3Fe(NO3)3 + NO ↓+ 5H2O
2FeO + 4H2SO4 —> Fe2SO4)3 + SO2 + 4H2O
Tuy nhiên nếu như HNO3 loãng vẫn có tính oxi hóa thì H2SO4 loãng lại không có tính oxi hóa. Ví dụ
3Fe3O4 + 28HNO3 l -> 9Fe(NO3)3 + NO↓+ 14H2O Fe3O4 + 4H2SO4 l —> FeSO4 + Fe2(S04)3 + 4H2O

CH3CH2CH2OH \(\underrightarrow{H_2SO_{4đ}}\) CH3CH=CH2 + H2O
CH3CH(OH)CH3 \(\underrightarrow{H_2SO_{4đ}}\) CH3CH=CH2 + H2O
=> alkene sinh ra khi đun propan-1-ol và propan-2-ol với dung dịch sulfuric acid đặc ở nhiệt độ thích hợp đều là CH3CH=CH2.

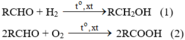
Trong (1), anđehit đóng vai trò là chất oxi hoá
Trong (2), anđehit đóng vai trò là chất khử.

Lấy mỗi chất một ít ra các ống nghiệm tương ứng có đánh số từ 1 đến 4:
1- Cho quỳ tím vào 4 lọ mẫu thử đã đánh số => Lọ chứa Axit etanoic sẽ đổi màu quỳ tím thành đỏ
2- Tiếp tục cho 3 lọ còn lại phản ứng hóa học với Dd AgNO3/NH3, có xúc tác t0 => Lọ chứa Propanal sẽ có kết tủa màu trắng
CH3-CH2CHO + 2AgNO3 + 3NH3 + H2O → CH3-CH2COONH4 + 2Ag↓ + 2NH4NO3
3- Cho vào 2 lọ còn lại vài giọt Dd Br2 => Lọ chứa Stiren sẽ làm mất màu Dd Br2
C6H5CH=CH2 + Br2 →C6H5CHBr -CH2Br
4- Lọ còn lại là Etanol
Lấy mẫu thử: Lấy mỗi chất một ít ra các ống nghiệm tương ứng có đánh số từ 1 đến 4 :
| Axit etanoic | Etanol | Propanal | Stiren | |
| Quỳ tím | Đỏ | \(-\) | \(-\) | \(-\) |
| Dd AgNO3/NH3,to | \(\times\) | \(-\) | \(\downarrow\)Trắng | \(-\) |
| Dd Br2 | \(\times\) | \(-\) còn lại | \(\times\) | mất màu dd Br2 |
PTHH:
CH3\(-\)CH2CHO + 2AgNO3 + 3NH3 + H2O \(\underrightarrow{t}\) CH3\(-\)CH2COONH4 + 2Ag + 2NH4NO3
C6H5CH\(=\)CH2 + Br2 \(\rightarrow\) C6H5CHBr\(-\)CH2Br

CH3OH \(\underrightarrow{H_2SO_{4đ}}\) CH3-O-CH3 + H2O
2C2H5OH \(\underrightarrow{H_2SO_{4đ}}\) C2H5-O-C2H5 + H2O
CH3OH + C2H5OH\(\underrightarrow{H_2SO_{4đ}}\) CH3-O-C2H5 + H2O
-acid sunfuric loãng là axit mạnh:
Fe+H2SO4(l)→FeSO4+H2��+�2��4(�)→����4+�2
Zn+H2SO4(l)→ZnSO4+H2��+�2��4(�)→����4+�2
Ba(OH)2+H2SO4→BaSO4+2H2O
acid sunfuric đặc có tính oxi hóa mạnh:
2Fe+6H2SO4(đ)→Fe2(SO
- Tính acid:
Zn + H2SO4 → ZnSO4 + H2
CuO + H2SO4 → CuSO4 + H2O
Ba(OH)2 + H2SO4 → BaSO4 + 2H2O
CaCO3 + H2SO4 → CaSO4 + CO2 + H2O
- Tính oxi hóa mạnh:
Cu + 2H2SO4 đặc, nóng → CuSO4 + SO2 + 2H2O
- Tính háo nước:
C12H22O11 —> 12C + 11H2O H2SO4→H2SO4
2SO4→H2SO412CH2SO4→H2SO4m
H2SO4→H2SO4