Thủy phân hoàn toàn 42,38 gam hỗn hợp X gồm hai triglixerit mạch hở trong dung dịch KOH 28% (vừa đủ), cô cạn dung dịch sau phản ứng, thu được phần hơi Y nặng 26,2 gam và phần rắn Z. Đốt cháy hoàn toàn Z thu được K2CO3 và 152,63 gam hỗn hợp CO2 và H2O. Mặt khác, cho 0,15 mol X vào dung dịch Br2 trong CCl4, số mol Br2 phản ứng là
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Chọn A.
Vì Y, Z có mạch cacbon không phân nhánh nên số chức este tối đa là 2.
Khi nung F với vôi tôi xút thì:
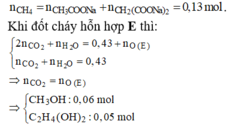
Hỗn hợp X gồm (CH3COO)2C2H4 (0,05 mol) và CH2(COOCH3)2 (0,03 mol) Þ %mZ = 64,38%

Chọn A.
Vì Y, Z có mạch cacbon không phân nhánh nên số chức este tối đa là 2.
Khi nung F với vôi tôi xút thì: n C H 4 = n C H 3 C O O N a + n C H 2 ( C O O N a ) 2 = 0 , 13 m o l
Khi đốt cháy hỗn hợp E thì: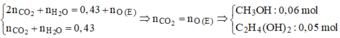
Hỗn hợp X gồm (CH3COO)2C2H4 (0,05 mol) và CH2(COOCH3)2 (0,03 mol) Þ %mZ = 64,38%

Chọn A.
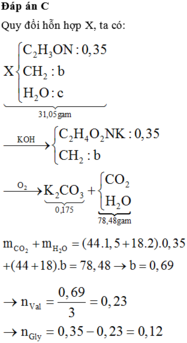
Quy đổi hỗn hợp thành C2H3ON (x mol), CH2 (y mol), H2O.Ta có:
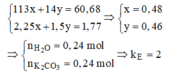 : X, Y, Z đều là đipeptit.
: X, Y, Z đều là đipeptit.
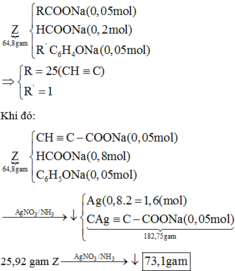
Hỗn hợp muối gồm GlyK: 0,25 mol và AK (A là C4H9O2N): 0,23 mol
Khi đó E gồm X: Gly-Gly (0,06 mol); Y: Gly-A (0,13 mol); Z: A-A (0,05 mol) Þ %mY = 54,56%

Chọn đáp án A
đốt m gam X dạng C n H 2 n O 2 + 0 , 155 m o l O 2 → t 0 0 , 13 m o l C O 2 + 0 , 13 m o l H 2 O
(có n H 2 O = n C O 2 = 0 , 13 m o l do đốt X là hỗn hợp este no, đơn chức, mạch hở).
• bảo toàn nguyên tố O có n X = 1 2 ∑ n O t r o n g X = ( 0 , 13 × 3 - 0 , 155 × 2 ) ÷ 2 = 0 , 04 m o l
♦ Thủy phân m g a m X ( 0 , 04 m o l ) + 0 , 06 m o l K O H → 5 , 04 g a m h a i c h ấ t r ắ n + 2 a n c o l đ ồ n g đ ẳ n g k ế t i ế p
► 5,04 gam 2 chất rắn gồm 0,02 mol KOH
→ chất còn lại là 1 muối kali nữa
⇒ Mmuối = (5,04 – 0,02 × 56) ÷ 0,04
= 98 = 15 + 44 + 39
⇒ muối là CH3COOK.
C t r u n g b ì n h = ∑ n C O 2 ÷ n X
= 0,13 ÷ 0,04 = 3,25
→ CTPT của 2 este là C3H6O2 và C4H8O2.
Biết muối
⇒ cấu tạo của 2 este tương ứng là CH3COOCH3 và CH3COOC2H5
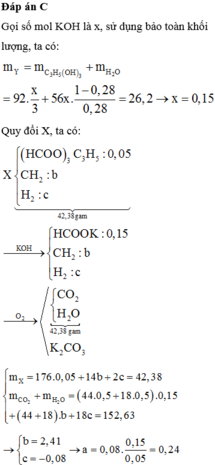

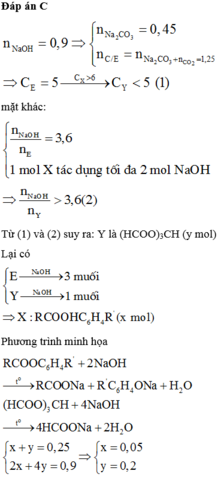
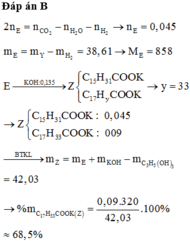

n KOH = a(mol)
=> n glixerol = a/3 (mol)
m dd KOH = 56a/28% = 200a(gam)
=> m H2O = 200a -56a =144a(gam)
Suy ra :
144a + 92 . a/3 = 26,2
=> a = 0,15(mol)
Bảo toàn nguyên tố K :
n K2CO3 = 1/2 n KOH = 0,075(mol)
Bảo toàn khối lượng :
m Z = 42,38 + 0,15.56 - 0,05.92 = 46,18(gam)
m O2 = 152,63 - 46,18 + 0,075.138 = 116,8(gam)
n O2 = 116,8/32 = 3,65(mol)
n COOK = n KOH = 0,15(mol)
Gọi n CO2 = x(mol) ; n H2O = y(mol)
44x + 18y = 152,63
Bảo toàn O : 0,15.2 + 3,65.2 = 2x + y + 0,075.3
=> x = 2,485 ; y = 2,405
n CO2 - n H2O = (k - 1).n Z
<=> 2,485 - 2,405 = (k - 1).0,15
<=> k = 23/15
=> kC=C = 23/15 - 1 = 8/15
Mặt khác :
n Br2 = k.n X = 0,15 . 8/15 . 3= 0,24(mol)