cho sơ đồ phản ứng hoá học Mg cháy trong oxi:Mg+O2=MgO
a) Lập PTHH
b) Tính khối lượng MgO tạo thành khi đốt cháy 0.4 mol Mg
c) tính thể tích khí oxi (ở đktc) đã tham gia phản ứng để tạo ra 20g MgO?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) PTHH: 2Mg + O2 -> 2MgO
b) PT bảo toàn khối lượng: mMg + mO2 = mMgO
c) Theo câu b ta có: mO2 = mMgO - mMg = 15 - 9 = 6(g)
a ) Phương trình hóa học của phản ứng :
2Mg + O2--> 2MgO
b ) Phương trình bảo toàn khối lượng :
mMg + mo2 = mMgO
c ) Tính khối lượng của oxi đã phản ứng :
Áp dụng định luật bảo toàn khối lượng , ta có :
mMg + mo2 = mMgO
9g + mo2= 15g
mo2 = 15g - 9g
mo2 = 6g
=> mo2= 6g

Đáp án A
Ta có dãy chuyển đổi số OXH của S như sau:
![]()
Phản ứng thuộc loại phản ứng oxi hoá-khử khi S thay đổi số ôxi hóa.
Nhưng H2SO4 → SO2 có thể là phản ứng:
![]()
là phản ứng trao đổi

Chọn C. ta có dãy chuyển đổi số OXH của S như sau:
S0 → S-2 → S-2 → S+6 → S+4 → S0 . phản ứng thuộc loại phản ứng oxi hoá-khử khi S thay đổi số ôxi hóa. Nhưng H2SO4 → SO2 có thể là phản ứng: Na2SO3 + H2SO4 → Na2SO4 + H2O + SO2 là phản ứng trao đổi.

TẠI SAAAAAAOOOOOOO!!!!
KHÔNG!!
WHYY >:(((
sao trường tôi ko có giáo án full phép môn khoa hc tự nhiên
TẠI SAO

Đáp án A
Phương trình phản ứng:

Trong tất cả các phản ứng trên, có 4 phản ứng oxi hóa – khử là (1), (2), (5) và (6).

Đáp án A
Phương trình phản ứng :
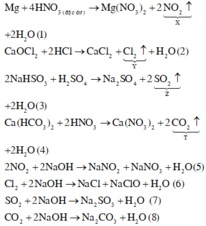
Trong tất cả các phản ứng trên, có 4 phản ứng oxi hóa – khử là (1), (2), (5) và (6).
a, \(2Mg+O_2\underrightarrow{t^o}2MgO\)
b, Theo PT: \(n_{MgO}=n_{Mg}=0,4\left(mol\right)\)
⇒ mMgO = 0,4.40 = 16 (g)
c, \(n_{MgO}=\dfrac{20}{40}=0,5\left(mol\right)\)
Theo PT: \(n_{O_2}=\dfrac{1}{2}n_{MgO}=0,25\left(mol\right)\)
⇒ VO2 = 0,25.22,4 = 5,6 (l)